Содержание
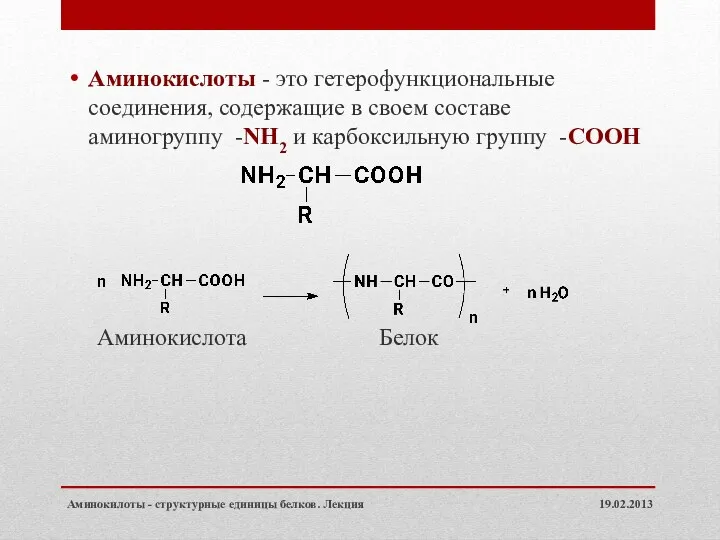
- 2. Аминокислоты - это гетерофункциональные соединения, содержащие в своем составе аминогруппу -NH2 и карбоксильную группу -COOH Аминокислота
- 3. Историческая справка В 1820 г французский ученый Анри Браколио, нагревая кожу, хрящи, сухожилия с водным раствором
- 4. Классификация АК (по положению аминогруппы) В зависимости от положения аминогруппы различают α, β, γ, …ε –
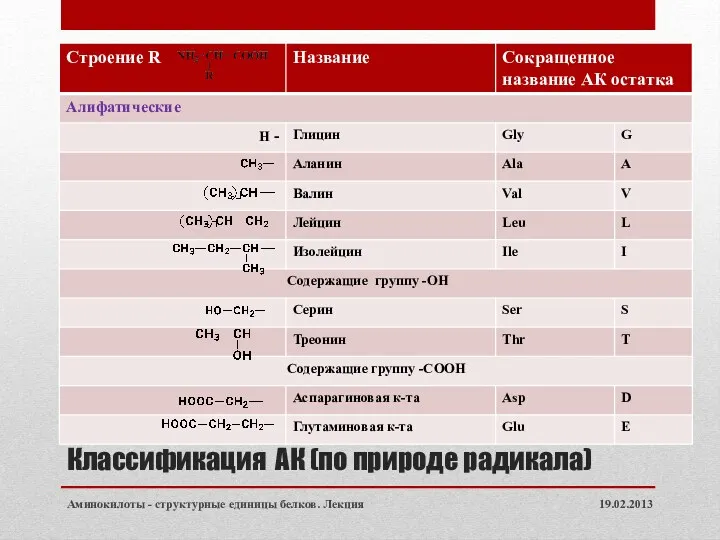
- 5. Классификация АК (по природе радикала) 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 6. Классификация АК (по природе радикала) 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
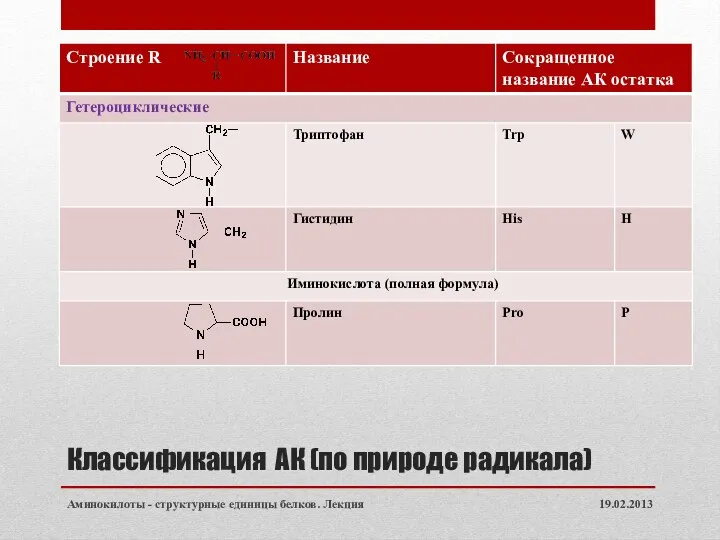
- 7. Классификация АК (по природе радикала) 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
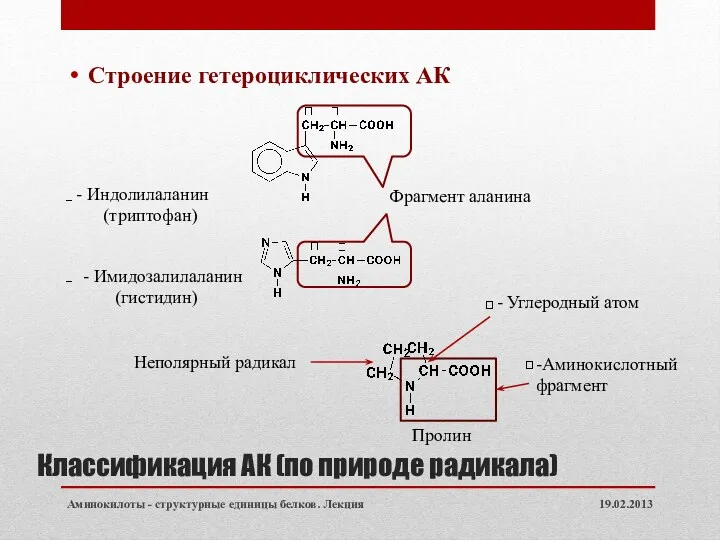
- 8. Классификация АК (по природе радикала) Строение гетероциклических АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция Фрагмент
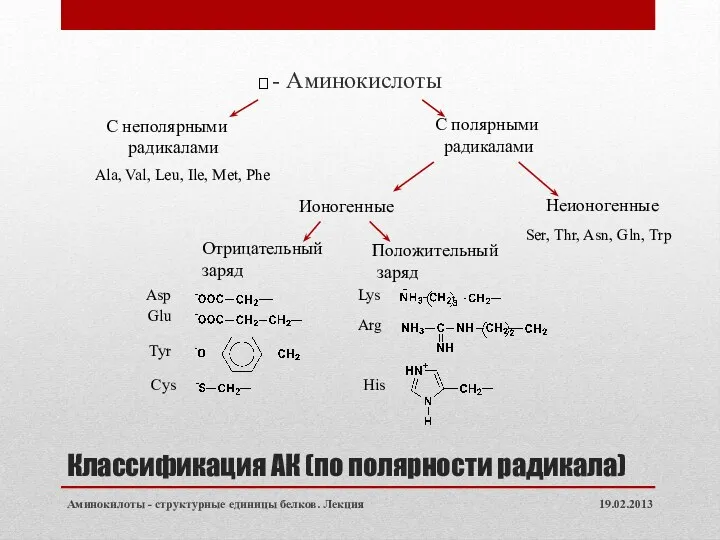
- 9. Классификация АК (по полярности радикала) - Аминокислоты 19.02.2013 Аминокилоты - структурные единицы белков. Лекция С неполярными
- 10. Классификация АК (по биологической функции) - Аминокислоты 19.02.2013 Аминокилоты - структурные единицы белков. Лекция Заменимые Незаменимые
- 11. Стереоизомерия АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция L- -аминокислота D- -аминокислота L - изолейцин
- 12. Некоторые биологически важные АК Некоторые АК, которые не кодируются генами, но образуются, например, в результате пострансляционной
- 13. Некоторые биологически важные АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 14. Кислотно-основные свойства АК Изоэлектрическая точка – pI – значение рН при котором концентрация биполярных ионов максимальна.
- 15. Кислотно-основные свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция Серин Аспарагиновая кислота
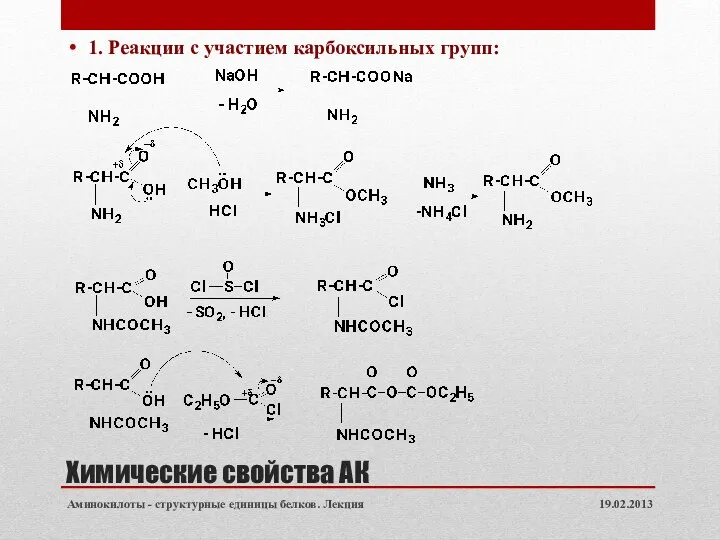
- 16. Химические свойства АК 1. Реакции с участием карбоксильных групп: 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
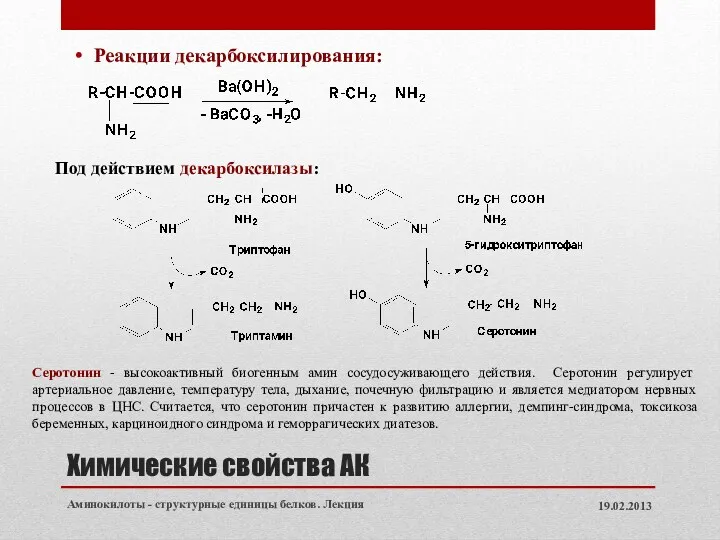
- 17. Химические свойства АК Реакции декарбоксилирования: 19.02.2013 Аминокилоты - структурные единицы белков. Лекция Серотонин - высокоактивный биогенным
- 18. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция Гистамин оказывает широкий спектр биологического действия.
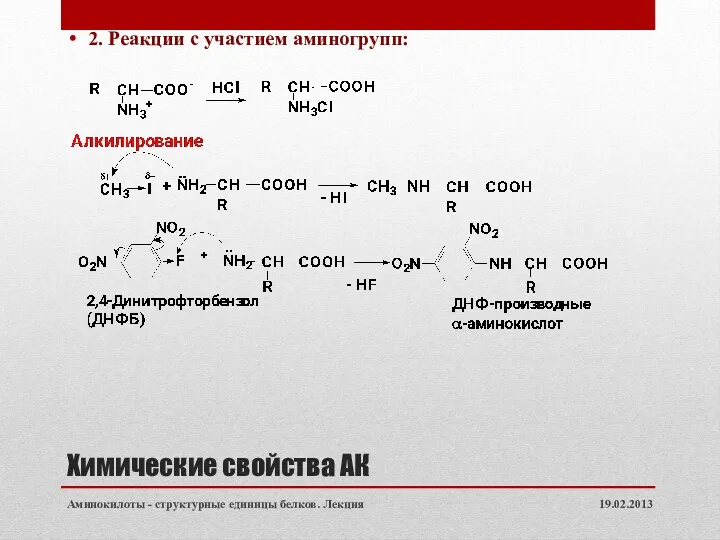
- 19. Химические свойства АК 2. Реакции с участием аминогрупп: 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 20. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 21. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция Фенилтиогидантоиновое производное АК (ФТГ-производное АК) ФИТЦ
- 22. Химические свойства АК Реакции дезаминирования: 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 23. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция В животных тканях Г. Эйлером открыт
- 24. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция В животных тканях и печени человека
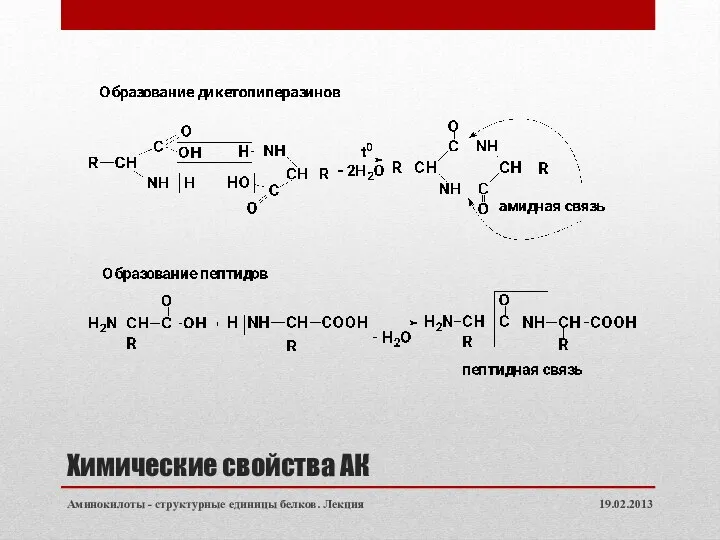
- 25. Химические свойства АК 3. Реакции с участием и карбоксильных и аминогрупп: 19.02.2013 Аминокилоты - структурные единицы
- 26. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 27. Химические свойства АК 4. Реакции с участием боковой цепи: 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
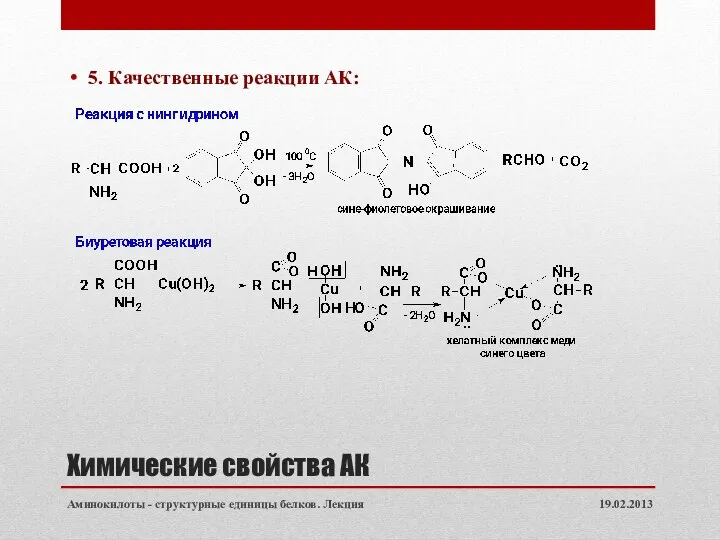
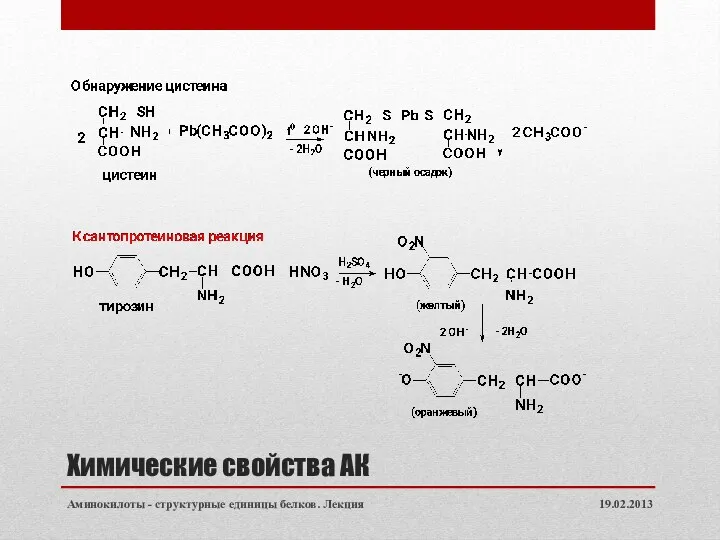
- 28. Химические свойства АК 5. Качественные реакции АК: 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 29. Химические свойства АК 19.02.2013 Аминокилоты - структурные единицы белков. Лекция
- 31. Скачать презентацию

















 Етилен і ацетилен – ненасичені вуглеводні
Етилен і ацетилен – ненасичені вуглеводні Химия лекция (вебинар)
Химия лекция (вебинар) Алкины. 10 класс
Алкины. 10 класс Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи Химическая организация клетки. Неорганические вещества, входящие в состав клетки
Химическая организация клетки. Неорганические вещества, входящие в состав клетки Положение в ПСХЭ и строение атома
Положение в ПСХЭ и строение атома Топаз. Хімічна формула топаза
Топаз. Хімічна формула топаза Атомно-кристаллическое строение материалов
Атомно-кристаллическое строение материалов Полимеры. Протезы трахеи
Полимеры. Протезы трахеи Seminar on kesterites
Seminar on kesterites Органикалық химияға кіріспе. Органикалық заттардың ерекшеліктері
Органикалық химияға кіріспе. Органикалық заттардың ерекшеліктері Классификация органических соединений. Урок химии в 10 классе
Классификация органических соединений. Урок химии в 10 классе Хромопротеиды: биологическая роль. Синтез и распад гема. Метаболизм билирубина
Хромопротеиды: биологическая роль. Синтез и распад гема. Метаболизм билирубина Введение в химию. 8 класс
Введение в химию. 8 класс Галогены. Применение галогенов и их соединений
Галогены. Применение галогенов и их соединений Фосфор и его соединения
Фосфор и его соединения Магний и кальций
Магний и кальций Признаки химических реакций
Признаки химических реакций Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Прикладная химия. Теплоперенос в химических реакторах и теплообменники
Прикладная химия. Теплоперенос в химических реакторах и теплообменники Гетерогенные процессы и равновесия
Гетерогенные процессы и равновесия Періодичний закон. Хімія. 8 клас
Періодичний закон. Хімія. 8 клас Метанол, етанол та їхнє застосування
Метанол, етанол та їхнє застосування Гидролиз солей. Лекция №9
Гидролиз солей. Лекция №9 Химия и пища
Химия и пища Металлические стёкла
Металлические стёкла Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості Ion exchange
Ion exchange