Слайд 2

План лекции:
Понятие о хромопротеинах, их классификация.
Строение и функции гемопротеинов.
Биосинтез гема.
Распад гемопротеинов.
Клинико-биохимические
аспекты метаболизма гемопротеинов.
Слайд 3

1. Понятие о хромопротеинах, их классификация.
Белки бывают простые и сложные. У
сложных белков имеется небелковая часть – простетическая группа.
Слайд 4

Хромопротеины – это сложные белки, содержащие окрашенную простетическую группу. По этой
причине молекулы хромопротеинов окрашены в определённый цвет (chromos - краска).
Слайд 5

В природе известны следующие виды хромопротеинов:
магнийпорфирины (хлорофилл)
флавопротеины (рибофлавин)
гемопротеины (гем)
Слайд 6

Магнийпорфирины – это зелёные хлорофилл содержащие белки. Они образуются в растениях
и сине-зелёных водорослях.
Слайд 7
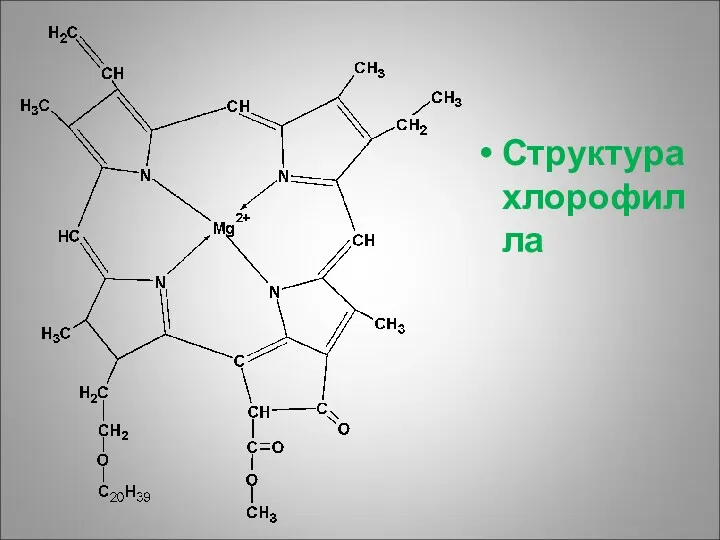
Структура хлорофилла
Слайд 8

Их функция – это преобразование солнечной энергии в энергию макроэргических связей
АТФ. Кроме того, именно хлорофилл инициирует реакцию фотохимического разложения воды:
2Н2О → О2 + 4Н+ + 4ē
Благодаря этой реакции в атмосферу постоянно выделяется кислород, а для растений О2 – всего лишь побочный продукт.
Слайд 9

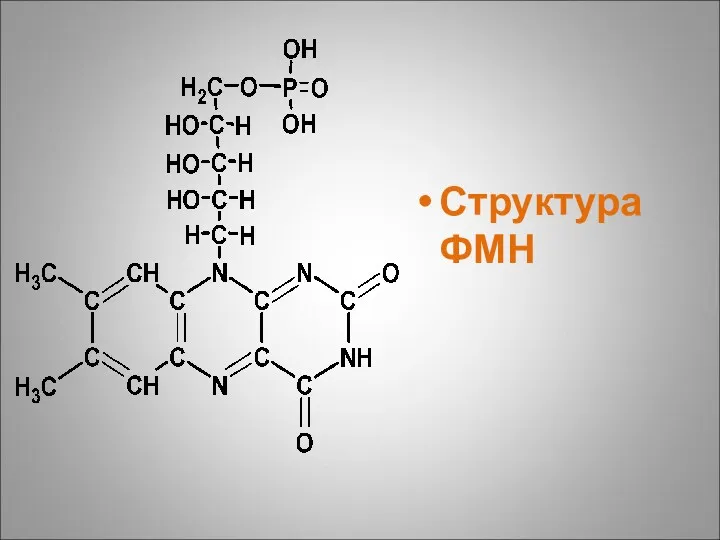
Флавопротеины
Это жёлтые белки, содержащие рибофлавин. Все они являются ферментами класса оксидоредуктаз.
Играют большую роль в реакциях окислительного метаболизма.
Нам они известны, как ФМН- и ФАД-зависимые дегидрогеназы. Для образования флавопротеинов организму животных требуется поступление в достаточном количестве витамина В2 – рибофлавина.
Слайд 10
Слайд 11

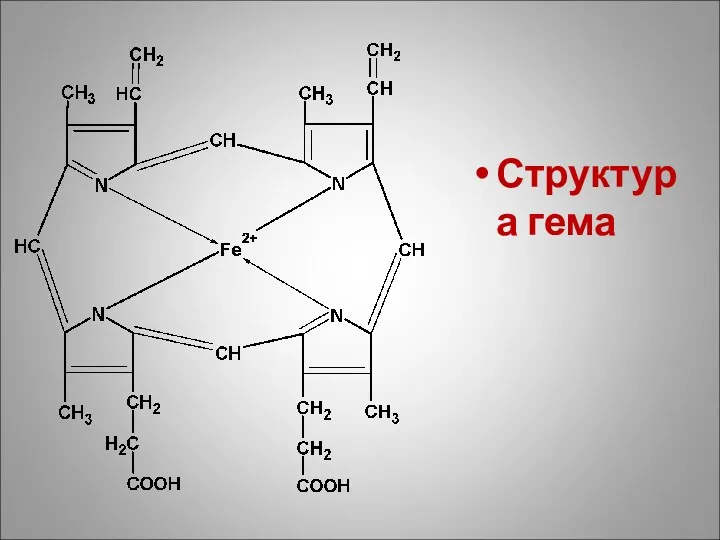
Гемопротеины
В состав гемопротеинов входит гем, который придаёт им красное окрашивание.
Гем –
тетрапиррольный цикл, содержащий ион двухвалентного железа.
Слайд 12
Слайд 13

2. Строение и функции гемопротеинов.
Гемопротеины подразделяются на:
Дыхательные белки (гемоглобин, миоглобин)
Ферменты
Слайд 14
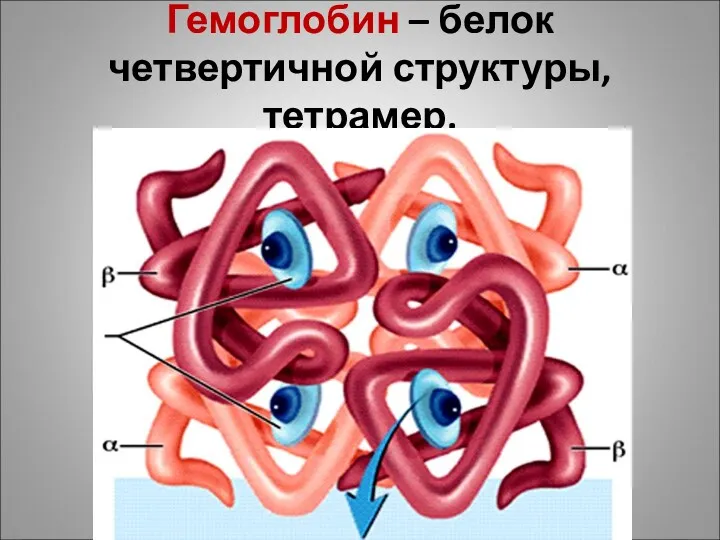
Гемоглобин – белок четвертичной структуры, тетрамер.
Слайд 15

Два олигомера α-цепей состоят из 141 аминокислотных остатка, и два олигомера
β-цепей – из 146 аминокислотных остатка.
Каждая субъединица нековалентно связана с гемом. В одной молекуле гемоглобина содержится 4 гема.
Молекулярная масса гемоглобина составляет около 68 000. В одном эритроците насчитывается до 340 млн. молекул гемоглобина.
Слайд 16

Атом железа в гемоглобине может быть в состоянии Fe2+ или Fe3+,
но только Fe2+ способен переносить кислород. Связывая кислород, атом железа не меняет степени окисления.
Процесс связывания гемоглобина с кислородом называется оксигенацией. Одна молекула гемоглобина способна переносить 4 молекулы кислорода. Оксигенированный гемоглобин называют оксигемоглобином.
Слайд 17

Гемоглобин способен транспортировать и углекислый газ – от тканей к лёгким
(в виде карбогемоглобина). Но углекислый газ присоединяется к свободным аминогруппам молекулы глобина, а не к гему.
Слайд 18

Очень высокое сродство гемоглобина к окиси углерода (СО). При их взаимодействии
образуется устойчивая молекула карбоксигемоглобина. Она теряет способность к транспорту кислорода.
Гемоглобин в присутствии некоторых токсикантов окисляется до метгемоглобина (Fe3+), который также теряет транспортную функцию.
Слайд 19

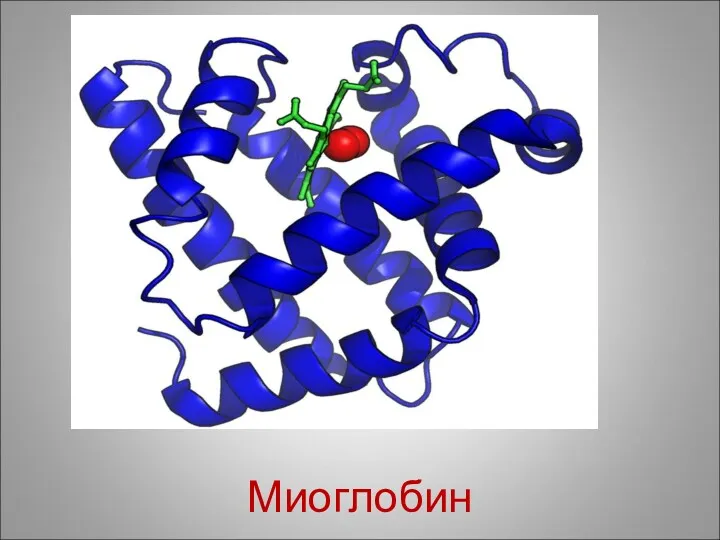
Миоглобин
Миоглобин (молекулярная масса 16 000, состоит из 153 аминокислот) имеет третичную структуру,
одну полипептидную цепь, один гем и может связывать одну молекулу кислорода.
Функция миоглобина заключается в создании в мышцах кислородного резерва, который расходуется по мере необходимости, восполняя временную нехватку кислорода.
Слайд 20
Слайд 21

Гем-содержащие ферменты
Если в составе дыхательных гемопротеинов степень окисления железа не меняется,
то в составе ферментов обязательно проявляется переменная степень окисления железа. Это необходимо для переноса электронов.
Все гем-содержащие ферменты относятся к окислительно-восстановительным (класс оксидоредуктаз).
Слайд 22

Важнейшие гем-содержащие ферменты:
каталаза
цитохромы
пероксидазы
Слайд 23

Слайд 24

Гем синтезируется во всех тканях, но с наибольшей скоростью в костном
мозге и печени.
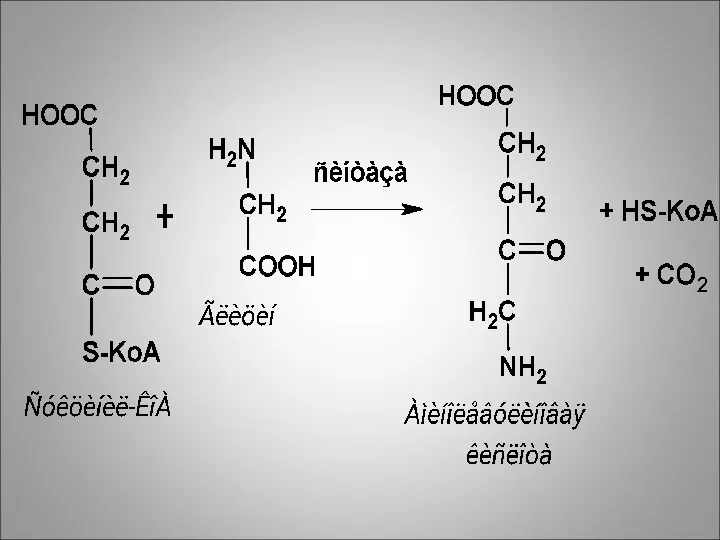
Первая реакция синтеза гема - образование 5-аминолевулиновой кислоты из глицина и сукцинил-КоА идёт в матриксе митохондрий.
Реакцию катализирует фермент аминолевулинатсинтаза
(содержит витамин В6)
Слайд 25
Слайд 26

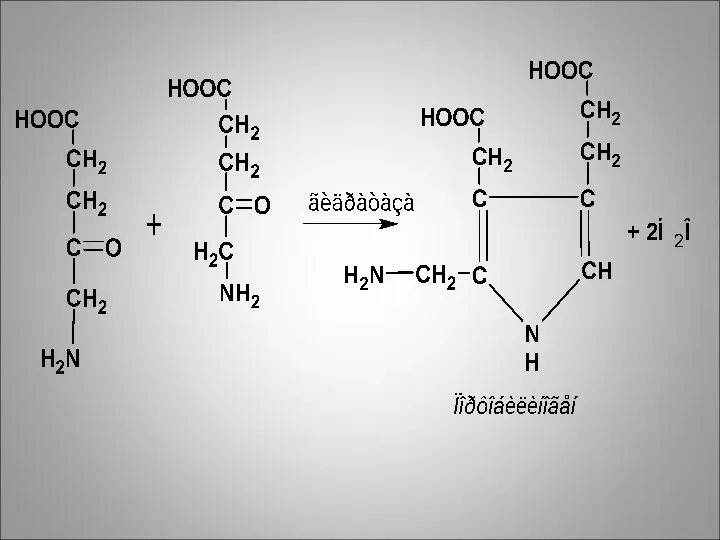
Из митохондрий 5-аминолевулиновая кислота поступает в цитоплазму. В цитоплазме проходят промежуточные
этапы синтеза гема. Рассмотрим следующую реакцию.
Под влиянием аминолевулингидратазы происходит конденсация двух молекул 5-аминолевулиновой кислоты с образованием порфобилиногена и двух молекул воды.
Слайд 27
Слайд 28

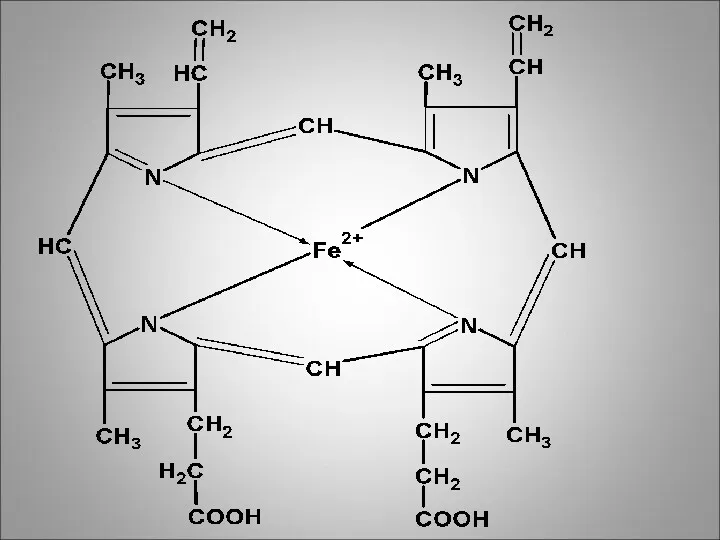
Затем происходит ряд последовательных реакций, в результате которых образуется тетрапиррольный цикл
– протопорфирин. Фермент феррохелатаза, присоединяя к протопорфирину двухвалентное железо, превращает его в гем.
Слайд 29
Слайд 30

Источником железа для синтеза гема служит депонирующий железо белок ферритин. Синтезированный
гем, соединяясь с α и β-полипепептидными цепями глобина, образует гемоглобин.
Гем регулирует синтез глобина: при снижении скорости синтеза гема синтез глобина в ретикулоцитах тормозится.
Слайд 31

Слайд 32

Рассмотрим распад хромопротеинов на примере гемоглобина, который количественно превосходит все другие
белки этой группы.
Продолжительность существования эритроцитов в крови животного составляет 90–120 суток, а затем они разрушаются с освобождением молекул гемоглобина.
Их катаболизм происходит главным образом в ретикулоэндотелиальных клетках селезёнки, лимфатических узлов, костного мозга и печени.
Слайд 33

В течение суток в организме животного разрушается 1–2 % эритроцитов крови.
В одну секунду в организме животного разрушаются 3 млн. эритроцитов крови.
Слайд 34

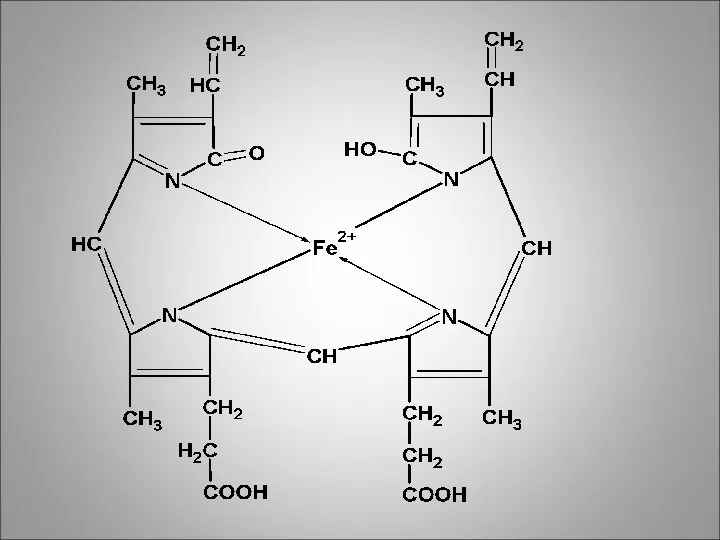
Распад гема начинается с разрыва одного метинового мостика между двумя пиррольными
кольцами с сохранением на этой стадии атома железа, глобина и циклической структуры. Это приводит к получению вердоглобина.
Эта реакция катализируется ферментом гемоксигеназой с участием 2О2 и НАДФН2
Слайд 35
Слайд 36

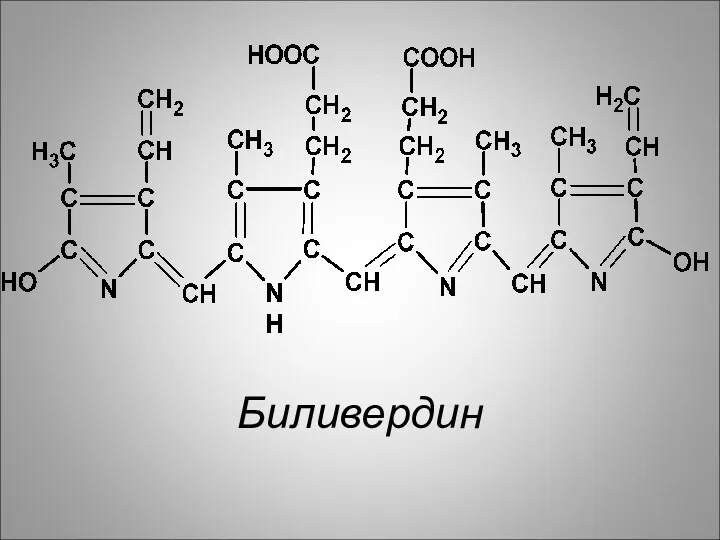
Далее, от вердоглобина отщепляется ион железа и белок глобин. В результате
образуется биливердин, который имеет линейную структуру.
Слайд 37
Слайд 38

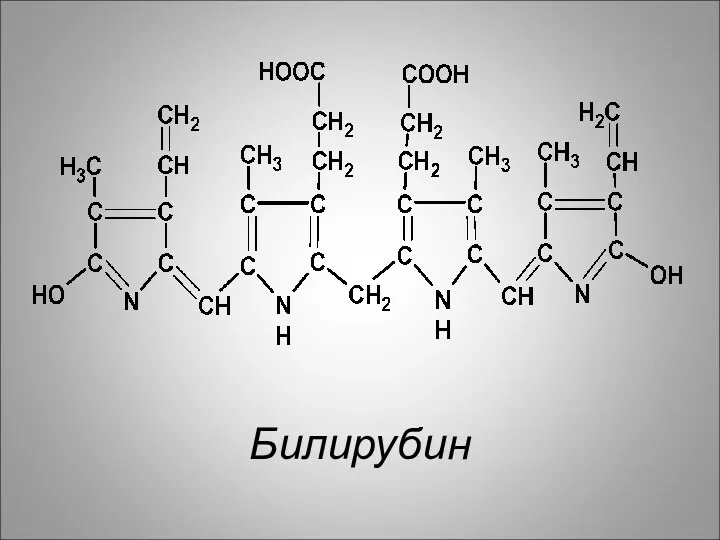
Под влиянием биливердин-редуктазы биливердин при участии НАДФН2 восстанавливается в другой
желчный пигмент – билирубин:
Слайд 39
Слайд 40

Образовавшийся в селезенке билирубин поступает в кровь. Билирубин плохо растворим в
воде, поэтому он связывается с альбумином и транспортируется в печень.
Билирубин в комплексе с альбумином называется свободный (неконъюгирован-ный) или непрямой билирубин. Образование таких комплексов не позволяет выделяться билирубину с мочой.
Слайд 41

Из сосудистого русла в гепатоциты билирубин попадает с помощью белков-переносчиков.
Далее при
участии белка лигандина он транспортируется в ЭПР, где протекает реакция с участием фермента
УДФ-глюкуронилтрансферазы
Билирубин + УДФ-глюкуроновая кислота ?
Билирубин-глюкуронид
Кроме глюкуроновой кислоты, в реакцию могут вступать сульфаты, фосфаты, глюкозиды.
Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин. Он хорошо растворим в воде.
Слайд 42

После конъюгации билирубин секретируются в желчные протоки, в желчный пузырь и
далее в кишечник.
В начальных отделах тонкого кишечника прямой билирубин не всасывается в кровь.
Слайд 43

В подвздошной и ободочной кишках коньюгаты билирубина атакуются бактериями и деконъюгируются.
Бактериальные ферменты восстанавливают билирубин до уробилиногена.
Часть этих продуктов обратно всасывается в кровь, они вновь попадают в печень и реэкскретируется через кишечник.
Лишь 1 – 2 % и них выделяется с мочой. Во внешней среде происходит их окисление кислородом воздуха , в результате образуется уробилин – жёлтый пигмент мочи.
Слайд 44

Уробилиноген в толстом кишечнике с помощью бактериальных ферментов может присоединять четыре
атома водорода и переходить в стеркобилиноген.
Слайд 45

Большая часть метаболитов билирубина выводится из организма через кишечник. Во внешней
среде они окисляются до стеркобилина – пигмента каловых масс.
Слайд 46

5. Клинико-биохимические аспекты метаболизма гемопротеинов.
Слайд 47

Количество гемоглобина в крови животных разных видов (г/л)
Слайд 48

Основные причины снижения концентрации гемоглобина:
Дефицит железа
Дефицит витаминов (В6, В12, фолиевой кислоты)
Кровопотери
Алиментарное
истощение
Почечная недостаточность (терминальная стадия)
Злокачественные новообразования
Слайд 49

Основные причины повышения концентрации гемоглобина:
Обезвоживание
Гипоксия
Слайд 50

Концентрация общего билирубина в крови животных разных видов (мкмоль/л)
Слайд 51

Причины увеличения концентрации билирубина:
Гемолиз эритроцитов (повышается концентрация непрямого билирубина)
Цитолиз гепатоцитов (повышается
в первую очередь прямой билирубин и в меньшей степени непрямой)
Нарушение эвакуации желчи, холестаз (повышается прямой билирубин, непрямой остаётся в норме). Прямой билирубин всасывается в кровь из желчных протоков и желчного пузыря.
Слайд 52

Если билирубин обнаруживается в моче, то это может быть только прямой
билирубин (непрямой в мочу не фильтруется, так как связан с альбумином)



















































 Удивительные свойства воды
Удивительные свойства воды Electronică aplicată. (Curs 2)
Electronică aplicată. (Curs 2) Пространственное строение органических соединений. (Лекция 2)
Пространственное строение органических соединений. (Лекция 2) 20230416_urok_na_20.02.2023
20230416_urok_na_20.02.2023 Неізогіпсичні перетворення функціональних груп. Реакції окиснення
Неізогіпсичні перетворення функціональних груп. Реакції окиснення Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Электронная конфигурация К. Классификация химических элементов. 8 класс
Электронная конфигурация К. Классификация химических элементов. 8 класс Спирты. Физические и химические свойства
Спирты. Физические и химические свойства Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування
Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування 20230321_obobshchenie_po_elektroliticheskoy_dissotsiatsii
20230321_obobshchenie_po_elektroliticheskoy_dissotsiatsii Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Типовые процессы технологии неорганических веществ. (Тема 3)
Типовые процессы технологии неорганических веществ. (Тема 3) ЕГЭ Химия. Задание №5
ЕГЭ Химия. Задание №5 Изучение строения и свойств глюкозы
Изучение строения и свойств глюкозы Железо и его соединения
Железо и его соединения Химические превращения веществ
Химические превращения веществ Белки. Функции белков
Белки. Функции белков Високомолекулярні сполуки. Полімери
Високомолекулярні сполуки. Полімери Простые спектры 1Н ЯМР
Простые спектры 1Н ЯМР Значення хімічних процесів у природі
Значення хімічних процесів у природі Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас
Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас Реакции ионного обмена
Реакции ионного обмена Жиры. Мыла. 10 класс
Жиры. Мыла. 10 класс Группа редкоземельных элементов
Группа редкоземельных элементов Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі
Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі Железо
Железо Crystallography. Part 4: Crystal Forms Twinning
Crystallography. Part 4: Crystal Forms Twinning Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)