Слайд 2

Алкины
Ацителен – первый представитель алкинов - С2Н2
Алкины - углеводороды, содержащие тройную
связь между атомами углерода.
Общая формула - …
Слайд 3
Алкины
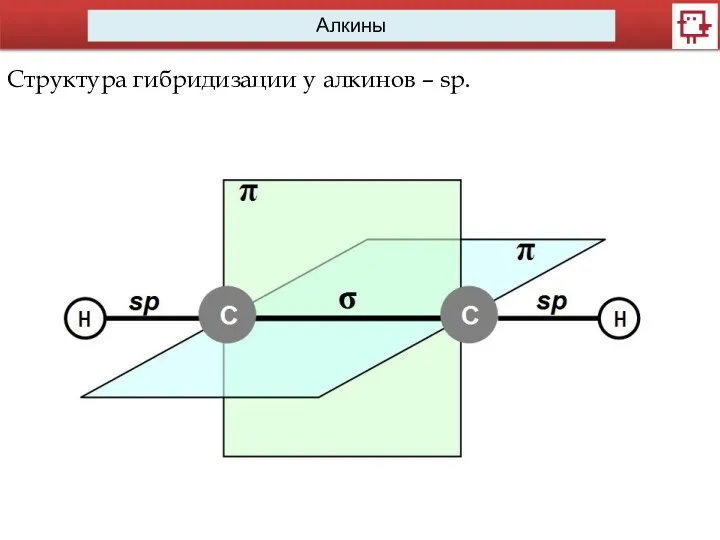
Структура гибридизации у алкинов – sp.
Слайд 4
Алкины
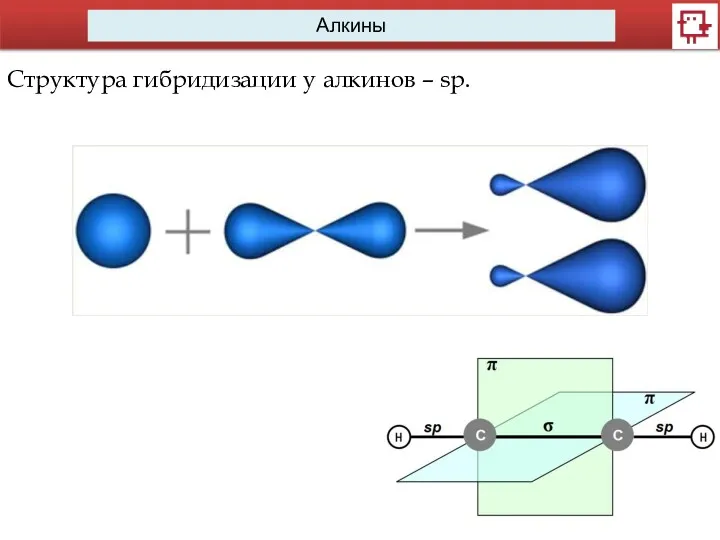
Структура гибридизации у алкинов – sp.
Слайд 5

Алкины
Номенклатура.
Названия совпадают с аналогичными для предельных углеводородов, только суффикс –ан,
заменяется на –ин.
Слайд 6

Алкины
Получение.
В лаборатории ацетилен получают при взаимодействии карбида кальция с водой:
CaC2 +
2H2O = C2H2 + Ca(OH)2
В промышленности делают многоступенчатый процесс:
CH4 = C + 2H2
2CH4 = C2H2 + 3H2
C2H2 = 2C + H2
Слайд 7

Алкины
Химические свойства.
Реакции присоединения.
С галогенами:
С водородом, при нагревании и в
присутствии катализатора (Ni, Pl, Pd):
С водой (реакция Кучерова):
Слайд 8
Алкины
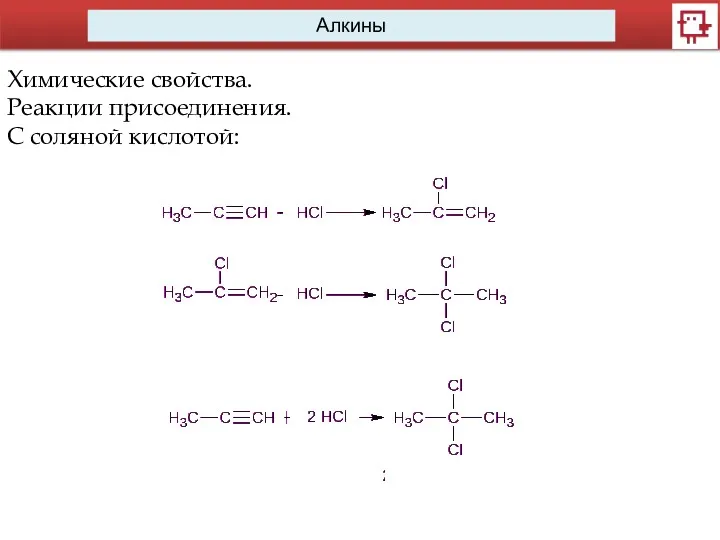
Химические свойства.
Реакции присоединения.
С соляной кислотой:
Слайд 9

Алкины
Химические свойства.
Реакции присоединения.
С соляной кислотой:
Слайд 10
Алкины
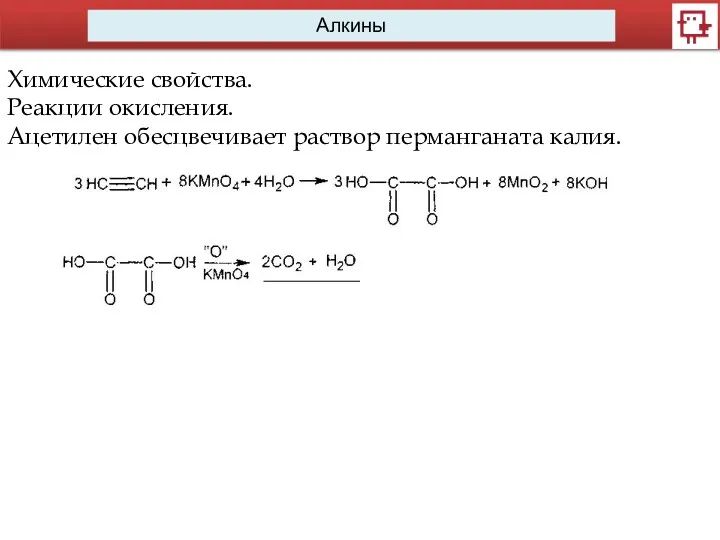
Химические свойства.
Реакции окисления.
Ацетилен обесцвечивает раствор перманганата калия.
Слайд 11

Алкины
Химические свойства.
Реакции окисления.
Горение на воздухе:
! Ацетилен взрывоопасен, поэтому его хранят
и транспортируют в баллонах в виде ацетоновых растворов, которым пропитаны пористые материалы!
2С2Н2 + О2 = 4СО2 + 2Н2О
Слайд 12
Алкины
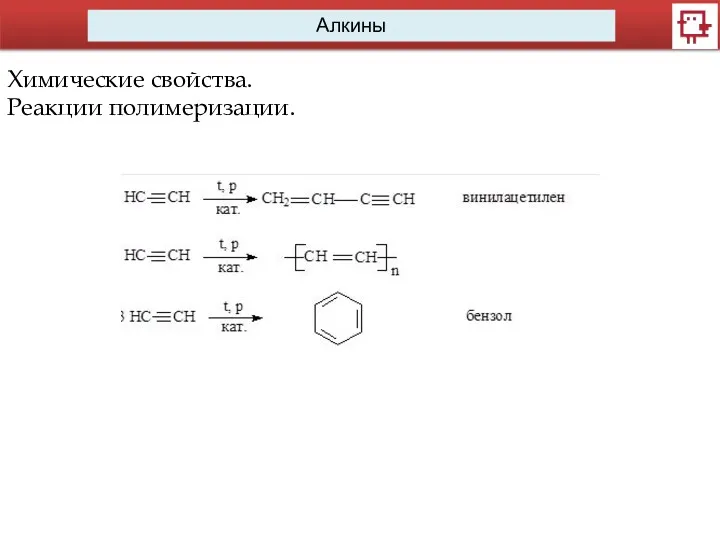
Химические свойства.
Реакции полимеризации.
Слайд 13
Алкины
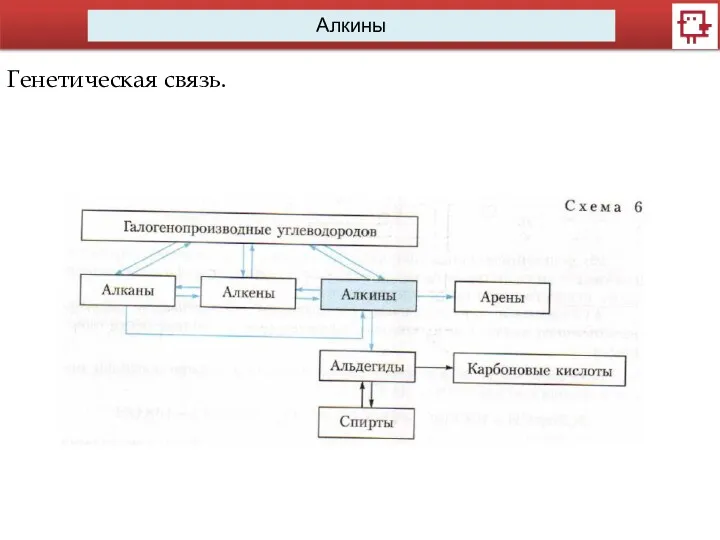
Генетическая связь.












 Сполуки неметалічних елементів з Гідрогеном. Особливості водних розчинів цих сполук, їх застосування
Сполуки неметалічних елементів з Гідрогеном. Особливості водних розчинів цих сполук, їх застосування Катионы IV аналитической группы
Катионы IV аналитической группы Строение атома и периодический закон. (Тема 2)
Строение атома и периодический закон. (Тема 2) Қазақстанда химияны оқыту әдістемесінің даму тарихы
Қазақстанда химияны оқыту әдістемесінің даму тарихы Химическая промышленность
Химическая промышленность Функціональні похідні аліфатичних вуглеводнів галогенопохідні вуглеводнів
Функціональні похідні аліфатичних вуглеводнів галогенопохідні вуглеводнів Природній та супутній нафтові гази, їх склад, використання
Природній та супутній нафтові гази, їх склад, використання Кислород/водород. Повторение
Кислород/водород. Повторение Лаборатория красивых волос
Лаборатория красивых волос Аммиак (9 класс)
Аммиак (9 класс) ферментер
ферментер Гидролиз солей
Гидролиз солей Химические свойства и получение алканов
Химические свойства и получение алканов Механическая смесь и растворы
Механическая смесь и растворы Химическая связь и ее типы. Кристаллические решётки
Химическая связь и ее типы. Кристаллические решётки Массовая доля элемента в веществе
Массовая доля элемента в веществе Цинк и его применение
Цинк и его применение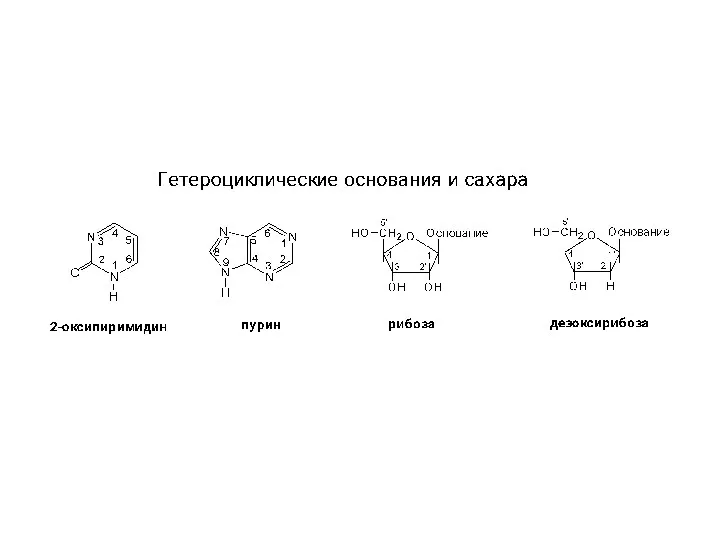 Структура гетероциклов, нуклеозидов и нуклеотидов
Структура гетероциклов, нуклеозидов и нуклеотидов Химические уравнения Закон сохранения массы веществ
Химические уравнения Закон сохранения массы веществ Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Пластические массы и изделия на их основе
Пластические массы и изделия на их основе Химические уравнения
Химические уравнения p-элементы 17 группы периодической системы: галогены
p-элементы 17 группы периодической системы: галогены Химия и проблемы экологии. Кислотные дожди
Химия и проблемы экологии. Кислотные дожди Тотығу-тотықсыздану титрлеу әдісі
Тотығу-тотықсыздану титрлеу әдісі Химическая связь в кластерах
Химическая связь в кластерах Карбоновые кислоты и их функциональные производные. Хроматографические методы исследования
Карбоновые кислоты и их функциональные производные. Хроматографические методы исследования Ionic polymerization
Ionic polymerization