Содержание
- 2. Карбоновые кислоты – это производные углеводородов , в состав молекул которых входит одна или несколько карбоксильных
- 3. В зависимости от числа карбоксильных групп в составе одной молекулы различают: Одноосновные Классификация
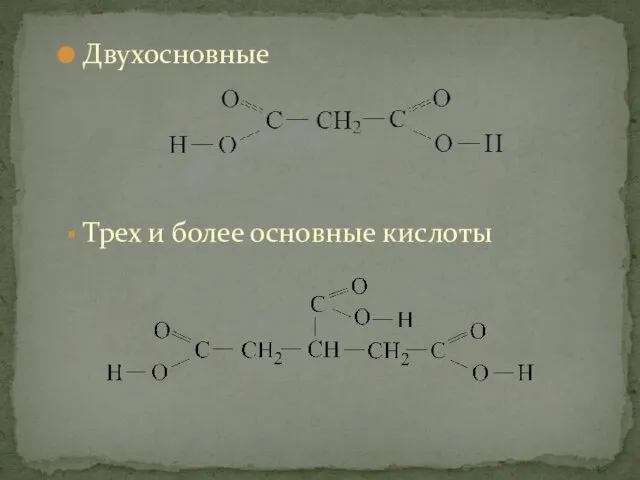
- 4. Двухосновные Трех и более основные кислоты
- 5. Номенклатура
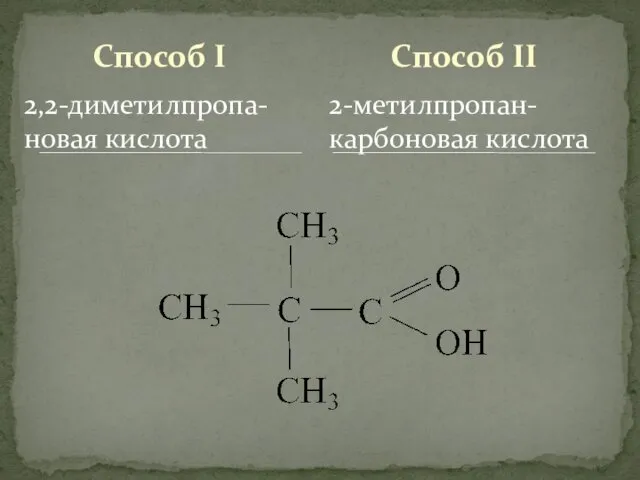
- 7. Способ I 2,2-диметилпропа-новая кислота 2-метилпропан-карбоновая кислота Способ II
- 8. При образовании названий карбо-новых кислот положение радикалов обо-значают буквами греческого алфавита (α, β, γ, δ, ε
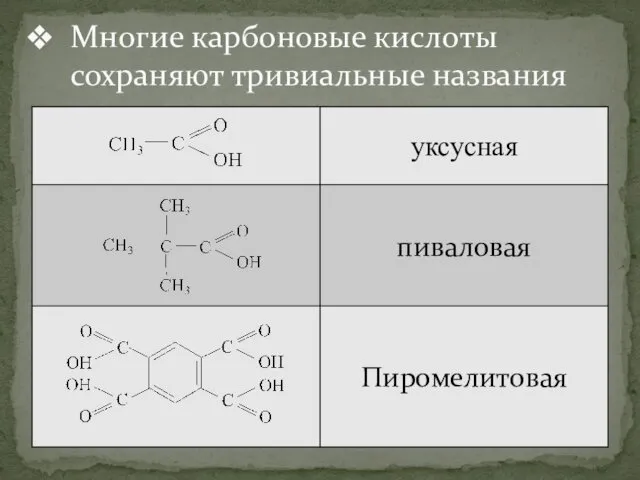
- 9. Многие карбоновые кислоты сохраняют тривиальные названия
- 10. Одноосновные насыщенные (предельные) карбоновые кислоты
- 13. Изомерия насыщенных карбоновых кислот определяется строением углеводородного радикала (или структурная изомерия) Изомерия
- 14. Глубокое окисление первичных спиртов Гидролиз нитрилов Способы получения:
- 15. Гидролиз сложных эфиров глицерина (жиров). Реакция широко применяется для получения высокомолекулярных (С14 – С22) карбоновых кислот.
- 16. Химическое поведение кислот, в первую очередь, связано с наличием в их молекуле карбоксильной группы, а так
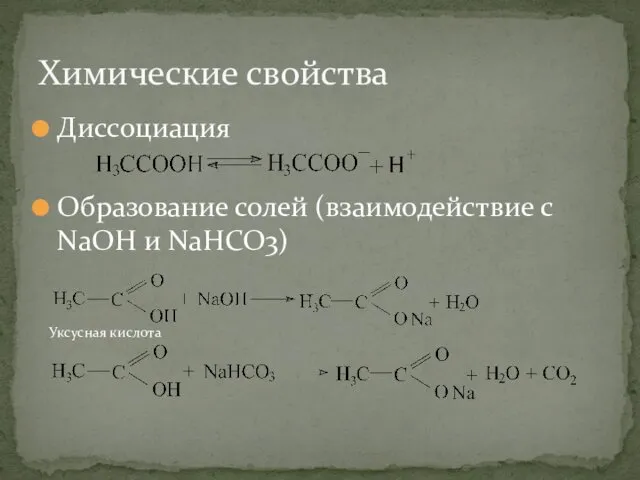
- 17. Диссоциация Образование солей (взаимодействие с NaOH и NaHCO3) Химические свойства
- 18. Образование галогенангидридов (взаимодействие с PCl5, PCl3 или HCl) Образование ангидридов
- 19. Образование сложных эфиров. Реакция этерификации. Образование амидов. Разложение солей аммония.
- 20. Реакции замещения в углеводородном радикале. Галогенирование алифати-ческих кислот в α-положение. Окисление карбоновых кислот. Окисление муравьиной кислоты.
- 21. Окисление карбоновых кислот, имеющих третичный атом углерода в α–положении. Окисление в биологических системах под действием фермента
- 22. Одноосновные ненасыщенные (непредельные) карбоновые кислоты
- 24. Изомерия ненасыщенных карбоновых кислот определяется: строением углеводородного радикала (или структурная изомерия) Положением двойных или тройных связей
- 25. Из галогенкарбоновы кислот (дегидро-галогенирование). Окисление непредельных альдегидов. Способы получения
- 26. Ненасыщенные одноосновные кислоты вступают во все реакции, характерные для кис-лот (образование солей, сложных эфиров, ангид-ридов, галогенангидридов,
- 27. Реакции присоединения (воды, спиртов, аммиака).
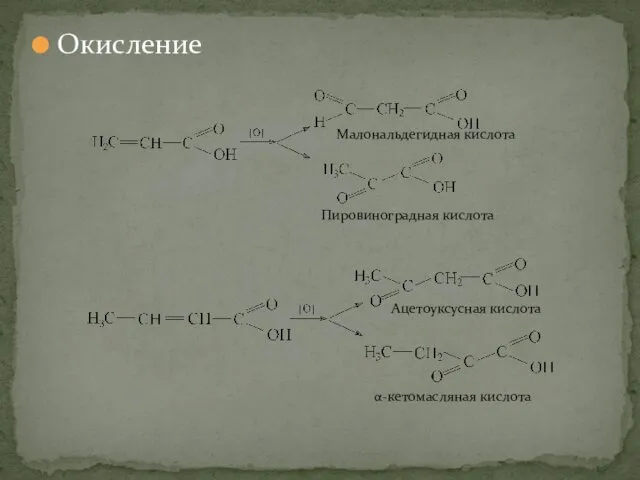
- 28. Окисление
- 29. Полимеризация. наиболее легко полимеризации подвергаются α,β-ненасыщенные монокарбоновые кислоты.
- 30. Отдельные представители. Линолевая кислота (бицис-октадекадиен-9,12-овая кислота) Линоленовая (трицис-октадекатриен-9,12,15-овая кислота)
- 31. Ароматические кислоты
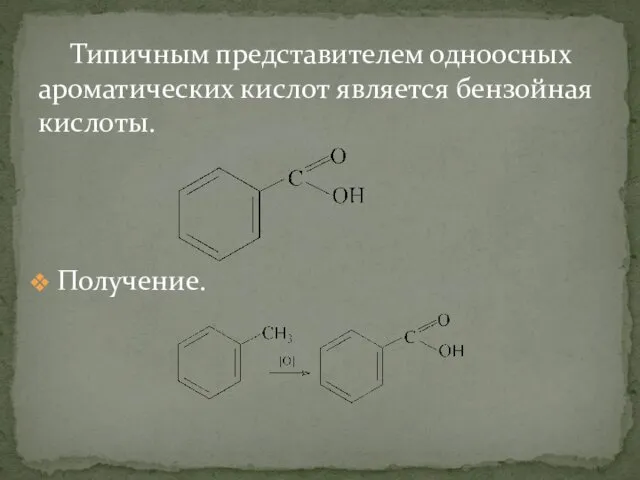
- 32. Типичным представителем одноосных ароматических кислот является бензойная кислоты. Получение.
- 33. Реакции карбоксильной группы. Для аренкарбоновых кислот характерны все реакции насыщенных карбоновых кислот в карбоксильной группе. Химические
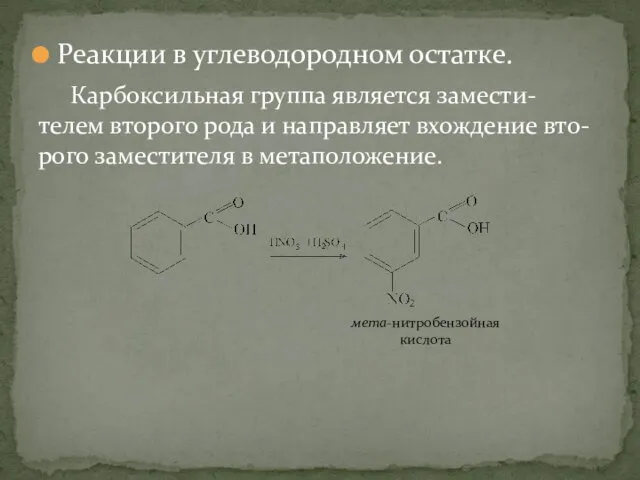
- 34. Реакции в углеводородном остатке. Карбоксильная группа является замести-телем второго рода и направляет вхождение вто-рого заместителя в
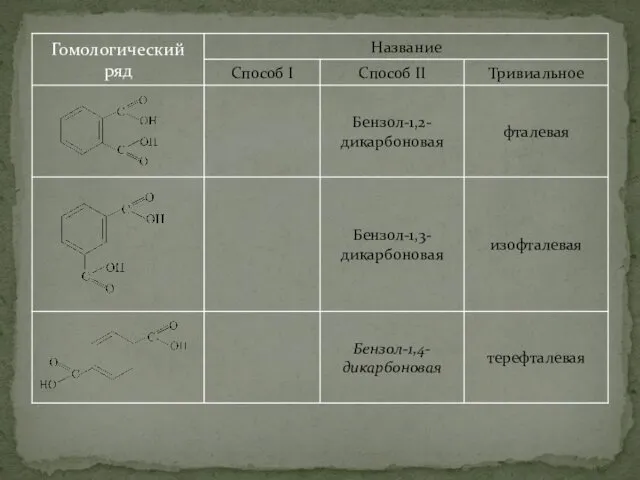
- 35. Двухосновные кислоты
- 38. Структурная изомерия насыщенных али-фатических двухосновных карбоновых кислот. У ненасыщенных кислот имеет место геометрическая изомерия. У ароматических
- 39. Для получения двухосновных кислот используют принципиально те же методы, что и для одноосновных, с той разницей,
- 40. Двухосновные кислоты вступают во все химические реакции, характерные для одноосновных кислот: образование солей, сложных эфиров, ангидридов,
- 42. Скачать презентацию































 Поверхностные явления. Типы поверхностных явлений
Поверхностные явления. Типы поверхностных явлений Графит
Графит Серная кислота и её свойства
Серная кислота и её свойства Оксиды, их классификация и свойства
Оксиды, их классификация и свойства Алкадиены. Строение алкадиенов
Алкадиены. Строение алкадиенов Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Действующие вещества. Лексикон
Действующие вещества. Лексикон Классификация минералов в соответствии с систематикой, утвержденной IMA
Классификация минералов в соответствии с систематикой, утвержденной IMA Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды Кислород. Промышленный способ (перегонка жидкого воздуха)
Кислород. Промышленный способ (перегонка жидкого воздуха) Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества
Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества Гидроочистка нефти и газа
Гидроочистка нефти и газа Поверхностные явления
Поверхностные явления Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Центрифугирование в почвоведении
Центрифугирование в почвоведении Классификация химических реакций (11 класс)
Классификация химических реакций (11 класс) Особливості горіння дисперсних систем
Особливості горіння дисперсних систем Первая группа периодической системы Менделеева. Щелочные металлы
Первая группа периодической системы Менделеева. Щелочные металлы Оптические свойства салических породообразующих минералов (лекция 8)
Оптические свойства салических породообразующих минералов (лекция 8) Альдегиды и кетоны
Альдегиды и кетоны Углеводы. Молекулярные формулы
Углеводы. Молекулярные формулы Трансмиссионные масла
Трансмиссионные масла Атомно-молекулярное учение. (Лекция 1)
Атомно-молекулярное учение. (Лекция 1) Закон постоянства состава
Закон постоянства состава Путешествие на остров Соединений химических элементов. Урок-игра
Путешествие на остров Соединений химических элементов. Урок-игра Кобальт. Химический элемент
Кобальт. Химический элемент 20230306_oni_byli_pervymi
20230306_oni_byli_pervymi