Содержание
- 2. 1. Поверхностные явления 1.1. Типы поверхностных явлений Поверхностное натяжение Поверхностные плёнки Расклинивающее давление (Дерябин) Смачивание поверхности,
- 3. 3.1. Типы поверхностных явлений 3.1.1. Поверхностное натяжение
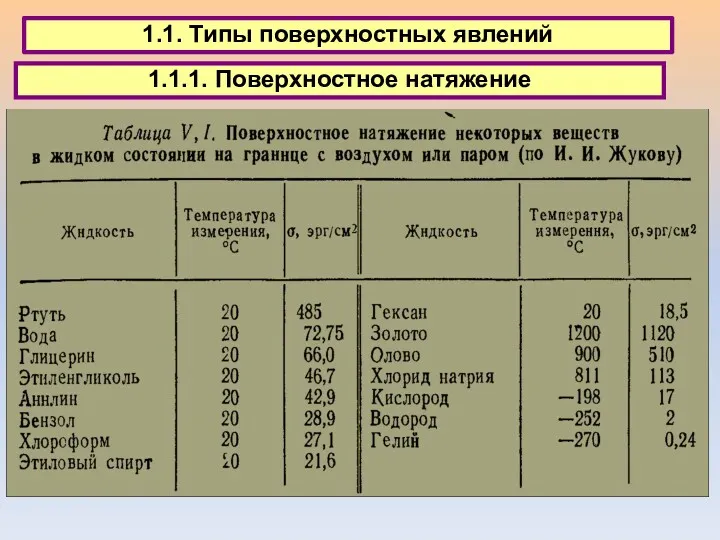
- 4. 1.1. Типы поверхностных явлений 1.1.1. Поверхностное натяжение
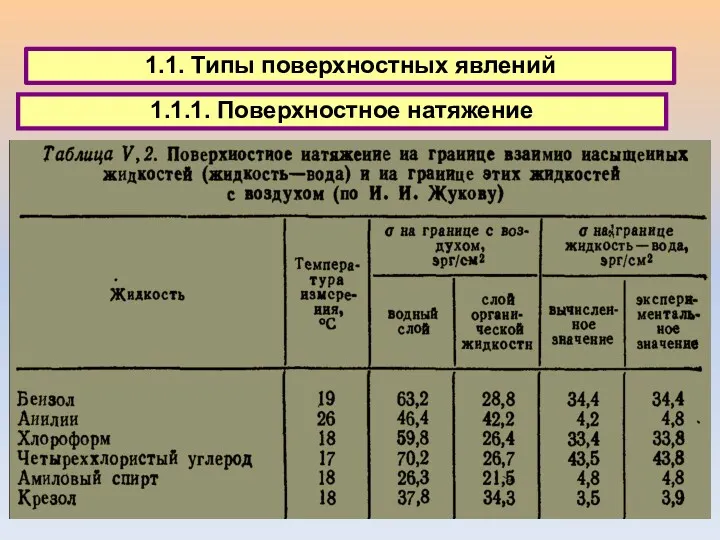
- 5. 1.1. Типы поверхностных явлений 1.1.1. Поверхностное натяжение
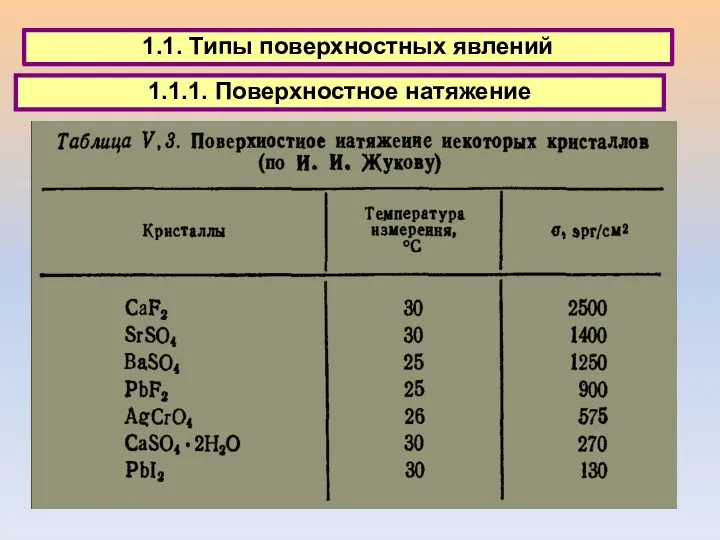
- 6. 1.1. Типы поверхностных явлений 1.1.1. Поверхностное натяжение
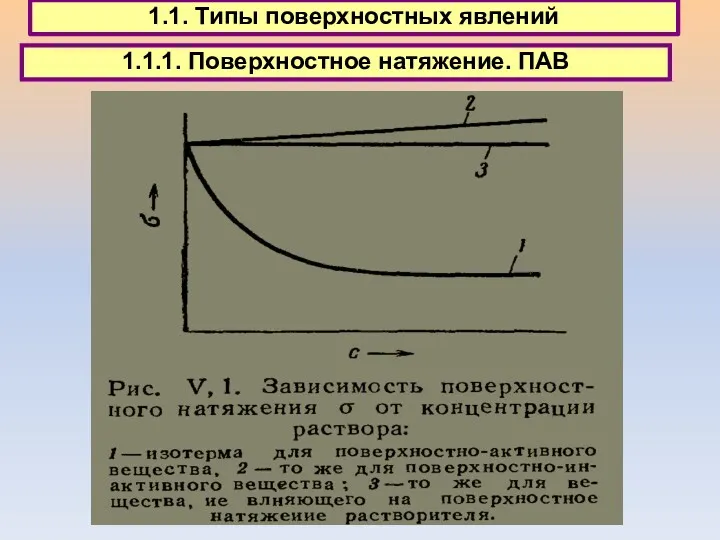
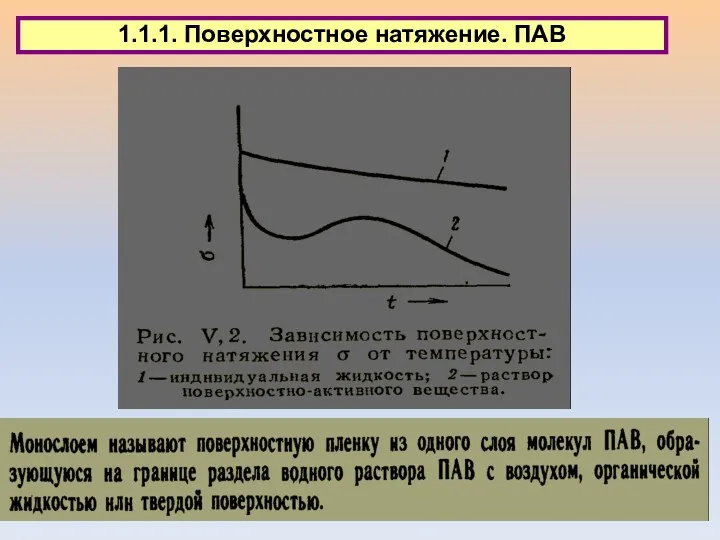
- 7. 1.1. Типы поверхностных явлений 1.1.1. Поверхностное натяжение. ПАВ
- 8. 1.1. Типы поверхностных явлений 1.1.1. Поверхностное натяжение. ПАВ
- 9. 1.1.1. Поверхностное натяжение. ПАВ
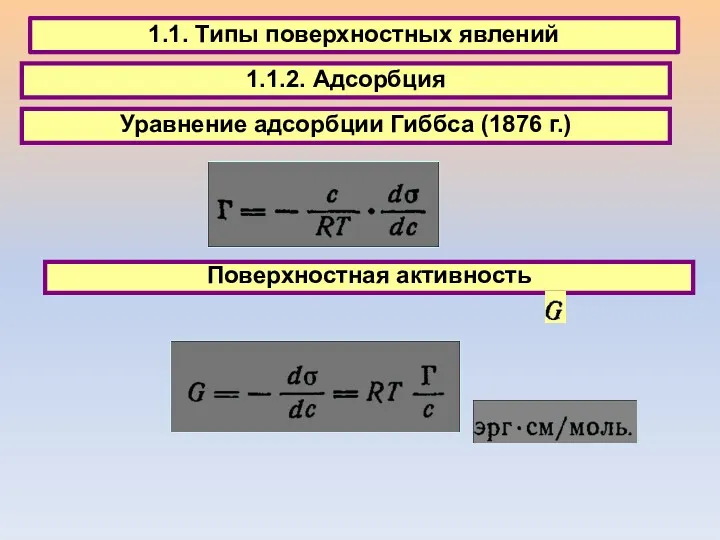
- 10. 1.1. Типы поверхностных явлений 1.1.2. Адсорбция Уравнение адсорбции Гиббса (1876 г.) Поверхностная активность
- 11. 1.1. Типы поверхностных явлений 1.1.2. Адсорбция Уравнение адсорбции Шишковского (1908 г.) Уравнение адсорбции Ленгмюра (1917 г.)
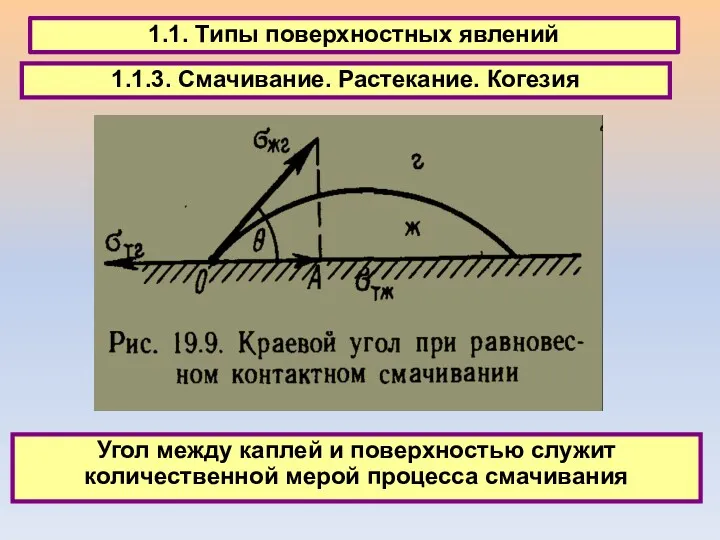
- 12. 1.1. Типы поверхностных явлений 1.1.3. Смачивание. Растекание. Когезия Угол между каплей и поверхностью служит количественной мерой
- 13. 1.1. Типы поверхностных явлений 1.1.3. Смачивание. Растекание. Когезия Угол между каплей и поверхностью служит количественной мерой
- 14. 1.1. Типы поверхностных явлений 1.1.3. Смачивание. Растекание. Когезия Уравнение Юнга (м – масло, в – вода)
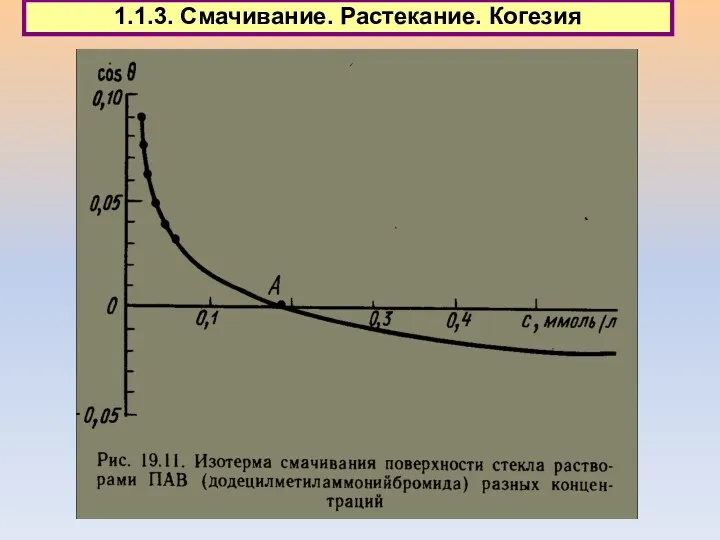
- 15. 1.1.3. Смачивание. Растекание. Когезия
- 16. 1. Поверхностные явления 1.1.3. Смачивание. Растекание. Когезия
- 17. 1.1.4. Сорбция. Адсорбция
- 18. 2. Электрохимические системы
- 19. 2. Электрохимические системы Предмет - взаимодействия ионов с электродами (электродные процессы). К ним относятся электролиз и
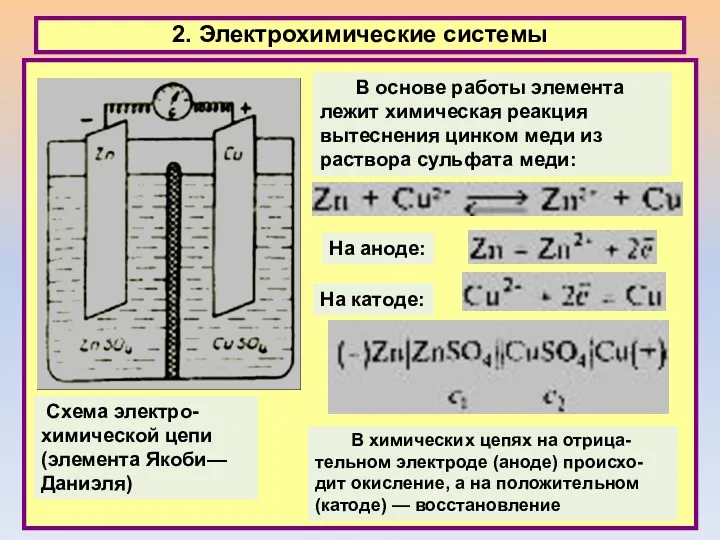
- 20. 2. Электрохимические системы Схема электро-химической цепи (элемента Якоби—Даниэля) В основе работы элемента лежит химическая реакция вытеснения
- 21. 2. Электрохимические системы На границах раздела между фазами в цепи существуют разности (скачки) потенциалов, именно: Если
- 22. 2. Электрохимические системы В самом общем случае, когда соприкасаются растворы различных электролитов и разной концентрации, диффузионные
- 23. 2. Электрохимические системы В нём при работе на аноде происходит процесс окисления цинка: Элемент Вольта как
- 24. 2. Электрохимические системы В нём при работе на аноде происходит процесс окисления цинка: Элемент Вольта как
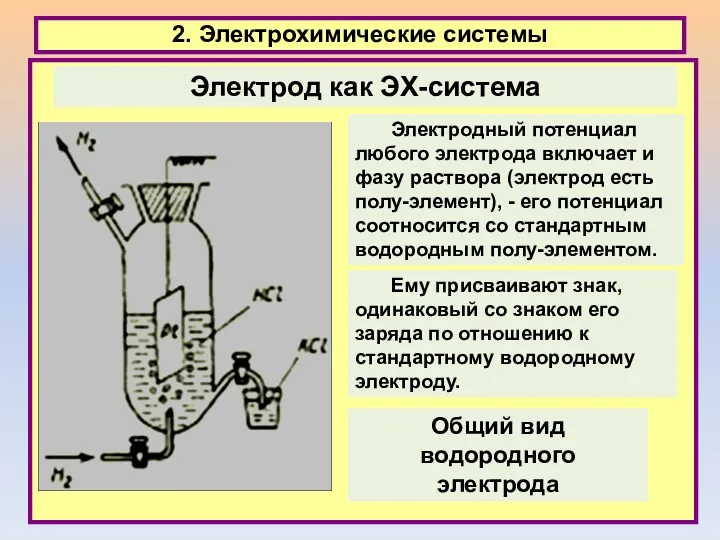
- 25. 2. Электрохимические системы Электродный потенциал любого электрода включает и фазу раствора (электрод есть полу-элемент), - его
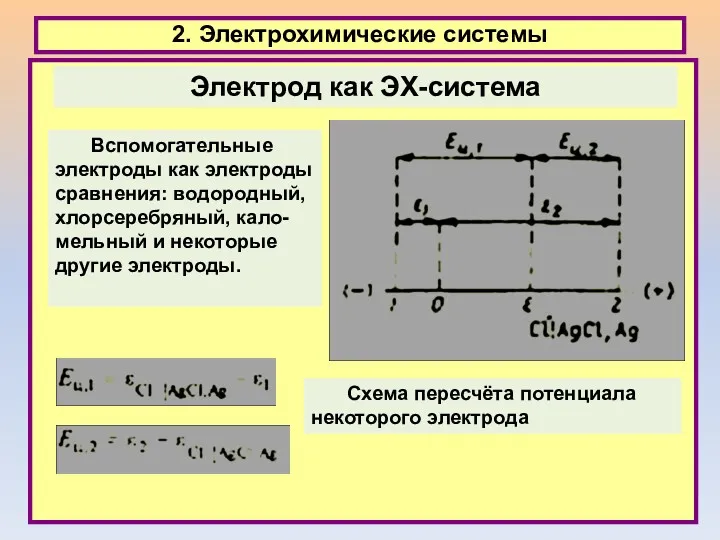
- 26. 2. Электрохимические системы Схема пересчёта потенциала некоторого электрода Электрод как ЭХ-система Вспомогательные электроды как электроды сравнения:
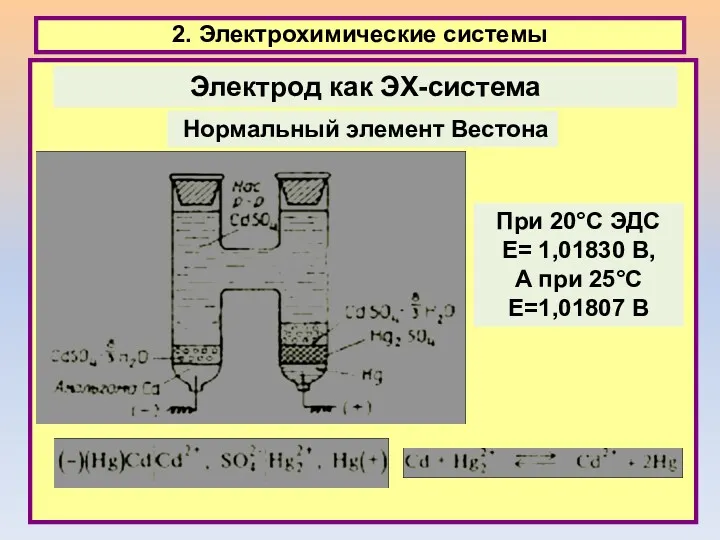
- 27. 2. Электрохимические системы Электрод как ЭХ-система Нормальный элемент Вестона При 20°С ЭДС Е= 1,01830 В, А
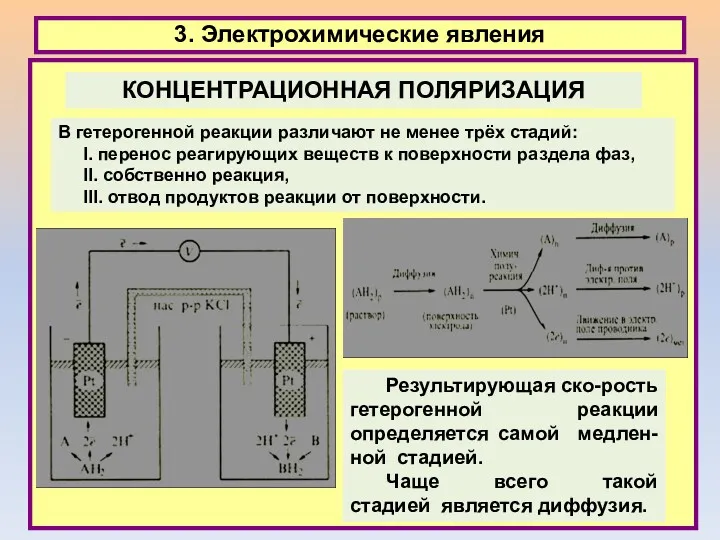
- 28. 3. Электрохимические явления В гетерогенной реакции различают не менее трёх стадий: I. перенос реагирующих веществ к
- 29. 3. Электрохимические явления Если к какому-либо электроду, например к серебряному в растворе AgNO3 с концентрацией С°
- 30. 3. Электрохимические явления c(s) — концентрация ионов серебра в диффузионном слое вблизи поверхности электрода. Она меньше
- 31. 3. Электрохимические явления Электролиз как процесс – это пропускание тока через раствор или расплав электролита, вызывающее
- 32. 3. Электрохимические явления Уравнение "электрической" составляющей тока с учётом связи подвижности частиц с коэффициентом диффузии (D):
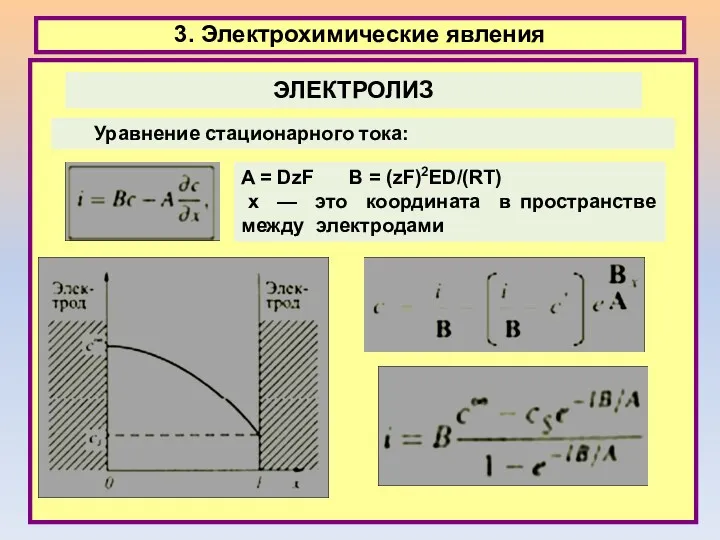
- 33. 3. Электрохимические явления Уравнение стационарного тока: ЭЛЕКТРОЛИЗ A = DzF B = (zF)2ED/(RT) х — это
- 34. 3. Электрохимические явления Уравнения стационарного электролиза: I. Если реакция на электроде является достаточно быстрой (по сравнению
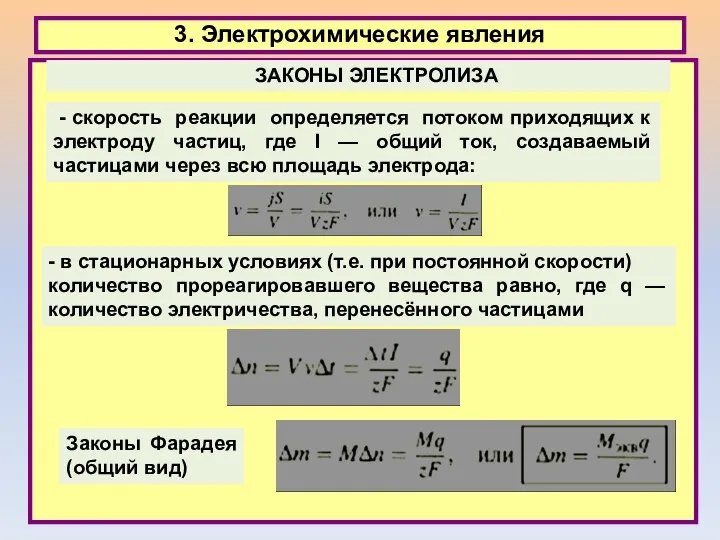
- 35. 3. Электрохимические явления ЗАКОНЫ ЭЛЕКТРОЛИЗА - скорость реакции определяется потоком приходящих к электроду частиц, где I
- 37. Скачать презентацию



















 Пластмассы в автомобилестроении
Пластмассы в автомобилестроении Спирты & Фенолы
Спирты & Фенолы Строение атома. Классификация ядер атомов
Строение атома. Классификация ядер атомов Реакции ионного обмена
Реакции ионного обмена Алюминий и его соединения
Алюминий и его соединения Чисті речовини та суміші. Способи розділення
Чисті речовини та суміші. Способи розділення Относительные атомные и молекулярные массы
Относительные атомные и молекулярные массы Газовые законы для идеальных и реальных газов. Лекция 1
Газовые законы для идеальных и реальных газов. Лекция 1 Роль химии в современной цивилизации
Роль химии в современной цивилизации Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Неметаллические конструкционные материалы
Неметаллические конструкционные материалы Аммиак. Состав вещества
Аммиак. Состав вещества General characteristics of halogens. Halogen compounds
General characteristics of halogens. Halogen compounds Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс В мире криссталлов
В мире криссталлов Соединения химических элементов. Валентность и степень окисления элементов
Соединения химических элементов. Валентность и степень окисления элементов Алюминий
Алюминий Растворение. Растворы
Растворение. Растворы Нанокаталіз. Активність каталізатора
Нанокаталіз. Активність каталізатора Штучні і синтетичні волокна
Штучні і синтетичні волокна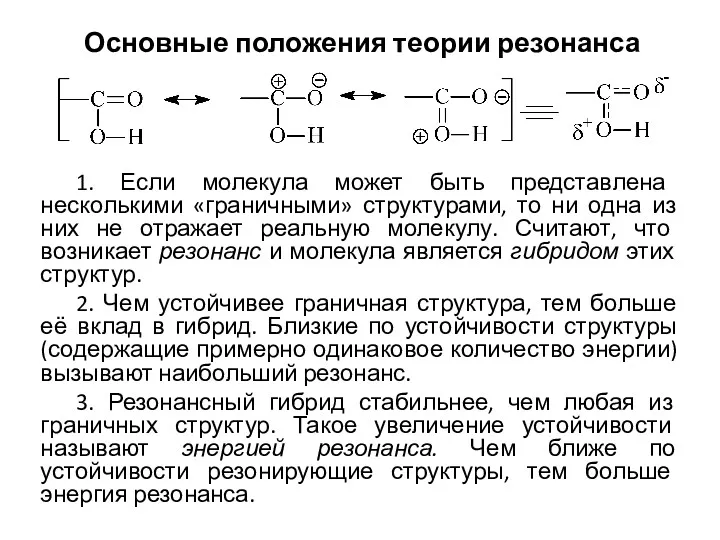 Основные положения теории резонанса
Основные положения теории резонанса Щелочные металлы
Щелочные металлы Природный газ и нефть
Природный газ и нефть Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Нанотрубка - как аллотропная модификация углерода
Нанотрубка - как аллотропная модификация углерода 5511c750430548bfa1da4ba840324bb2
5511c750430548bfa1da4ba840324bb2 Химическая промышленность России
Химическая промышленность России Проект Кабинет химии будущего
Проект Кабинет химии будущего