Содержание
- 2. Общая характеристика Алюминий – наиболее распространенный металл и третий по распространенности химический элемент в земной коре
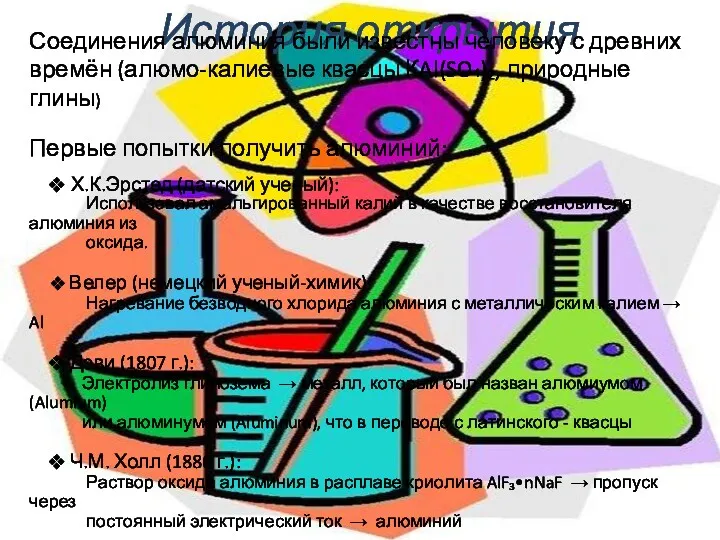
- 3. История открытия Соединения алюминия были известны человеку с древних времён (алюмо-калиевые квасцы КAl(SO₄)₂, природные глины) Первые
- 4. Эрстед Дэви Холл
- 5. Физические свойства Серебристо-белый легкий металл Температура плавления = 660°С Плотность = 2,7 кг/м³ Температура кипения =
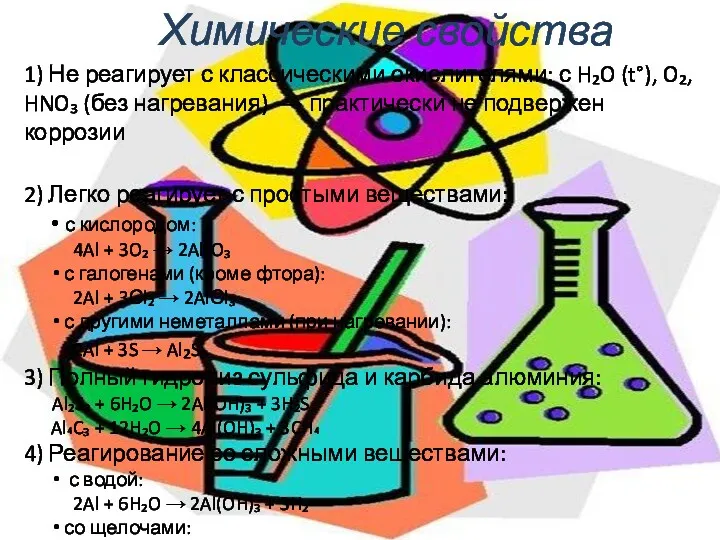
- 6. Химические свойства 1) Не реагирует с классическими окислителями: с H₂O (t°), O₂, HNO₃ (без нагревания) →
- 7. 2Al + 6NaOH → 2Na₃AlO₃ + 3H₂ 5) Легкое растворение в соляной и разбавленной серной кислотах:
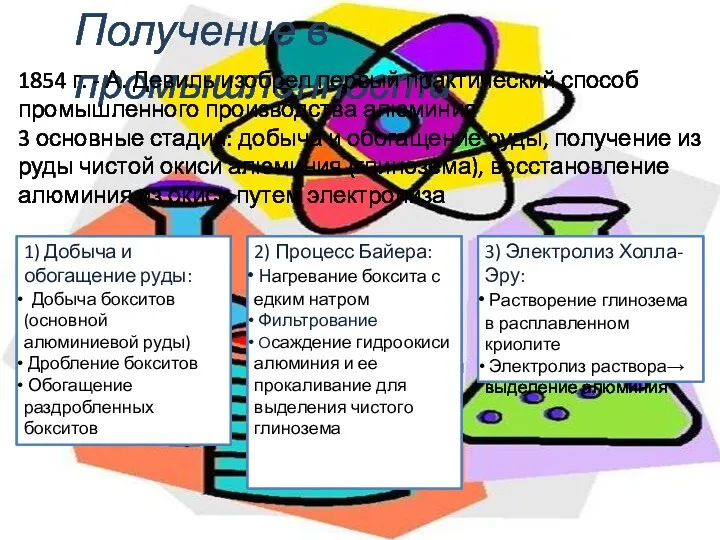
- 8. Получение в промышленности 1854 г. - А. Девиль изобрел первый практический способ промышленного производства алюминия 3
- 9. Получение в лаборатории 1827 г. - Фридрих Вёлер предложил лабораторный способ получения алюминия восстановлением металлическим калием
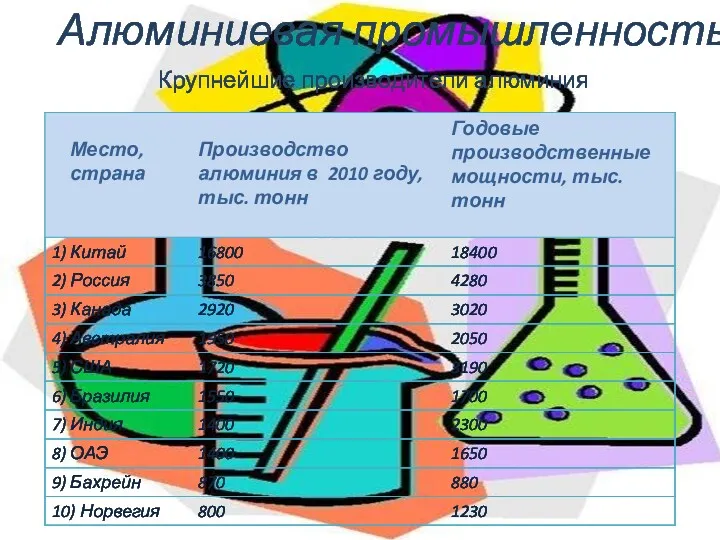
- 10. Алюминиевая промышленность Крупнейшие производители алюминия
- 11. В 1865 г. известный русский химик Н.Н. Бекетов открыл метод восстановления металлов с помощью алюминия, получивший
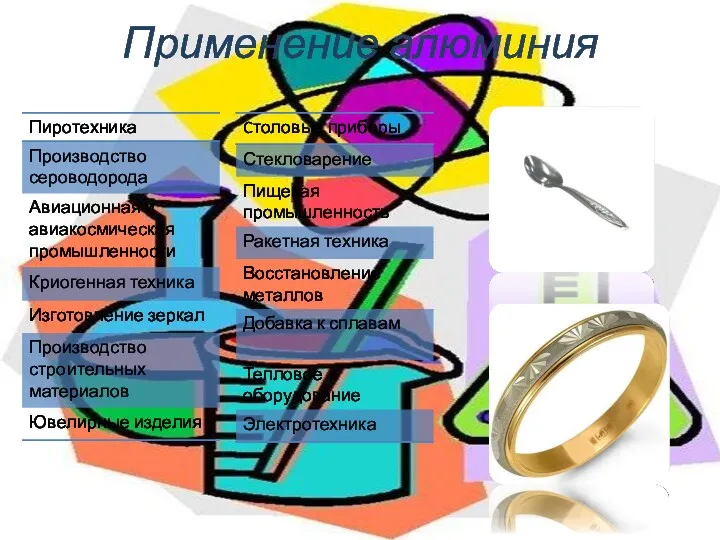
- 12. Применение алюминия
- 13. Алюминий в пище Продукты с алюминием: хлеб, дрожжи, синтетические пищевые добавки и искусственные красители, консервы, колбаса,
- 14. Вода из-под крана, прежде чем попасть в наш дом, проходит техническую очистку от примесей с помощью
- 15. Алюминий в дезодорантах, антиперспирантах и косметике Через кожу алюминий усваивается очень даже интенсивно В современных дезодорантах–антиперспирантах
- 16. Алюминий в лекарствах и вакцинах Гидроксиды алюминия являются составляющей основных вакцин. Группа западных ученых доказала, что
- 17. Алюминий в человеческом организме Практически во всех органах человека обнаружен алюминий Большинство биомолекул содержит алюминий, который
- 18. Алюминоз легких Особенно тяжелые отравления алюминием стали наблюдаться у рабочих при его широком применении в самолетостроении,
- 19. Алюминий и болезнь Альцгеймера Болезнь Альцгеймера (провалы в памяти и маразм при повышенной концентрации алюминия в
- 21. Скачать презентацию




 Химия. Отличие химических свойств от физических
Химия. Отличие химических свойств от физических Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс Химические формулы веществ (8 класс)
Химические формулы веществ (8 класс) Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів Ионное произведение воды. Водородный показатель воды
Ионное произведение воды. Водородный показатель воды Группа веществ, изолируемых полярными растворителями
Группа веществ, изолируемых полярными растворителями Пищевые добавки
Пищевые добавки Гидролиз органических и неорганических веществ
Гидролиз органических и неорганических веществ Алюминий и его соединения
Алюминий и его соединения Свойства металлов
Свойства металлов Хром и его соединения
Хром и его соединения Химический элемент. Электронное строение атома
Химический элемент. Электронное строение атома π-комплексы металлов. Природа связи металлуглерод в π-комплексах металлов. Отличия в свойствах от обычной σ-связи
π-комплексы металлов. Природа связи металлуглерод в π-комплексах металлов. Отличия в свойствах от обычной σ-связи Галогены
Галогены Поверхностно-активные вещества (ПАВ). Классификация, свойства и условия применения
Поверхностно-активные вещества (ПАВ). Классификация, свойства и условия применения Снег и лед. Тайны твердой воды
Снег и лед. Тайны твердой воды Подгруппа углерода
Подгруппа углерода Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов
Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов Летучие яды
Летучие яды Спирти. Історична довідка
Спирти. Історична довідка Водород. Нахождение в природе. Физические и химические свойства. Применение
Водород. Нахождение в природе. Физические и химические свойства. Применение Окислительно-востановительные реакции в растворах
Окислительно-востановительные реакции в растворах Органічна хімія, частина 1
Органічна хімія, частина 1 Мұнайдың химиялық және технологиялық жіктелуі
Мұнайдың химиялық және технологиялық жіктелуі Равновесия в растворах электролитов
Равновесия в растворах электролитов Щелочные металлы
Щелочные металлы Каучук и резина
Каучук и резина Рентгеноструктуралық анализ. Лауе тәжірибесі, Брегг-Вульф теңдеуі, оны шығару жолдары
Рентгеноструктуралық анализ. Лауе тәжірибесі, Брегг-Вульф теңдеуі, оны шығару жолдары