Содержание
- 2. Химическая формула Н2О СО2 НCl NaCl Н2SО4 C6H12О6 О2
- 3. В химии при письме вместо названий используют формулы веществ. Как вы думаете, почему? Н2О СО2 НCl
- 4. Формулы веществ записывать быстрее, они занимают мало место и несут много информации. Наша задача сегодня –
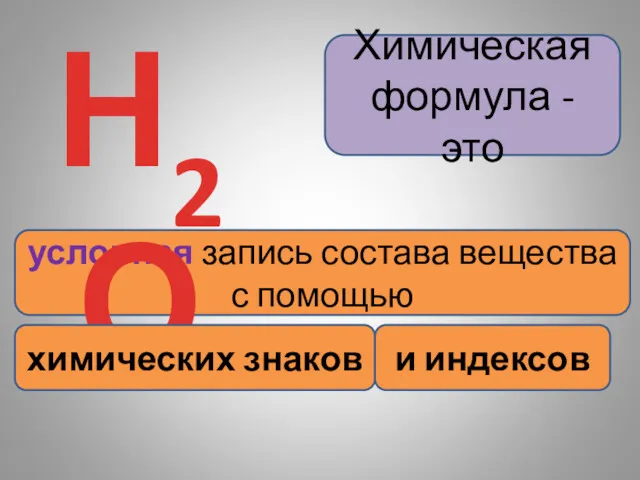
- 5. Химическая формула - это условная запись состава вещества с помощью Н2О химических знаков и индексов
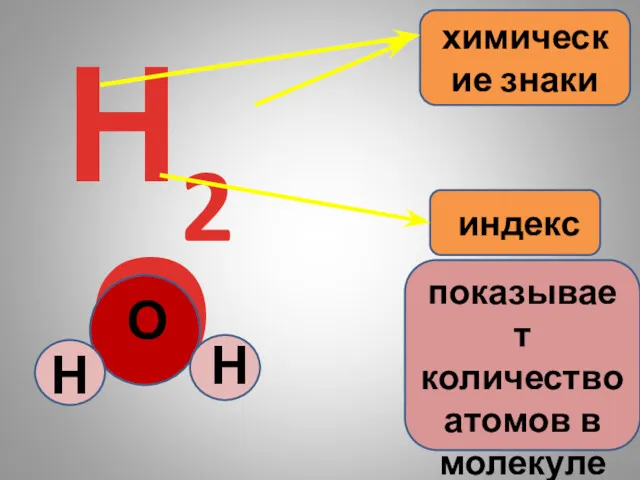
- 6. Н2О химические знаки индекс показывает количество атомов в молекуле
- 7. Информация, которую содержат химические формулы: 1) 1 молекула Н2О
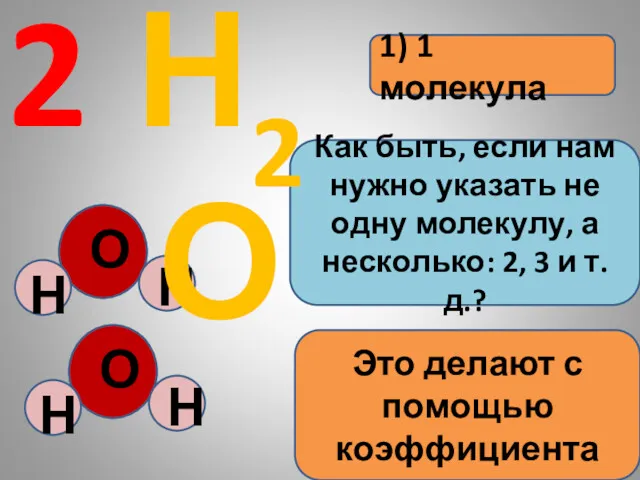
- 8. 1) 1 молекула 2 Как быть, если нам нужно указать не одну молекулу, а несколько: 2,
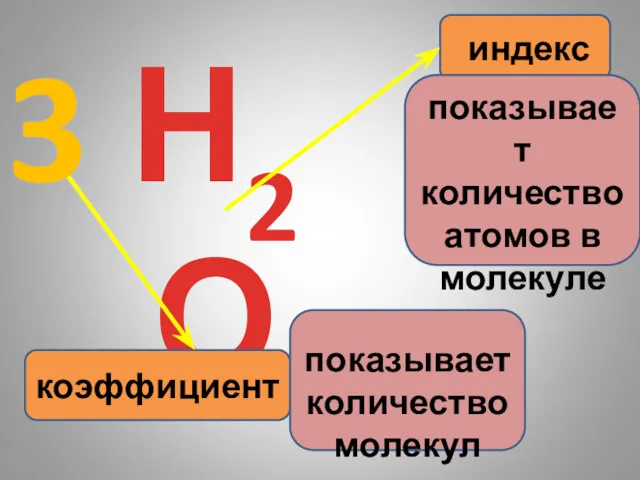
- 9. Н2О коэффициент индекс показывает количество атомов в молекуле 3 показывает количество молекул
- 10. II. Чтение химических формул. * Примеры: NH3 – молекула эн аш три состоит из одного атома
- 11. 1. В записи 5SO3 коэффициент равен: б) 15; в) 3; г) коэффициент отсутствует. 2. В записи
- 12. 3. В записи СO2коэффициент равен: б) 3; в) 2; г) коэффициент отсутствует. а) 1; 3. В
- 13. Информация, которую содержат химические формулы: 1) 1 молекула Н2О 2) Название вещества 3) Качественный состав
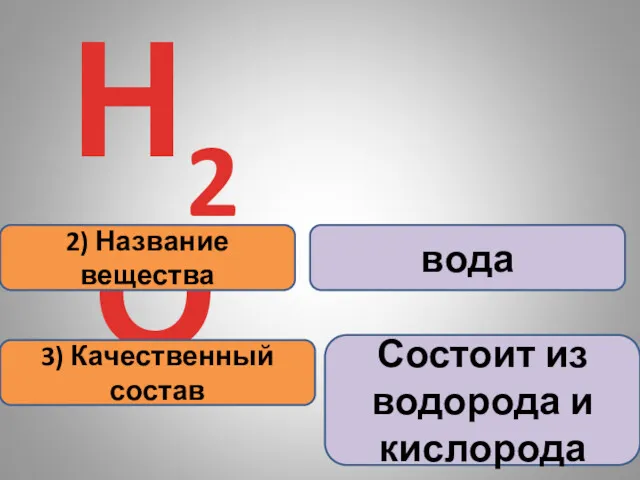
- 14. Н2О 2) Название вещества 3) Качественный состав вода Состоит из водорода и кислорода
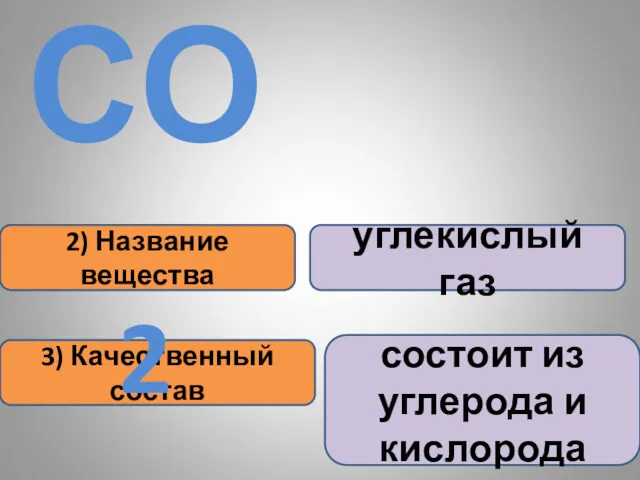
- 15. 2) Название вещества 3) Качественный состав углекислый газ состоит из углерода и кислорода СО2
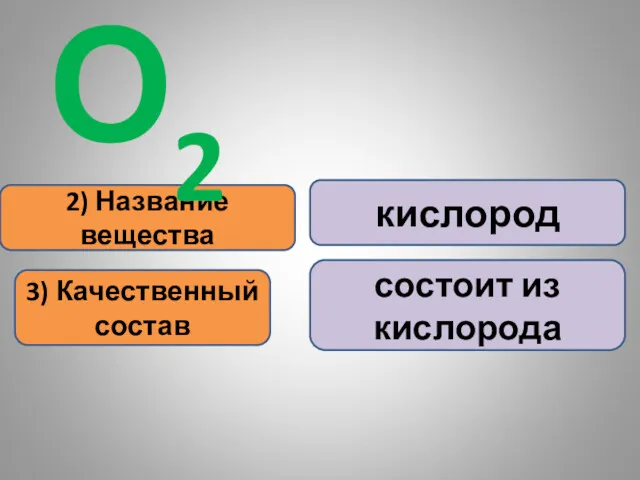
- 16. 2) Название вещества 3) Качественный состав кислород состоит из кислорода О2
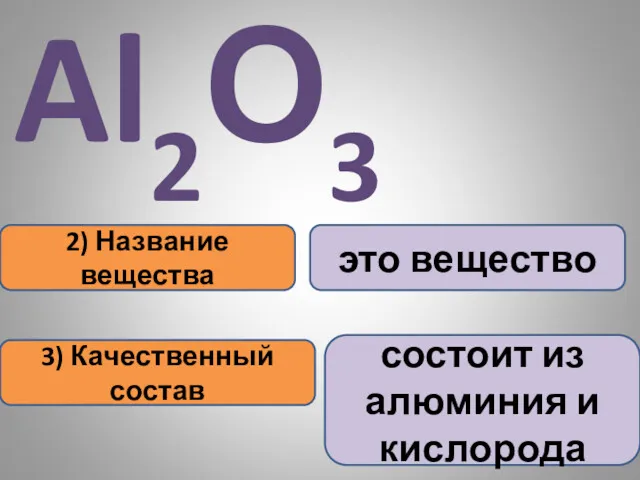
- 17. 2) Название вещества 3) Качественный состав это вещество состоит из алюминия и кислорода Al2О3
- 18. Информация, которую содержат химические формулы: 1) 1 молекула Н2О 2) Название вещества 3) Качественный состав 4)
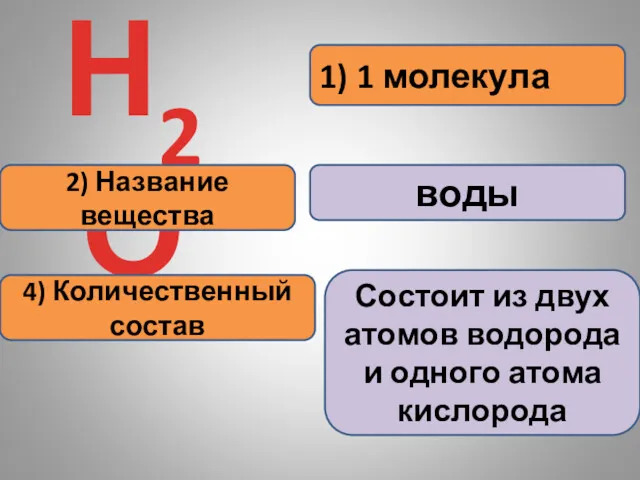
- 19. 1) 1 молекула Н2О 2) Название вещества воды 4) Количественный состав Состоит из двух атомов водорода
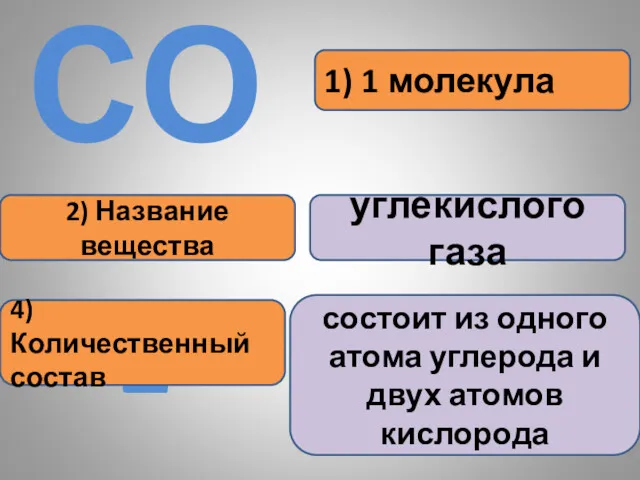
- 20. 1) 1 молекула 2) Название вещества углекислого газа СО2 4) Количественный состав состоит из одного атома
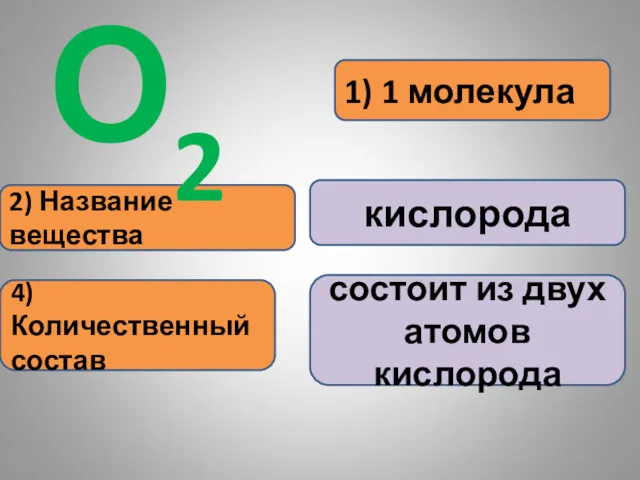
- 21. 1) 1 молекула 2) Название вещества кислорода О2 4) Количественный состав состоит из двух атомов кислорода
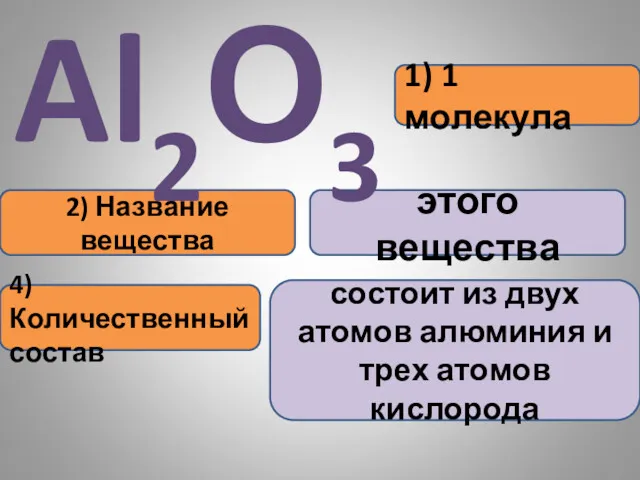
- 22. 1) 1 молекула 2) Название вещества этого вещества Al2О3 4) Количественный состав состоит из двух атомов
- 23. 7Н2SO4 Сколько молекул серной кислоты записано? Сколько атомов водорода записано? Сколько атомов серы записано? Сколько атомов
- 24. Когда мы знакомились с элементами, то узнали, что для измерения масс атомов ввели новую физическую величину.
- 25. Зная массы атомов, по химической формуле можно найти массу молекулы, которую назвали Мr - То есть
- 26. Информация, которую содержат химические формулы: 1) 1 молекула Н2О 2) Название вещества 3) Качественный состав 4)
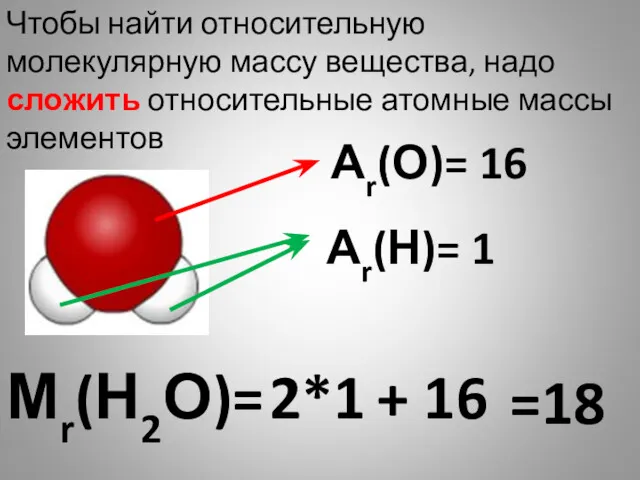
- 27. Мr(Н2О)= Чтобы найти относительную молекулярную массу вещества, надо сложить относительные атомные массы элементов Аr(О)= 16 Аr(Н)=
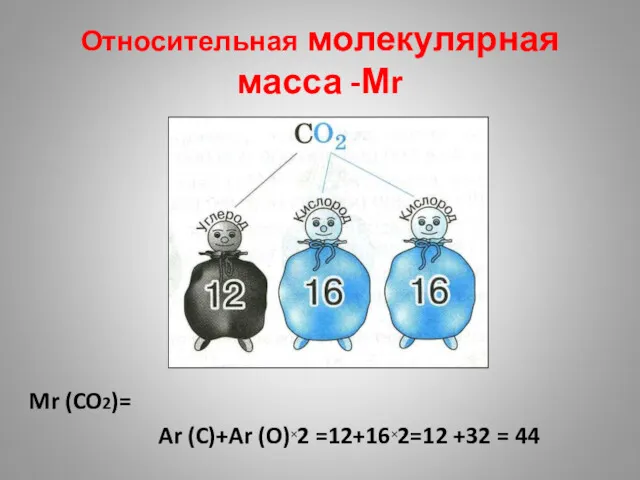
- 28. Относительная молекулярная масса -Мr Mr (CO2)= Ar (C)+Ar (O)×2 =12+16×2=12 +32 = 44
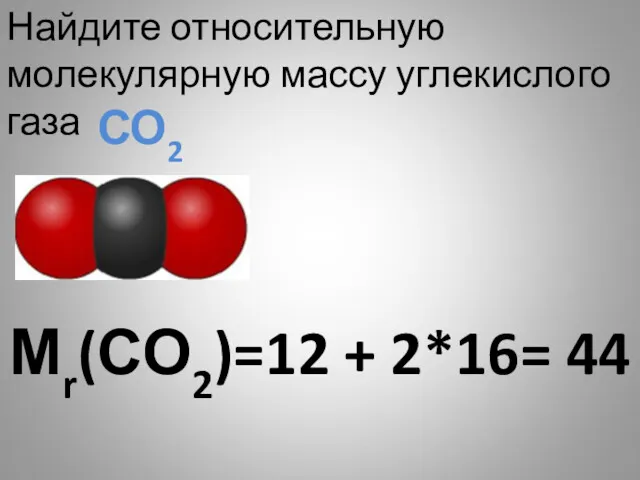
- 29. Мr(СО2)=12 + 2*16= 44 Найдите относительную молекулярную массу углекислого газа СО2
- 30. Найдите относительные молекуляр-ные массы следующих веществ: 1) кислорода О2 2) аммиака NH3 3) Оксида алюминия Аl2О3
- 31. Рассчитайте Мr (H2) = Mr (СаСl2) = Mr (CaCO3) = Мr (Ca(OH)2)= Mr (СН3СООН)= Мr (Ca3(PO4)2)=
- 32. САМОСТОЯТЕЛЬНАЯ РАБОТА 98 98 80 40 80 80 17 34
- 34. Скачать презентацию
















 Композиционные материалы для изоляции электрических машин
Композиционные материалы для изоляции электрических машин Кислоты НСL, H2 O, H2 CO3
Кислоты НСL, H2 O, H2 CO3 Физические явления – основа разделения смесей в химии (урок химии в 8 классе)
Физические явления – основа разделения смесей в химии (урок химии в 8 классе) Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл
Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл Цинк и его применение
Цинк и его применение Полимеры. Каучук
Полимеры. Каучук Полисахариды. Крахмал
Полисахариды. Крахмал Третья группа, главная подгруппа. 9 класс
Третья группа, главная подгруппа. 9 класс Сложные эфиры
Сложные эфиры Закон сохранения массы веществ. Уравнения химических реакций
Закон сохранения массы веществ. Уравнения химических реакций Значення хімічних процесів у природі
Значення хімічних процесів у природі Курс лекций: Методы диагностики и анализа микро- и наносистем
Курс лекций: Методы диагностики и анализа микро- и наносистем Твердое состояние вещества. Кристаллические и аморфные тела
Твердое состояние вещества. Кристаллические и аморфные тела Гидроксиды. Основания: способы получения
Гидроксиды. Основания: способы получения Жер қыртысының заттық және химиялық құрамы
Жер қыртысының заттық және химиялық құрамы Реакции деструкции макромолекул
Реакции деструкции макромолекул Неметаллы
Неметаллы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Классификация веществ по характеру связи
Классификация веществ по характеру связи Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс Chemistry of Coordination Compounds
Chemistry of Coordination Compounds Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов Субстраты и продукты биохимических реакций
Субстраты и продукты биохимических реакций Пурины. Строение пурина
Пурины. Строение пурина Высокомолекулярные соединения полимеры
Высокомолекулярные соединения полимеры Химическая связь
Химическая связь Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Получение и применение алканов
Получение и применение алканов