Содержание
- 2. Теоретическая часть 1. Скорость химических реакций Раздел химии, изучающий скорость и механизм химических реакций, называется химической
- 3. Гомогенные реакции протекают во всем объеме, например, реакции между растворенными веществами или газами: 2NO(г) + O2(г)
- 4. Различают среднюю и истинную скорость реакции. Если в момент времени τ₁ концентрация реагирующего вещества была с₁
- 5. Основными факторами, определяющими скорость химических реакций, являются: а) природа реагирующих веществ; б) концентрация; в) температура; г)
- 6. “k" называют еще удельной скоростью. Например, для реакции: 2SO₂ + O2 = 2SO3, Применяя закон действующих
- 7. где Vt2 и Vt₁ — скорости реакции соответственно при конечной t2 и начальной t₁ температурах; γ
- 8. где А — предэкспоненциальный множитель (постоянная величина, учитывающая число соударений молекул); R — универсальная газовая постоянная
- 9. Одним из наиболее распространенных в химической практике способов изменения скорости химических реакций является катализ. Катализом называется
- 10. 2. Химическое равновесие Многие химические реакции протекают до конца, т.е. исходные вещества целиком превращаются в конечные
- 11. Химическое равновесие — равновесие динамическое: в данных условиях непрерывно протекают две противоположно направленные реакции, концентрации же
- 12. Постоянная Кр называется константой химического равновесия, которая зависит от температуры и природы реагирующих веществ, но не
- 13. б) при повышении давления (для газов и паров) равновесие смещается в сторону той реакции, которая сопровождается
- 14. Экспериментальная часть Цель работы: изучить влияние различных факторов на скорость гомогенных и гетерогенных химических реакций и
- 15. Опыт № 2 Зависимость скорости реакции от концентрации реагирующих веществ В три пробирки налейте 0,1 н.
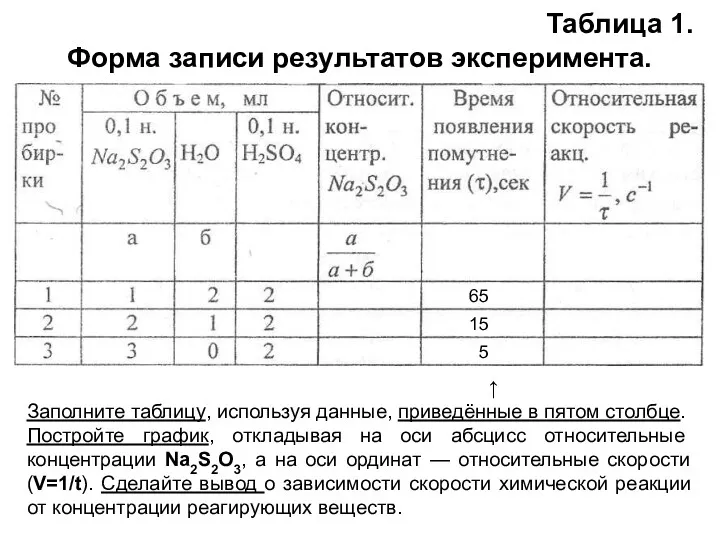
- 16. Таблица 1. Форма записи результатов эксперимента. 65 15 5 ↑ Заполните таблицу, используя данные, приведённые в
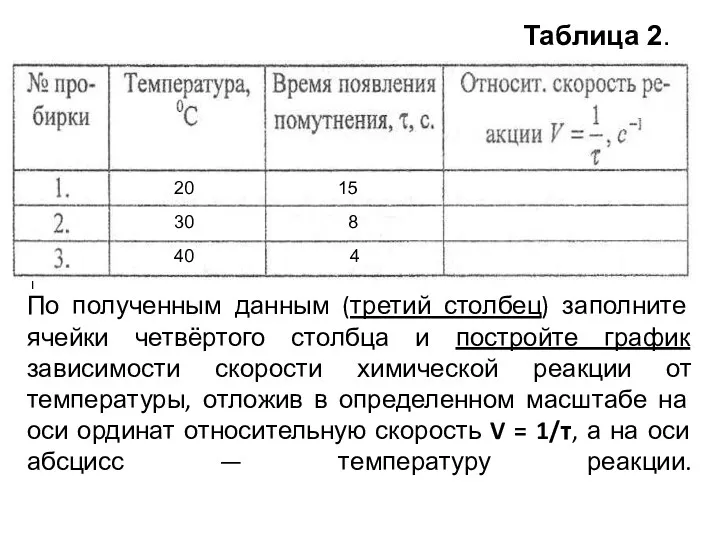
- 17. Опыт № 3 Влияние температуры на скорость химической реакции Налейте в три пробирки по 2 мл
- 18. ↑ По полученным данным (третий столбец) заполните ячейки четвёртого столбца и постройте график зависимости скорости химической
- 19. Опыт № 4 Влияние величины поверхности реагирующих веществ на скорость химической реакции в гетерогенной системе Отберите
- 20. Опыт № 5 Влияние изменения концентрации реагирующих веществ на химическое равновесие О смещении химического равновесия в
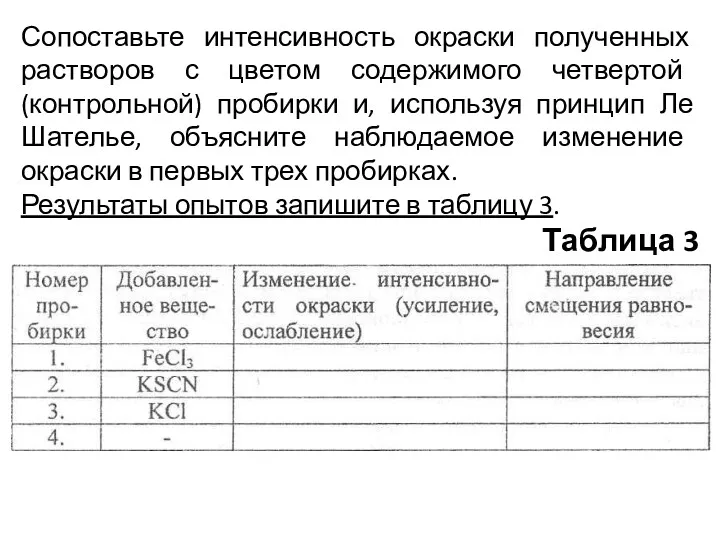
- 21. Сопоставьте интенсивность окраски полученных растворов с цветом содержимого четвертой (контрольной) пробирки и, используя принцип Ле Шателье,
- 23. Скачать презентацию

















 Отримання кисню. Властивості кисню
Отримання кисню. Властивості кисню Соли. Определение солей
Соли. Определение солей Смещение химического равновесия
Смещение химического равновесия Общая химия
Общая химия Циклоалканы
Циклоалканы Химическая кинетика и катализ
Химическая кинетика и катализ Solutions and solubilities
Solutions and solubilities Искусственные каменные материалы
Искусственные каменные материалы Строение атома
Строение атома Сапалық талдау. Сапалық аналитикалық реакциялар
Сапалық талдау. Сапалық аналитикалық реакциялар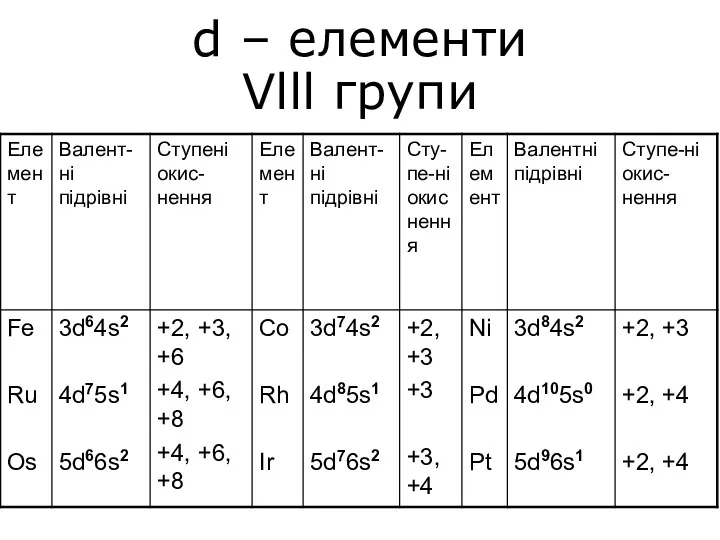 d – елементи Vlll групи
d – елементи Vlll групи Высокомолекулярные соединения (ВМС) или полимеры
Высокомолекулярные соединения (ВМС) или полимеры Реакции ионного обмена. Ионное произведение воды. Водородный показатель. Индикаторы
Реакции ионного обмена. Ионное произведение воды. Водородный показатель. Индикаторы Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Растворы электролитов. Буферные растворы. Лекция 4
Растворы электролитов. Буферные растворы. Лекция 4 Виды коррозии
Виды коррозии Майлардың анықтамасы
Майлардың анықтамасы Алюміній. Загальна характеристика, властивості. Алюміній оксид, алюміній гідроксид, їх амфотерність
Алюміній. Загальна характеристика, властивості. Алюміній оксид, алюміній гідроксид, їх амфотерність Спектральные методы: инфракрасная спектроскопия. Люминесцентный анализ
Спектральные методы: инфракрасная спектроскопия. Люминесцентный анализ Существенные изменения в измерителях ЕГЭ по химии
Существенные изменения в измерителях ЕГЭ по химии Окислительные методы получения органических соединений
Окислительные методы получения органических соединений Амины. Понятие об аминах. Анилин как органическое основание
Амины. Понятие об аминах. Анилин как органическое основание Алкадиены (диены, диеновые углеводороды)
Алкадиены (диены, диеновые углеводороды)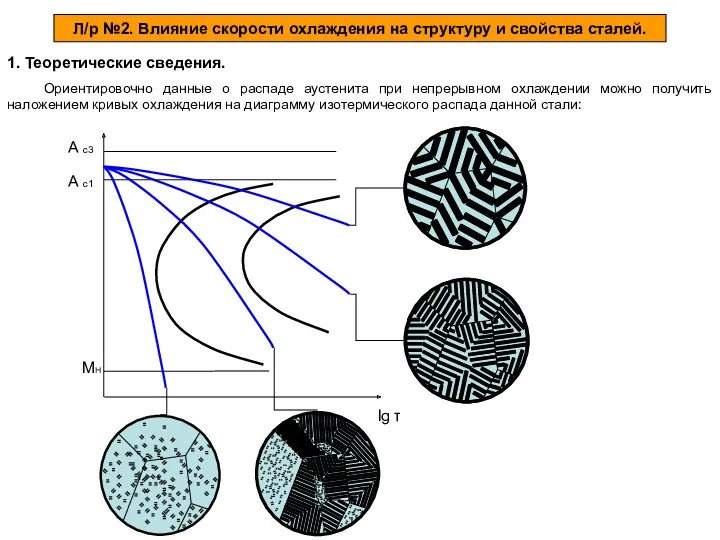 Влияние скорости охлаждения на структуру и свойства сталей
Влияние скорости охлаждения на структуру и свойства сталей Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов Алкины
Алкины Алкены. Этиленовые углеводороды, олефины
Алкены. Этиленовые углеводороды, олефины