Содержание
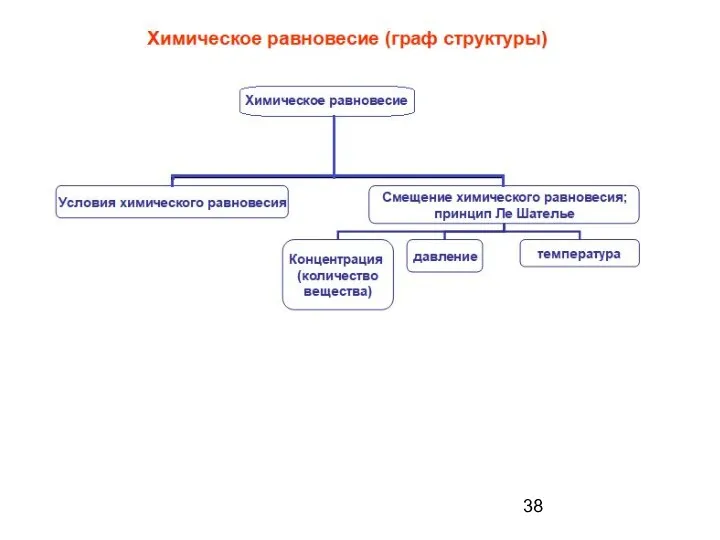
- 2. Граф структуры
- 3. ХИМИЧЕСКАЯ КИНЕТИКА И КАТАЛИЗ Химическая кинетика – учение о скоростях химических реакций и зависимости их от
- 4. Скорость реакции пропорциональна числу актов взаимодействия частиц реагентов в единице объема системы (для гомогенной реакции) или
- 5. Средняя скорость не отражает истинной скорости в каждый момент времени, поэтому мгновенную (истинную) скорость реакции v
- 6. Классификация химических реакций по числу стадий. Элементарная стадия реакции – превращение одной (распад или изомеризация) или
- 7. Скорость реакции в целом определяется лимитирующей (самой медленной) стадией реакции. В приведенном примере таковой является стадия,
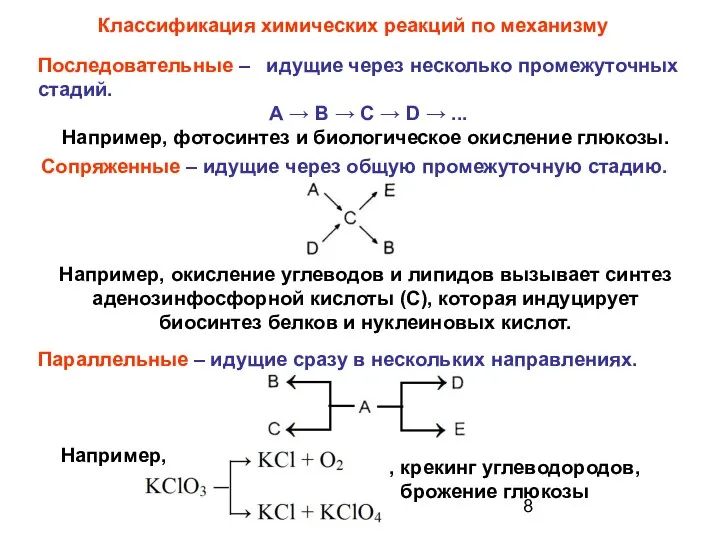
- 8. Сопряженные – идущие через общую промежуточную стадию. Классификация химических реакций по механизму Последовательные – идущие через
- 9. Цепные – стадии превращения реагентов в продукты многократно повторяются. Свободные радикалы – частицы с неспаренными электронами.
- 10. ВАЖНЕЙШИЕ ФАКТОРЫ, ВЛИЯЮЩИЕ НА СКОРОСТЬ РЕАКЦИЙ природа реагентов концентрация реагентов температура давление катализатор
- 11. ВЛИЯНИЕ ПРИРОДЫ РЕАГЕНТОВ Скорость химической реакции зависит от природы реагентов. Например, F2 реагирует с H2 значительно
- 12. ВЛИЯНИЕ КОНЦЕНТРАЦИЙ РЕАГЕНТОВ Необходимым условием химического взаимодействия является столкновение частиц реагентов. Чем больше концентрации реагентов, тем
- 13. где a, b, d, f – коэффициенты; A, B, D, F – формулы участников; кинетическое уравнение
- 14. Константа скорости химической реакции k численно равна скорости химической реакции v при концентрациях всех реагентов c,
- 15. В реакциях нулевого порядка скорость реакции не зависит от концентраций реагентов. В реакциях первого порядка скорость
- 16. Концентрации твердых и жидких (не растворённых!) веществ не входят в кинетические уравнения гетерогенных реакций, так как
- 17. ВЛИЯНИЕ ТЕМПЕРАТУРЫ Правило (закон) Вант-Гоффа При повышении температуры на 10 °С (10 K) скорость большинства химических
- 18. Уравнение Вант-Гоффа где v2 и v1 – скорости реакции при температурах T2 и T1 соответственно; Δt1
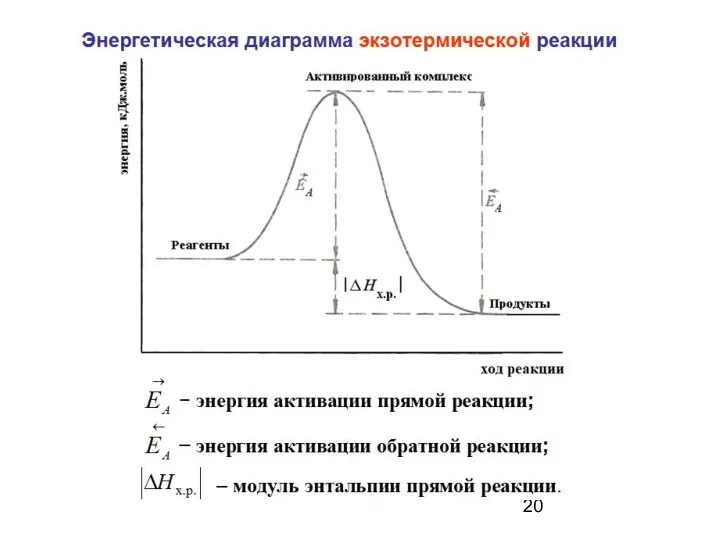
- 19. Энергия активации ЕA – минимальная энергия, которую надо добавить к средней суммарной кинетической энергии сталкивающихся частиц
- 21. Уравнение Аррениуса где ЕA – энергия активации; k – константа скорости реакции; R = 8,31 Дж/(моль·К)
- 22. Графический способ нахождения EA и A из уравнения Аррениуса Аналитический способ нахождения EA из уравнения Аррениуса
- 23. ВЛИЯНИЕ ДАВЛЕНИЯ Уравнение Клапейрона-Менделеева где p – давление; V – объем; n – количество вещества. Из
- 24. Катализаторы – вещества, увеличивающие скорость химических реакций, но не расходующиеся в них. Ингибиторы – вещества, замедляющие
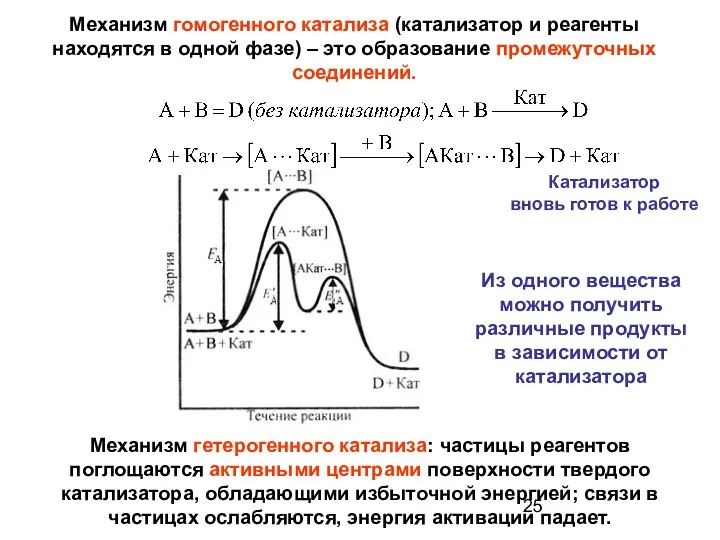
- 25. Катализатор вновь готов к работе Механизм гомогенного катализа (катализатор и реагенты находятся в одной фазе) –
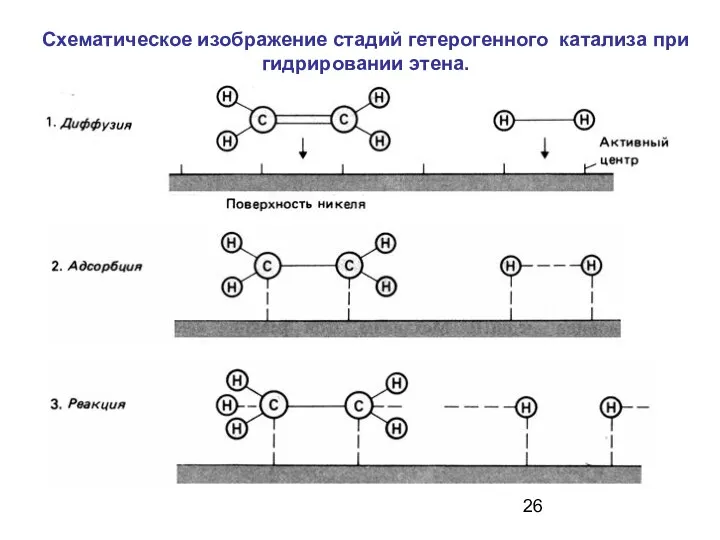
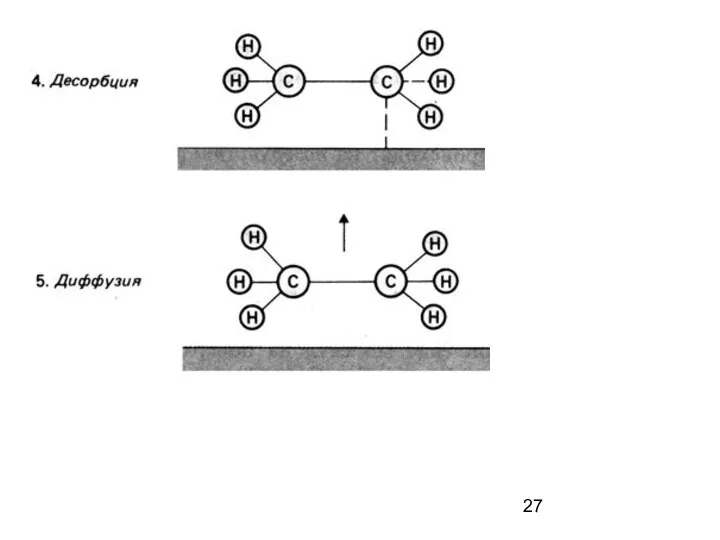
- 26. Схематическое изображение стадий гетерогенного катализа при гидрировании этена.
- 28. Ферменты (энзимы) – белковые молекулы, которые катализируют химические реакции в живых системах Отличия от химического катализа:
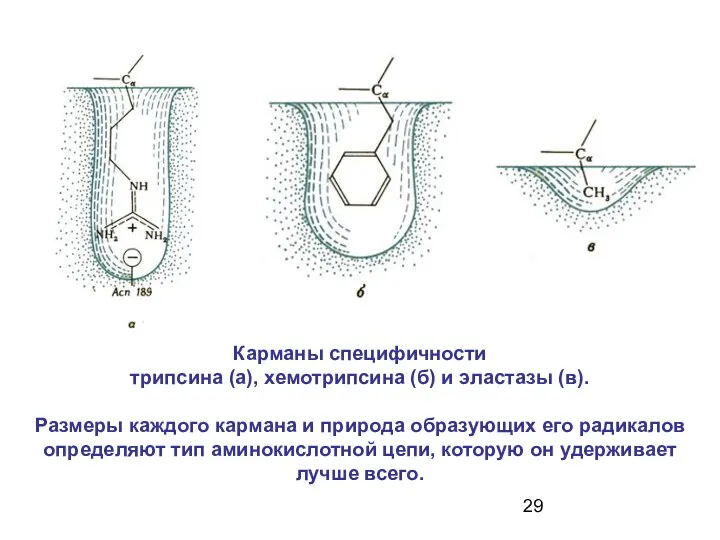
- 29. Карманы специфичности трипсина (а), хемотрипсина (б) и эластазы (в). Размеры каждого кармана и природа образующих его
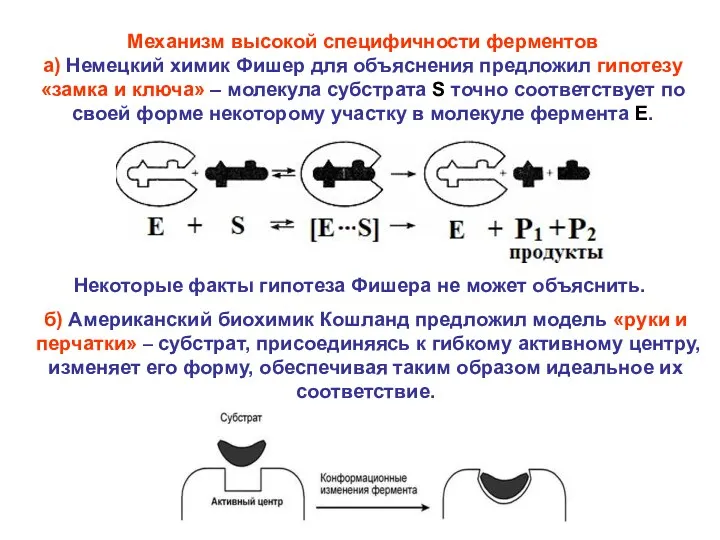
- 30. Механизм высокой специфичности ферментов а) Немецкий химик Фишер для объяснения предложил гипотезу «замка и ключа» –
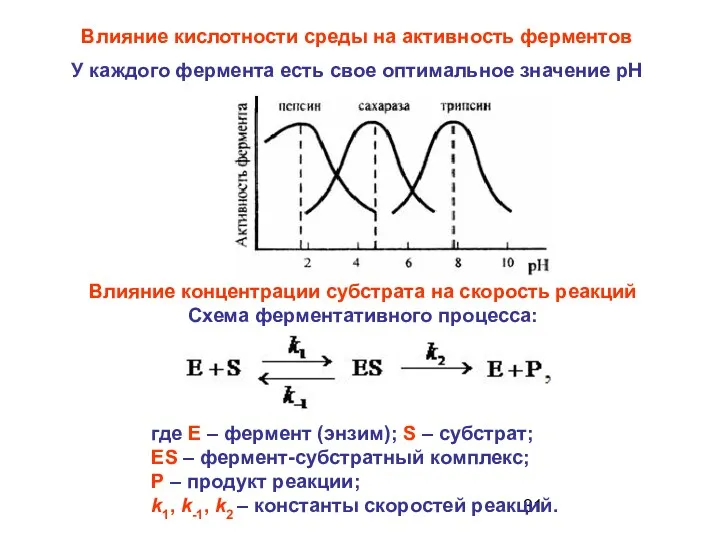
- 31. Влияние кислотности среды на активность ферментов У каждого фермента есть свое оптимальное значение рН Влияние концентрации
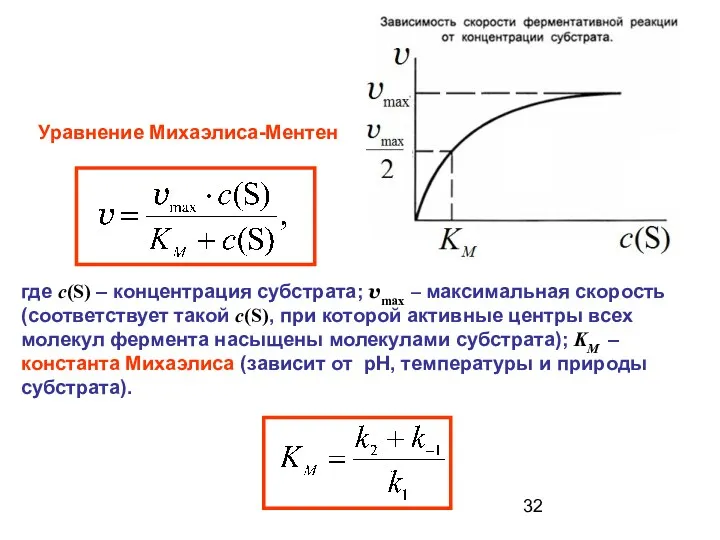
- 32. Уравнение Михаэлиса-Ментен где c(S) – концентрация субстрата; vmax – максимальная скорость (соответствует такой c(S), при которой
- 33. Физический смысл константы Михаэлиса Она численно равна концентрации субстрата c(S), при которой Чем она меньше, тем
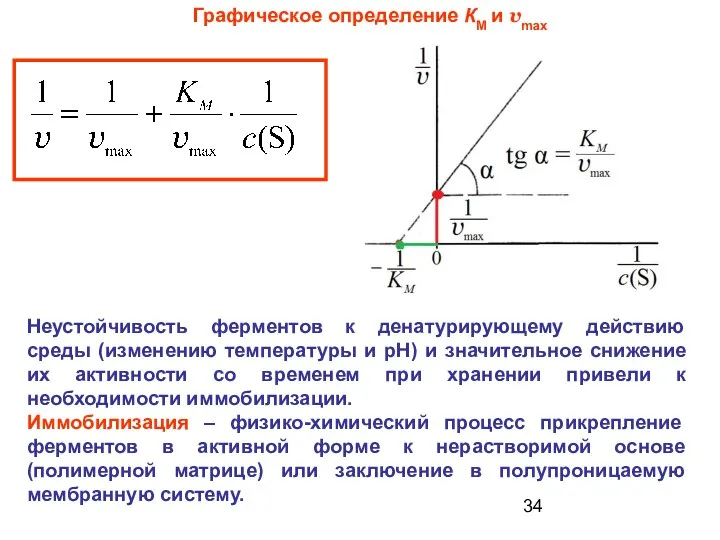
- 34. Графическое определение КМ и vmax Неустойчивость ферментов к денатурирующему действию среды (изменению температуры и рН) и
- 35. Значение ферментов и ферментативных реакций Применение ферментов в качестве лекарственных препаратов; Разработка методов диагностики с помощью
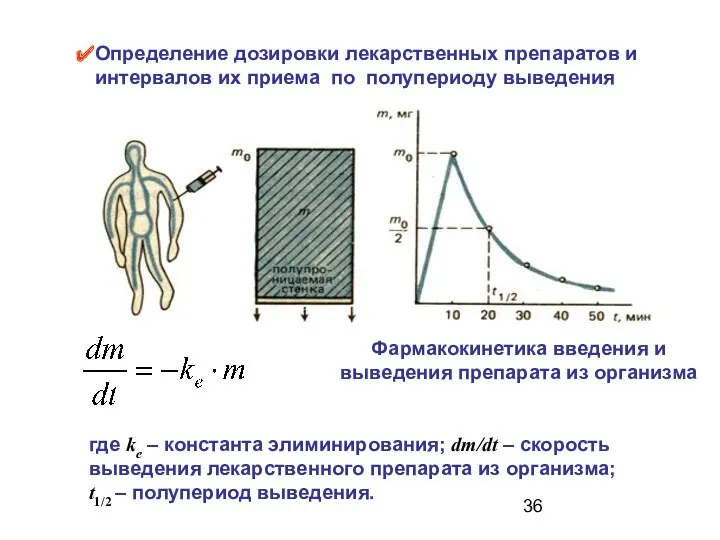
- 36. Определение дозировки лекарственных препаратов и интервалов их приема по полупериоду выведения Фармакокинетика введения и выведения препарата
- 37. Кафедра общей и медицинской химии «Химическое равновесие»
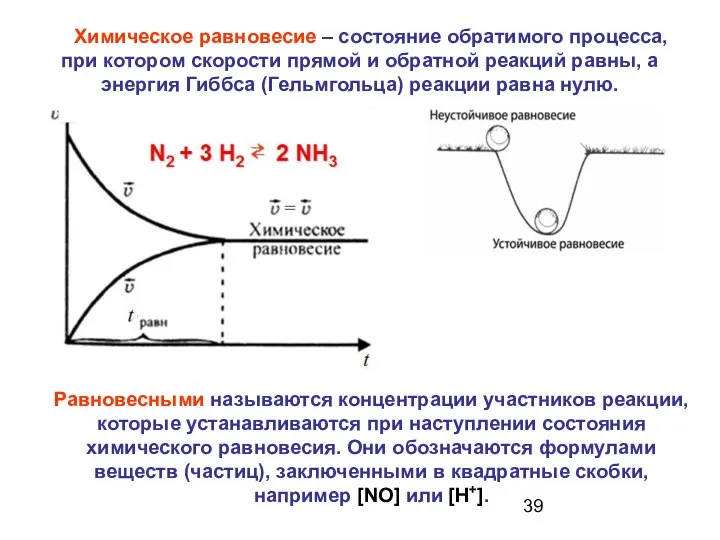
- 39. Химическое равновесие – состояние обратимого процесса, при котором скорости прямой и обратной реакций равны, а энергия
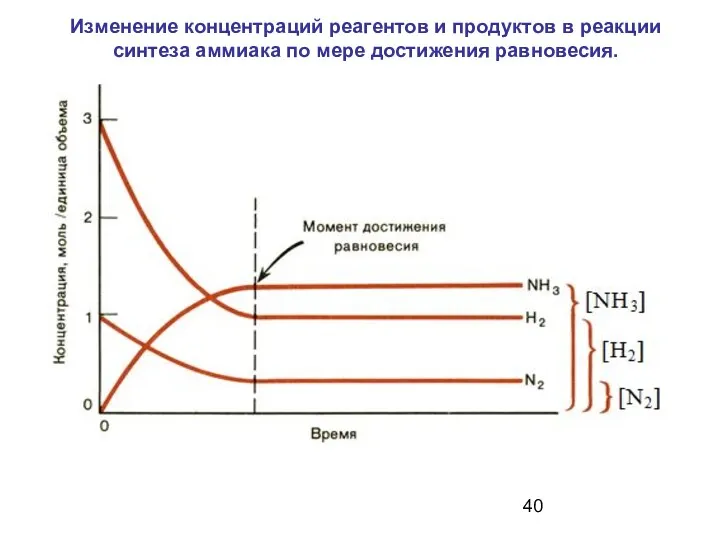
- 40. Изменение концентраций реагентов и продуктов в реакции синтеза аммиака по мере достижения равновесия.
- 41. Количественной характеристикой состояния равновесия является константа равновесия – постоянная при данной температуре для данной реакции величина,
- 42. Концентрации твердых и жидких (не растворённых!) веществ не входят в выражение констант равновесия гетерогенных реакций, вместо
- 43. Если считать, что прямая и обратная реакции являются простыми, то выражение константы равновесия может быть выведено
- 44. Состоянию равновесия соответствует определенное значение константы, т. е. соотношение равновесных концентраций. В одном состоянии может быть
- 45. Принцип Ле Шателье Если на систему, находящуюся в состоянии равновесия, оказывается внешнее воздействие, то равновесие смещается
- 46. прямая реакция – экзотермическая, обратная – эндотермическая, повышение температуры смещает равновесие влево, а понижение – вправо.
- 47. Если реагент добавляют в реакционную систему (повышают его концентрацию), то равновесие смещается вправо. Если же его
- 48. Рассмотрим добавление в эту систему жидкой воды, являющейся не только участником (реагентом), но и растворителем (разбавление).
- 49. Другими словами, после разбавления концентрации продуктов растут, что эквивалентно смещению равновесия вправо, т. е. добавление воды
- 50. В обеих частях уравнения суммы коэффициентов при формулах газов одинаковы и равны 4, поэтому изменение общего
- 52. Скачать презентацию



































 Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Соединения щелочных металлов
Соединения щелочных металлов Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ
Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ Відносна молекулярна маса речовини, її обчислення за хімічною формулою
Відносна молекулярна маса речовини, її обчислення за хімічною формулою Алканы
Алканы Химические свойства основных классов неорганических веществ
Химические свойства основных классов неорганических веществ Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек
Дистиляттағы цианидтер, алифаттық қатардағы галоген туындылары, хлороформ, хлоралгидрат, төртхлорлы көміртек Углеводородное сырье: способы переработки
Углеводородное сырье: способы переработки Предельные углеводороды
Предельные углеводороды Комплесные соединения
Комплесные соединения Мұнай. Мұнайдың шығу тарихы
Мұнай. Мұнайдың шығу тарихы Лекция 1. Периодический закон и периодическая система химических элементов. Индустрия красоты
Лекция 1. Периодический закон и периодическая система химических элементов. Индустрия красоты Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу
Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу Алкалоидтар түсінігі. Никотин, кофеин,морфин, хинин туралы түсініктер
Алкалоидтар түсінігі. Никотин, кофеин,морфин, хинин туралы түсініктер Неметаллические материалы, используемые в машино- и приборостроении
Неметаллические материалы, используемые в машино- и приборостроении Спирти. 3агальна характеристика спиртів
Спирти. 3агальна характеристика спиртів Алюминий и его соединения
Алюминий и его соединения Метаболизм нуклеиновых кислот
Метаболизм нуклеиновых кислот Азотистые гетероциклические соединения
Азотистые гетероциклические соединения Формы минералов и их агрегатов
Формы минералов и их агрегатов Химические свойства металлов
Химические свойства металлов Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Угарный газ
Угарный газ Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия
Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия Адсорбция. Разделение однородных и неоднородных смесей
Адсорбция. Разделение однородных и неоднородных смесей Ферум та його сполуки
Ферум та його сполуки Аминокислоты. Белки
Аминокислоты. Белки