Содержание
- 2. Запишите и заполните пропуски: Азот образует шесть оксидов. степени окисления +1 N2O +2 N…O… +3 N2O3
- 3. несолеобразующий +1 N2O оксид азота (I), закись азота или «веселящий газ», возбуждающе действует на нервную систему
- 4. NO +2 В природе образуется при разряде молнии: N2 + O2 = 2NO легко окисляется: 2N+2O
- 5. N2O3 +3 Химические свойства: NO2 + NO N2O3 Получение: ВСЕ свойства кислотных оксидов. кислотный оксид жидкость
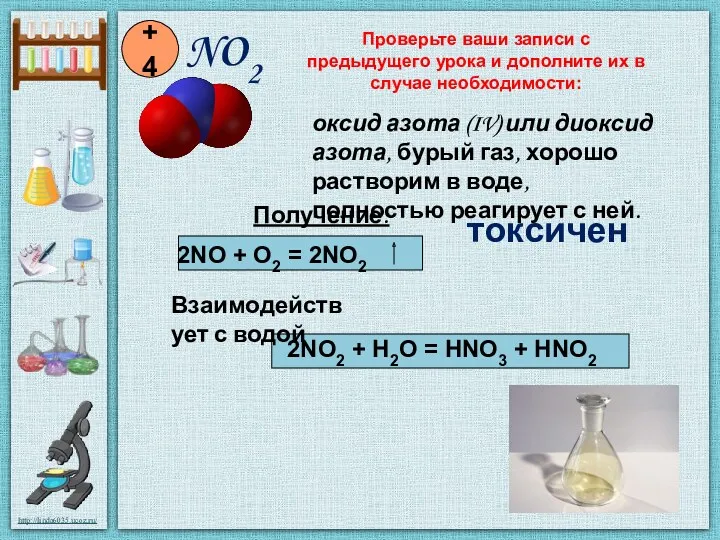
- 6. NO2 +4 Получение: 2NO + O2 = 2NO2 Взаимодействует с водой 2NO2 + H2O = HNO3
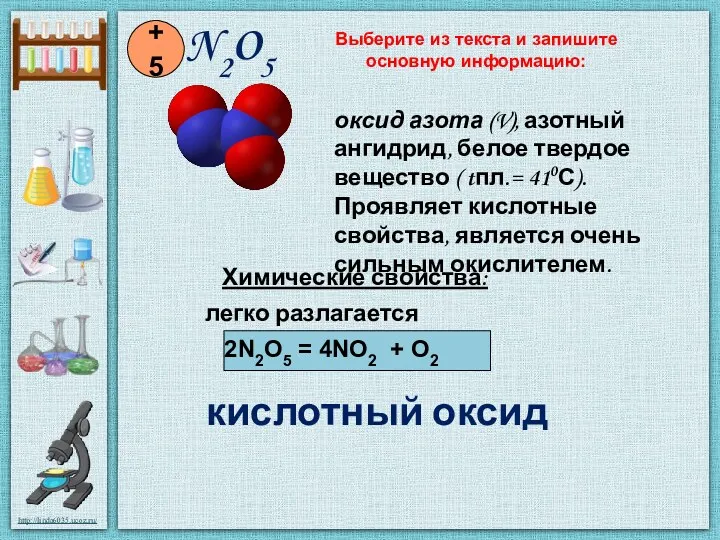
- 7. N2O5 +5 Химические свойства: легко разлагается 2N2O5 = 4NO2 + O2 кислотный оксид оксид азота (V),
- 8. HNO3 Азотная кислота. бесцветная гигроскопичная жидкость, c резким запахом, «дымит» на воздухе, неограниченно растворимая в воде.
- 9. Химические свойства азотной кислоты Азотная кислота проявляет все типичные свойства кислот. 1 3 2 3 1)
- 10. 4) особенности взаимодействия с металлами: (азотная кислота никогда не выделяет водород!) Me + HNO3 = Me(NO3)2
- 12. Скачать презентацию







 Биофизические основы патологии клетки. Свободные радикалы и болезни человека
Биофизические основы патологии клетки. Свободные радикалы и болезни человека Конструкционные функциональные волокнистые композиты. Стеклопластики
Конструкционные функциональные волокнистые композиты. Стеклопластики Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия
Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия Простые вещества
Простые вещества Приборы радиационной и химической разведки
Приборы радиационной и химической разведки Carbohydrates (sugars)
Carbohydrates (sugars) Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез Номенклатура органических соединений
Номенклатура органических соединений Основы химической термодинамики (лекция 6)
Основы химической термодинамики (лекция 6) алканы 170
алканы 170 Автомобильные эксплуатационные материалы и экономия топливно-энергетических ресурсов. Автомобильные бензины
Автомобильные эксплуатационные материалы и экономия топливно-энергетических ресурсов. Автомобильные бензины Ароматические углеводороды, строение, изомерия, номенклатура
Ароматические углеводороды, строение, изомерия, номенклатура Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Полисахаридтер – жоғары молекулалық көмірсулар
Полисахаридтер – жоғары молекулалық көмірсулар Массовая доля компонента вещества в смеси
Массовая доля компонента вещества в смеси Стекловолокно. Что такое стекловолокно?
Стекловолокно. Что такое стекловолокно? Геохимия ландшафтов
Геохимия ландшафтов Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Соли серной кислоты
Соли серной кислоты Летучие яды. Токсичные газы
Летучие яды. Токсичные газы Глицерин. Свойства и применение
Глицерин. Свойства и применение Свойства смесей ПАВ
Свойства смесей ПАВ Хлор (лат. Chlorum, Cl)
Хлор (лат. Chlorum, Cl) Коррозия и защита полимерных строительных материалов
Коррозия и защита полимерных строительных материалов Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов
Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов Жидкие кристаллы
Жидкие кристаллы Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Век пластмасс
Век пластмасс