Содержание
- 2. 1649 – Иоганн Гаубер - перегонка каменноугольной смолы 1825 – Майкл Фарадей – из конденсата светильного
- 3. Найдите молекулярную формулу углеводорода, содержащего 92,3% углерода, если относительная его плотность по водороду равна 39.
- 4. Физические свойства Бензол это жидкость, бесцветная, со своеобразным запахом. В воде не растворим, но в органических
- 5. Гомологический ряд бензола - 1 - 2 - 3 Записать структурные формулы
- 6. 1861 – Иоганн Лошмидт – предположил наличие цикла 1865 – Фридрих Август Кекуле – формула Кекуле
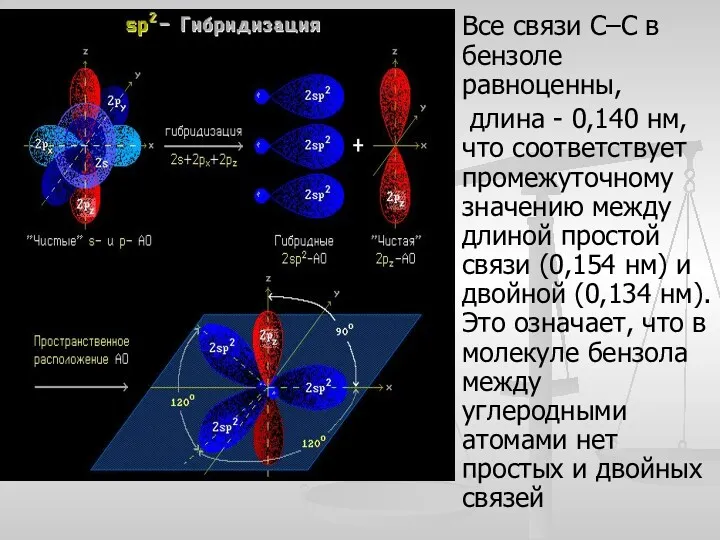
- 7. Все связи С–С в бензоле равноценны, длина - 0,140 нм, что соответствует промежуточному значению между длиной
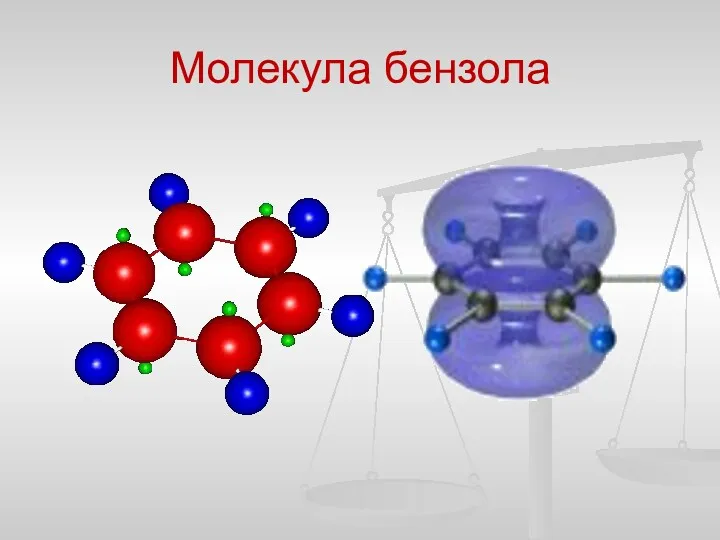
- 8. Молекула бензола
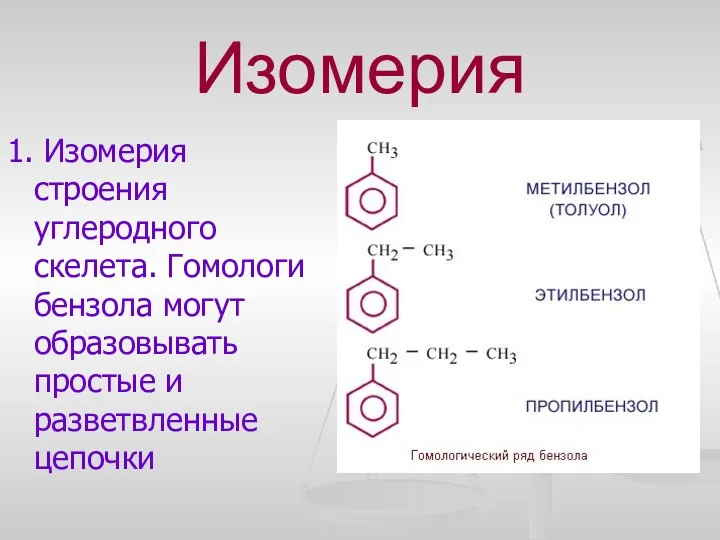
- 9. Изомерия 1. Изомерия строения углеродного скелета. Гомологи бензола могут образовывать простые и разветвленные цепочки
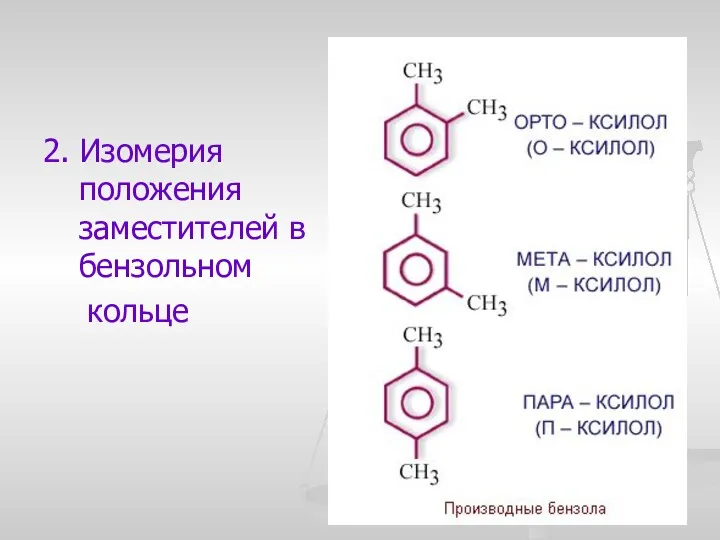
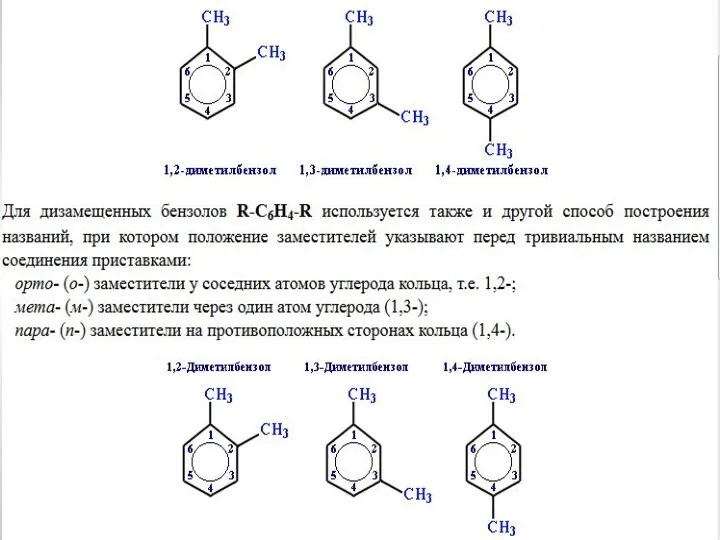
- 10. 2. Изомерия положения заместителей в бензольном кольце
- 11. 3. Изомерия положения двойной связи в молекулах непредельных гомологов бензола
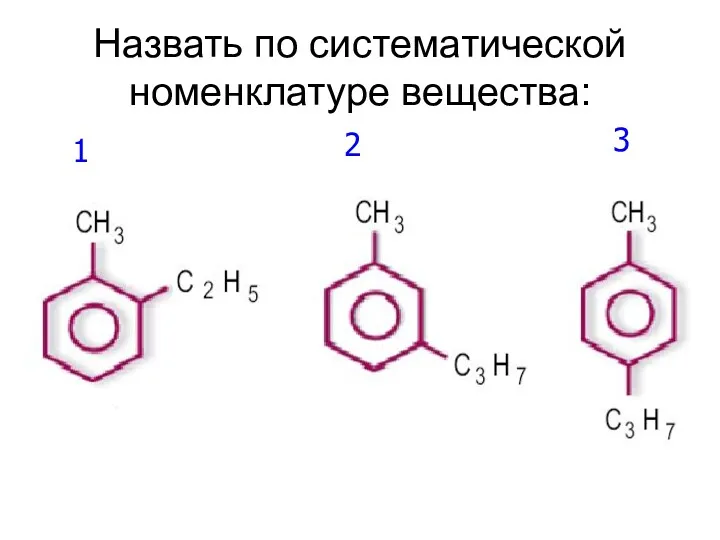
- 12. Назвать по систематической номенклатуре вещества: 1 2 3
- 13. Химические свойства Реакции присоединения гидрирование хлорирование Реакции замещения по бензольному кольцу бромирование нитрование алкилирование Реакции окисления
- 14. Реакции замещения галогенирование FeBr3 С6Н6 + Br2 C6H5Br + HBr Нитрование: H2SO4 С6Н6 + НОNО2 С6Н5NО2
- 15. Реакции присоединения 4. Гидрирование: С6Н6 + 3Н2 С6Н12 5. Хлорирование: свет С6Н6 + 3 Cl2 C6H6Cl6
- 16. Окисление 1.Горение бензола: 2С6Н6 + 15О2 = 12СО2 + 6Н2О Не окисляется даже сильными окислителями
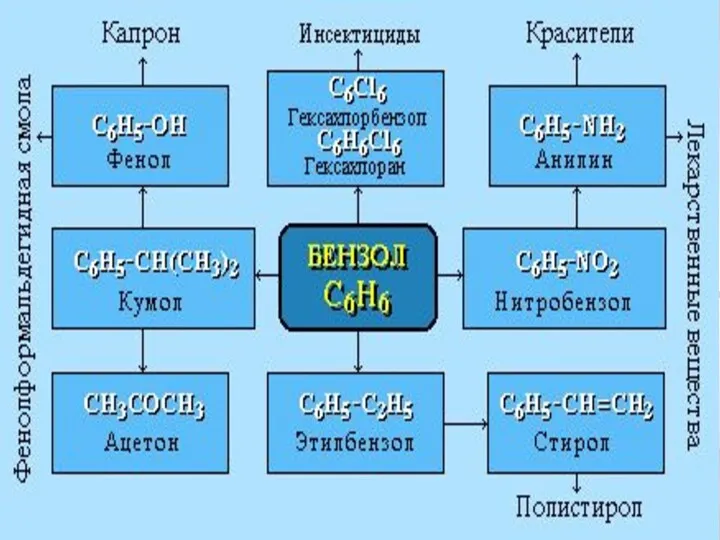
- 17. Получение Бензол получают из каменноугольной смолы, образующейся при коксовании угля. В настоящее время бензол получают из
- 18. С6Н14 ? С6Н6 + Н2 С6Н12 ? С6Н6 + 3Н2 3С2Н2 ? С6Н6 Другие способы получения
- 20. 1. Ароматическим углеводородам соответствует общая формула: а)СnН2n б)Сn Н2n-2 в)Сn Н2n-6 г)Сn Н2n+2 2.К ароматическим углеводородам
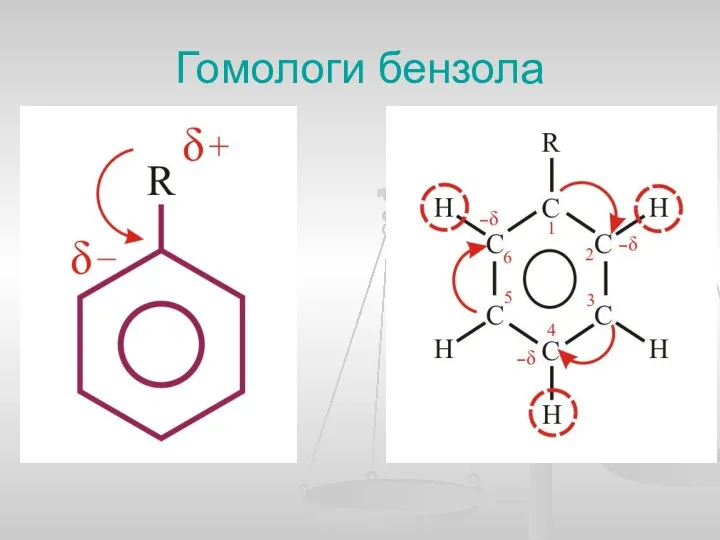
- 21. Гомологи бензола
- 22. Важнейшим фактором, определяющим химические свойства молекулы, является распределение в ней электронной плотности. Характер распределения зависит от
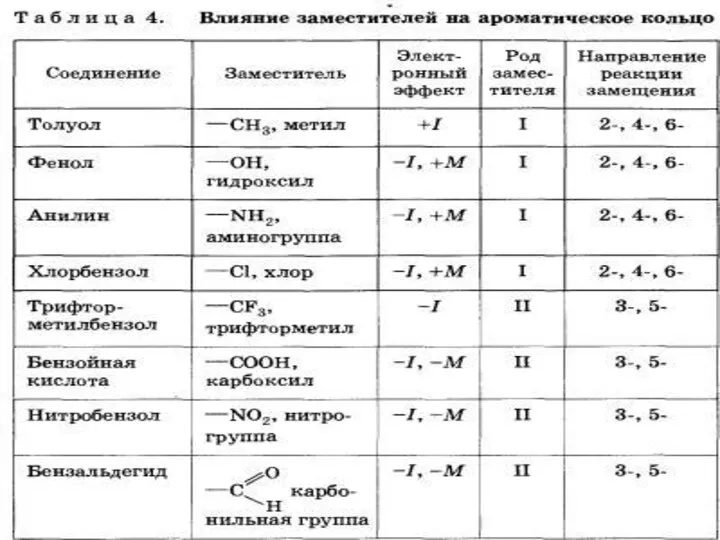
- 24. Заместители, обладающие +I-эффектом или +М-эффектом, способствуют электрофильному замещению в орто- и пара-положениях бензольного кольца и называются
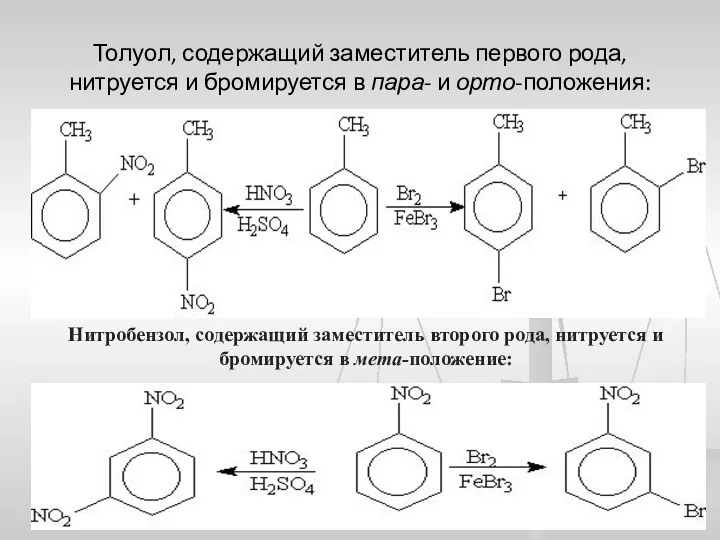
- 26. Толуол, содержащий заместитель первого рода, нитруется и бромируется в пара- и орто-положения: Нитробензол, содержащий заместитель второго
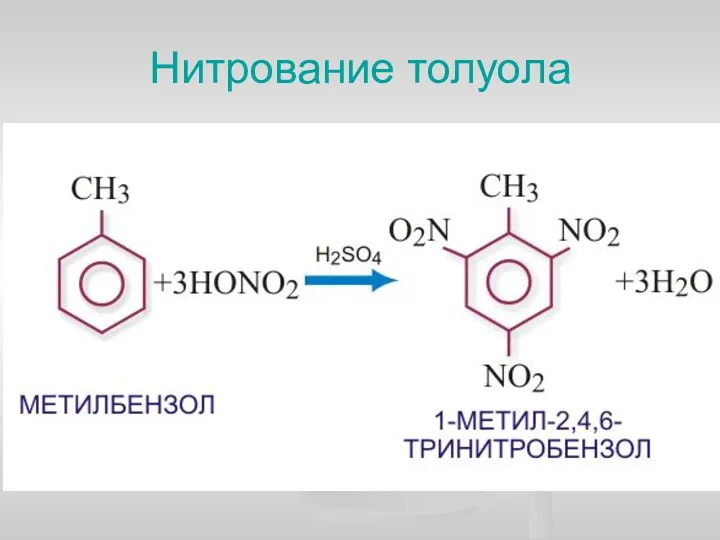
- 28. Нитрование толуола
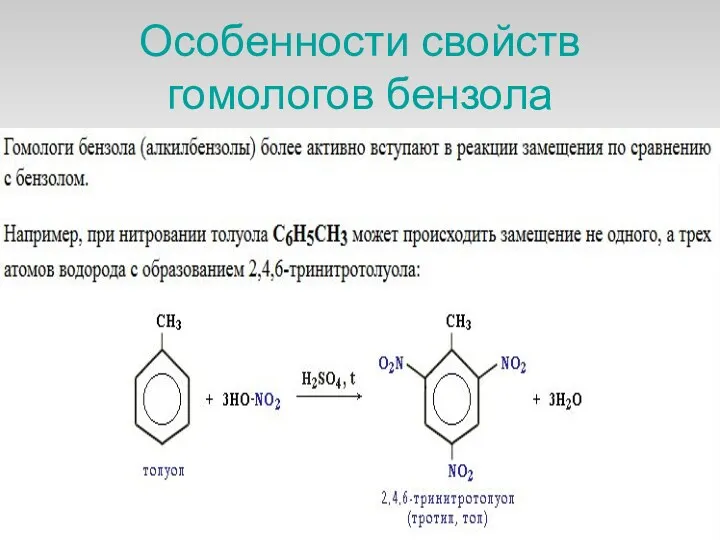
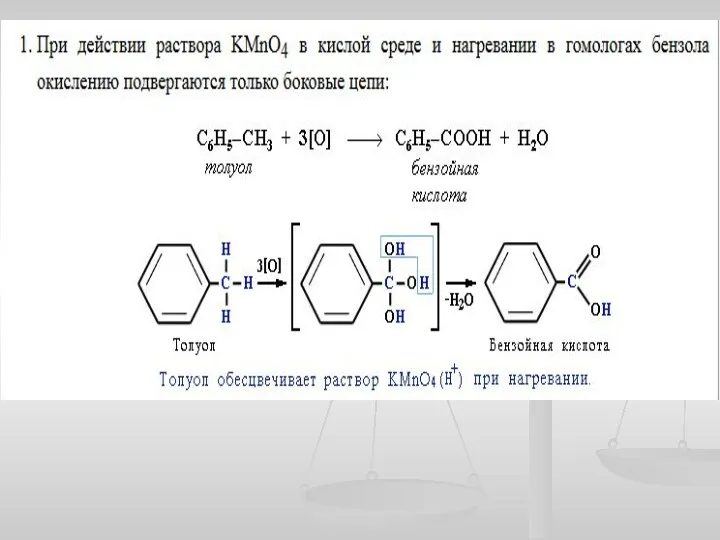
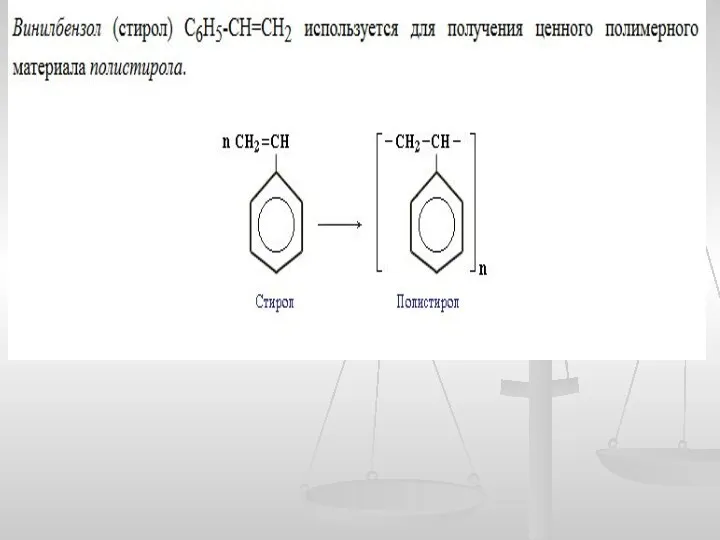
- 29. Особенности свойств гомологов бензола
- 35. Скачать презентацию


















 Амины
Амины Практическое занятие по основам биохимии с методами клинико-биохимических исследований
Практическое занятие по основам биохимии с методами клинико-биохимических исследований Свойства алкадиенов и их получение
Свойства алкадиенов и их получение Химия в организме человека
Химия в организме человека Марганец. Железо
Марганец. Железо Периодический закон и периодическая система Д.И. Менделеева. Вторичная периодичность. Тема №1
Периодический закон и периодическая система Д.И. Менделеева. Вторичная периодичность. Тема №1 Метод Молекулярных Орбиталей Хюккеля
Метод Молекулярных Орбиталей Хюккеля Халық арасында тез таралатын жұқпалы ауыру түрлері,Барсакелмес қорығы
Халық арасында тез таралатын жұқпалы ауыру түрлері,Барсакелмес қорығы Галогени. Знаходження в природі
Галогени. Знаходження в природі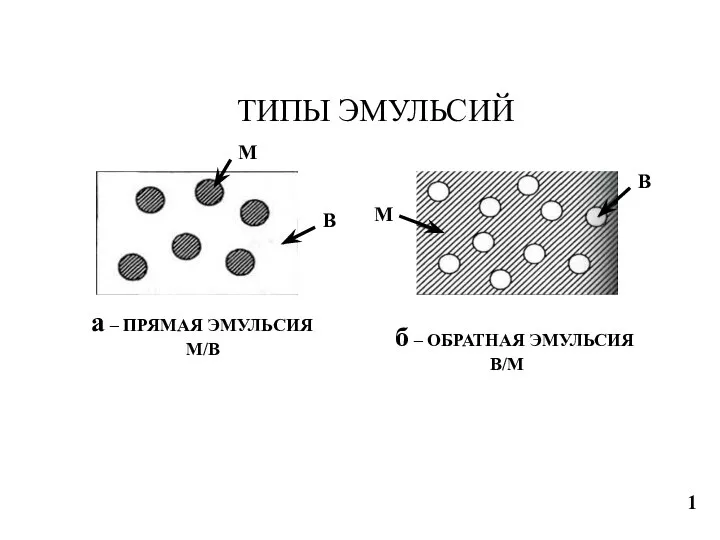 Типы эмульсий. Фракционный состав нефти. Типы нефти
Типы эмульсий. Фракционный состав нефти. Типы нефти Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13)
Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13) Химическая связь
Химическая связь Типы химических реакций
Типы химических реакций Природные источники углеводородов
Природные источники углеводородов Периодическая система химических элементов. Периоды
Периодическая система химических элементов. Периоды Лекция 2. Строение атома и Периодический закон Д.И. Менделеева
Лекция 2. Строение атома и Периодический закон Д.И. Менделеева Окислительно-восстановительные реакции
Окислительно-восстановительные реакции химиияяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяя
химиияяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяя Чистые вещества и смеси
Чистые вещества и смеси Самое удивительное на свете вещество - вода
Самое удивительное на свете вещество - вода Органическая химия. ДО. Глицерин как представитель многоатомных спиртов
Органическая химия. ДО. Глицерин как представитель многоатомных спиртов Металлы применяемые в строительстве
Металлы применяемые в строительстве Новые интеллектуальные материалы на основе полимеров
Новые интеллектуальные материалы на основе полимеров Химическая термодинамика
Химическая термодинамика Химический состав клетки. Неорганические вещества клетки. 10 класс
Химический состав клетки. Неорганические вещества клетки. 10 класс Введение. Методы и средства обучения химии
Введение. Методы и средства обучения химии Теоретические основы органической химии
Теоретические основы органической химии Рідкі кристали та їх властивості
Рідкі кристали та їх властивості