Алкадиены: гомологический ряд, общая формула, номенклатура. Сопряжённые, изолированные, кумулированные презентация
Содержание
- 2. Диеновые углеводороды или алкадиены —это непредельные, ациклические углеводороды, содержащие две двойные связи между атомами углерода. Общая
- 3. Гомологический ряд алкадиенов Диены образуют гомологический ряд пропандиена. Это простейший представитель алкадиенов. Названия гомологов согласно номенклатуре
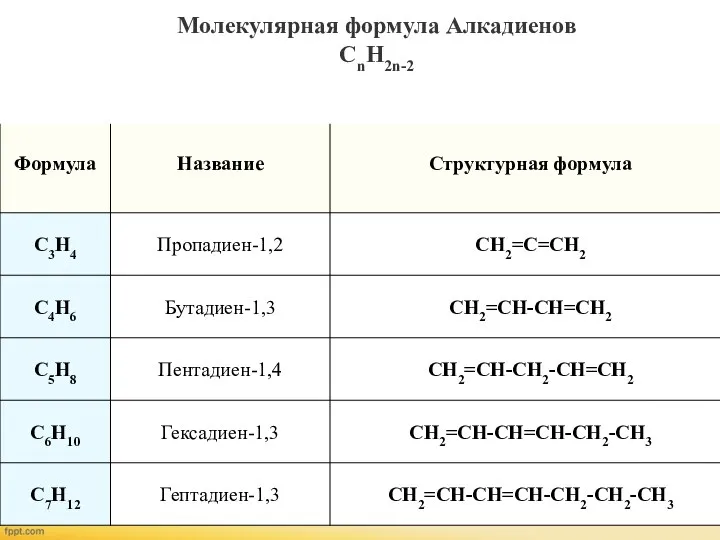
- 4. Молекулярная формула Алкадиенов CnH2n-2
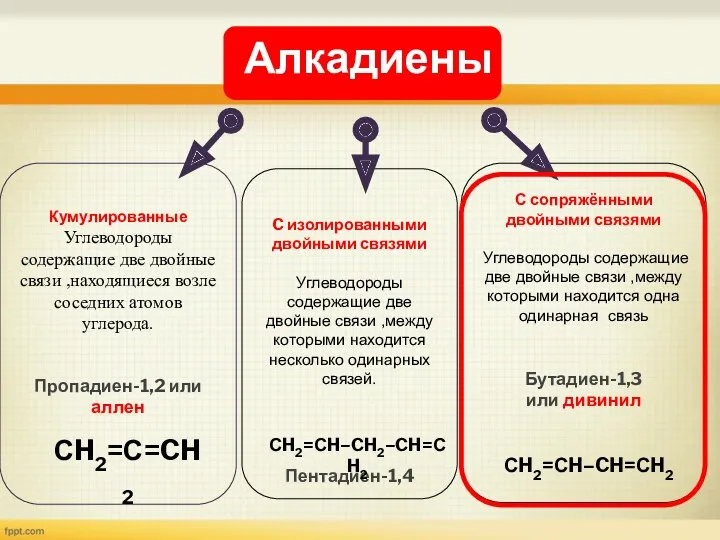
- 5. Кумулированные Углеводороды содержащие две двойные связи ,находящиеся возле соседних атомов углерода. Пропадиен-1,2 или аллен C изолированными
- 6. Электронное строение диенов π-электроны двойных связей образуют единое π-электронное облако (сопряженную систему) и делокализованы между всеми
- 7. 1.Сопряженные двойные связи разделены одной σ- связью: СН2=СН–СН=СН2 бутадиен -1, 3 (дивинил) СН3 -СН=СН-СН=СН-СН3 гексадиен-2, 4
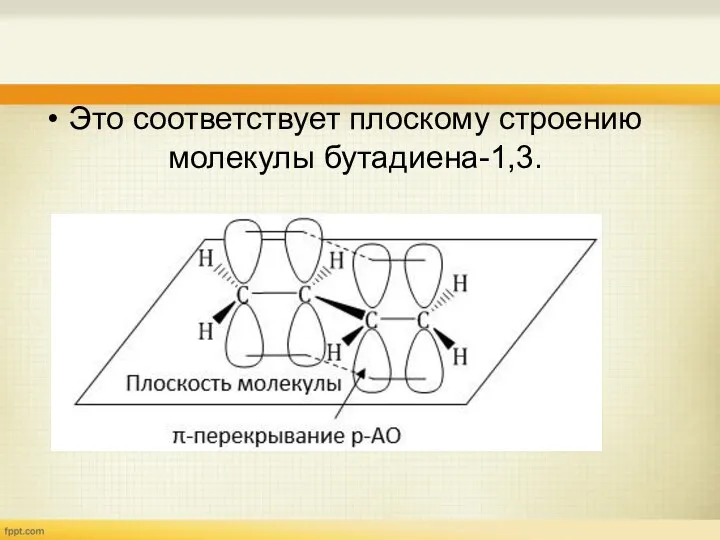
- 8. Это соответствует плоскому строению молекулы бутадиена-1,3.
- 9. Алкадиены с сопряжёнными двойными связями Пример: СН3 – СН = СН – СН = СН2 Другие
- 10. Кумулированные двойные связи расположены у одного атома углерода: СН2=С=СН2 (аллен) Подобные диены (аллены) относятся к довольно
- 11. Алкадиены с кумулированными двойными связями Пример: СН2 = С = СН2 Другие названия: кумулированные диены, 1,2-диены.
- 12. Изолированные двойные связи разделены в цепи двумя или более σ- связями: СН2=СН–СН2–СН=СН2. Диены этого типа проявляют
- 13. Алкадиены с изолированными двойными связями Пример: СН2 = СН – СН2 – СН = СН2 Другие
- 14. Номенклатура алкадиенов Главная цепь должна содержать обе двойные связи. Нумерацию ведут с того конца где ближе
- 15. Номенклатура алкадиенов Правила: 1. Главная цепь должна содержать обе двойные связи. 2. Нумерацию ведут с того
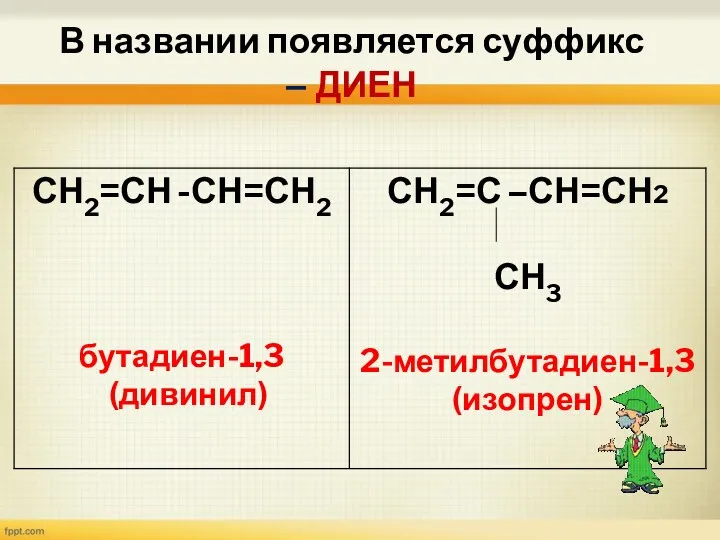
- 16. В названии появляется суффикс – ДИЕН
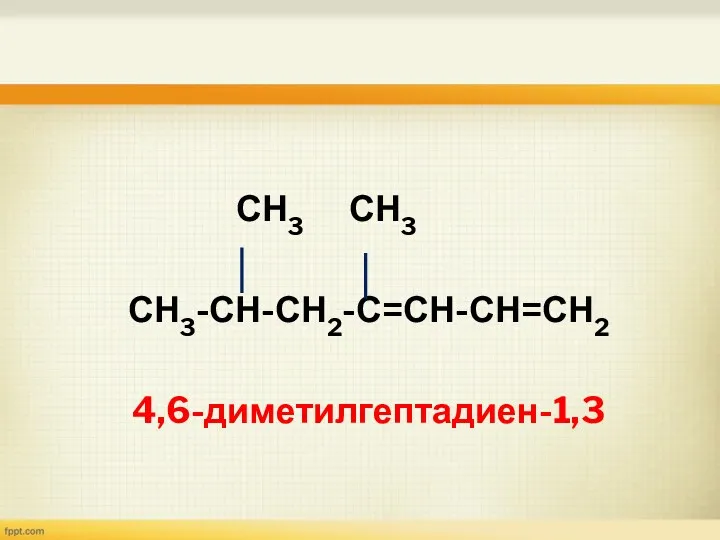
- 17. СН3 СН3 СН3-СН-СН2-С=СН-СН=СН2 4,6-диметилгептадиен-1,3
- 18. 1. Структурная: а) изомерия углеродного скелета б) изомерия положения двойных связей. 2. Пространственная: а)цис- и транс-
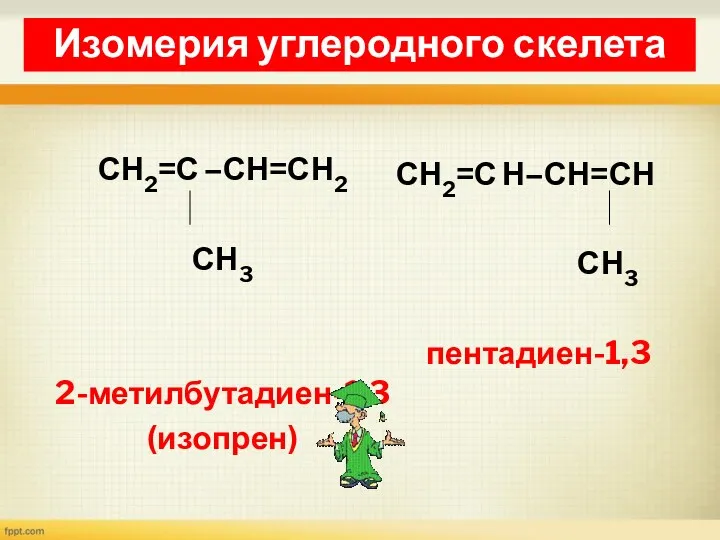
- 19. Изомерия диенов Изомерия углеродного скелета СН2=С –СН=СН2 СН3 2-метилбутадиен-1,3 (изопрен) СН2=С Н–СН=СН СН3 пентадиен-1,3
- 20. Изомерия положения двойных связей СН2 = СН – СН = СН2 бутадиен-1,3 СН2 = С =
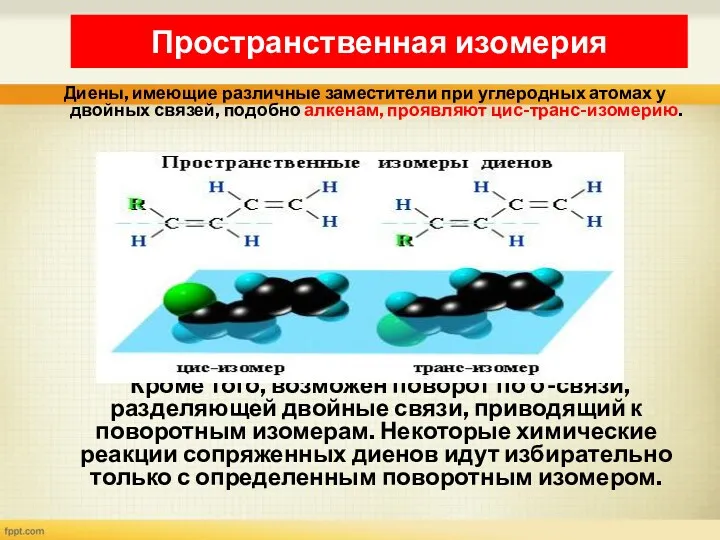
- 21. Диены, имеющие различные заместители при углеродных атомах у двойных связей, подобно алкенам, проявляют цис-транс-изомерию. Кроме того,
- 22. Межклассовая изомерия С алкинами и циклоалкенами Например, формуле С4Н6 соответствуют следующие соединения:
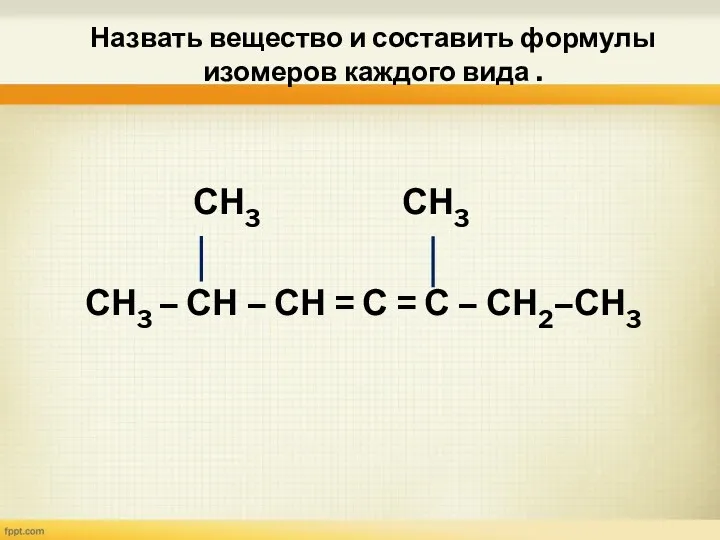
- 23. Назвать вещество и составить формулы изомеров каждого вида . СН3 СН3 СН3 – СН – СН
- 25. Скачать презентацию














 Atomic mass
Atomic mass Бытовая химия
Бытовая химия Каучук. Открытие каучука
Каучук. Открытие каучука Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Окислительновосстановительные реакции (ОВР)
Окислительновосстановительные реакции (ОВР) Кремний и его соединения
Кремний и его соединения Типы химических реакций в органической химии
Типы химических реакций в органической химии Химическая связь. 8 класс
Химическая связь. 8 класс Окислительно-восстановительные реакции. Генетический ряд кальция
Окислительно-восстановительные реакции. Генетический ряд кальция Ациклические углеводороды
Ациклические углеводороды Углеводы (сахариды)
Углеводы (сахариды) Стекло. Виды стекол
Стекло. Виды стекол Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Коррозия металлов. Методы защиты металлов от коррозии
Коррозия металлов. Методы защиты металлов от коррозии Поверхностные явления на границе раздела фаз. Хроматография, применение в медицинской практике
Поверхностные явления на границе раздела фаз. Хроматография, применение в медицинской практике Цікаві історичні факти з походження назв хімічних елементів
Цікаві історичні факти з походження назв хімічних елементів Химическая промышленность. Минеральные удобрения
Химическая промышленность. Минеральные удобрения Кислород и оксиген
Кислород и оксиген История открытия кислорода
История открытия кислорода Неорганические соединения галогенов
Неорганические соединения галогенов Выращивание кристаллов
Выращивание кристаллов Теплогенерация. Топливо и его горение
Теплогенерация. Топливо и его горение Задачи по химии
Задачи по химии Тіршілік гетерофункционалды қосылыстар
Тіршілік гетерофункционалды қосылыстар Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію Бериллий, магний и щелочноземельные металлы
Бериллий, магний и щелочноземельные металлы Коллигативные свойства растворов неэлектролитов
Коллигативные свойства растворов неэлектролитов Методы выделения и очистки продуктов биотехнологических производств
Методы выделения и очистки продуктов биотехнологических производств