Содержание
- 2. Коррозия – самопроизвольно протекающий процесс разруше-ния Ме при химическом и электрохимическом взаимодей-ствии с окружающей средой.
- 3. Большинство Ме находятся в природе в окисленном состоянии (в оксидах и солях, образующих различные минералы и
- 4. Авария на Саяно-Шушенской ГЭС (17.08.2009) Саяно-Шушенская ГЭС – крупнейшая электростанция России (на р. Енисей), высота плотины
- 5. При выборе конструкционных материалов наряду с необходимыми характеристиками этого материала всегда должна оцениваться его коррозионная устойчивость
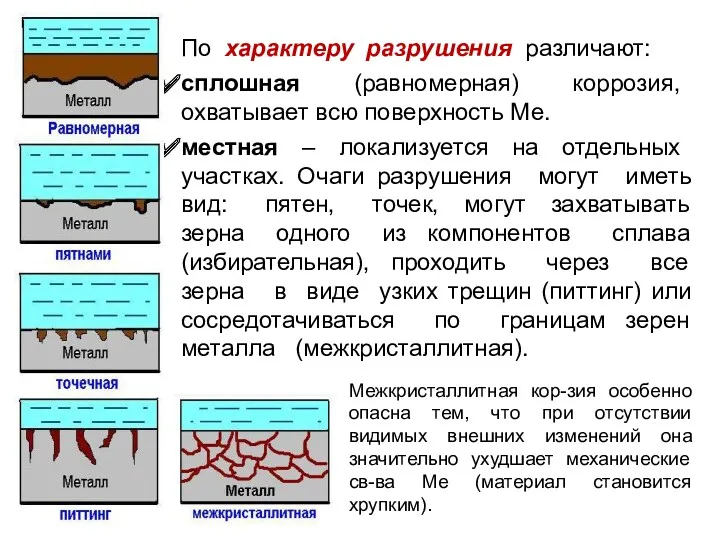
- 6. По характеру разрушения различают: сплошная (равномерная) коррозия, охватывает всю поверхность Ме. местная – локализуется на отдельных
- 7. По механизму протекания коррозионных процессов различают: химическая; электрохимическая коррозия. Химическая коррозия – окисление Ме в средах,
- 8. Э/Х коррозия – процесс само-произвольного разрушения Ме в среде электролита в результате образования на поверхности Ме
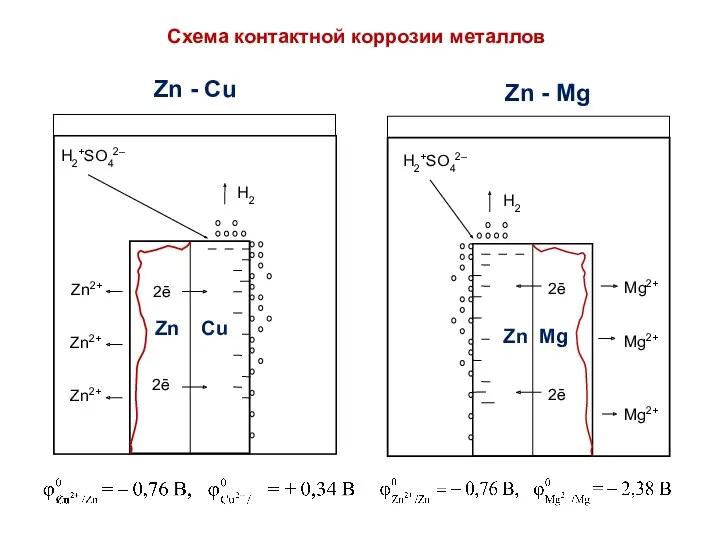
- 9. Причины Э/Х коррозии 1. Контакт 2-х разных по природе металлов в присутствии проводящей жидкости: А(–) Ме(1)
- 11. Zn + Н2SO4 = ZnSO4 + Н2 в-ль ок-ль φок-ля > φвос-ля, реакция протекает. Cu +
- 12. 2. Контакт c примесью другого металла в структуре конструкционного материала: А(–) Ме(1) | электролит | примесь
- 13. 3. Контакт в одном изделии участка самого Ме и соединения этого Ме в среде электролита. Контакт
- 14. 4. Неодинаковая механическая обработка различных участков одного и того же Ме (детали). Обработанная часть детали по
- 15. 5. Различные концентрации электролита. Создается пара даже на одном металле, т.к. концентрация ионов в электролите влияет
- 16. 6. Неравномерное насыщение кислородом различных участков металла. Наиболее окисленный участок Ме (бо́льший доступ О2) является Э/Х
- 17. Во всех случаях на поверхности Ме-ких конструкций самопроизвольно возникают макро- и микро- ГЭ, в которых протекает
- 18. В процессе коррозии электроды гальванопары поляризуются вследствие перехода ē-нов с анода на катод. Явление поляризации проявляется
- 19. По характеру катодного процесса различают коррозию с водородной и кислородной деполяризацией. Если окислителем (деполяризатором) являются катионы
- 20. Условия самопроизвольного протекания Э/Х коррозии: электрохимическое — Е > 0 (φк > φa), термодинамическое — ∆G
- 21. Скорость Э/Х коррозии зависит: природы металла (φ0); характера коррозионной среды (рН); наличия активаторов коррозии (O2, Сl–);
- 22. Химическая устойчивость Ме-ких конструкций к коррозии в значительной степени зависит от склонности Ме к пассивации (образование
- 23. Пример: Рассмотрим возможность коррозии стальной детали с медными заклепками в условиях влажной атмосферы (H2O, O2, pH=7).
- 24. Пример: Рассмотрим возможность коррозии стальной детали в условиях влажной атмосферы (H2O, O2, pH=7). А(–) Fе |
- 25. Пример: Рассмотрим возможность коррозии стальной детали в условиях кислой среды без доступа кислорода (H+, H2O, pH=2).
- 26. Пример: Железо и свинец находятся в растворе NaCl, контактирующим с воздухом (pH=7). Оценить возможность коррозии железа
- 27. Защита металлов от коррозии Выбор способа защиты от коррозии определяется природой корродирующего Ме, видом оборудования и
- 28. 2. Изменение состава коррозионной среды. Удаление активаторов коррозии (O2, Cl–, H+). При герметизации в приборостроительной практике
- 29. 3. Создание защитных покрытий на поверхности Ме. Окраска, покрытие специальными лаками и эмалями. Химические покрытия –
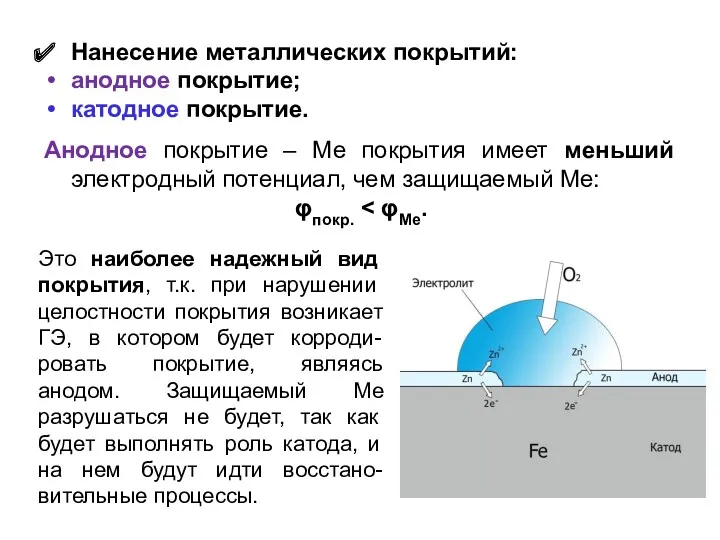
- 30. Нанесение металлических покрытий: анодное покрытие; катодное покрытие. Анодное покрытие – Ме покрытия имеет меньший электродный потенциал,
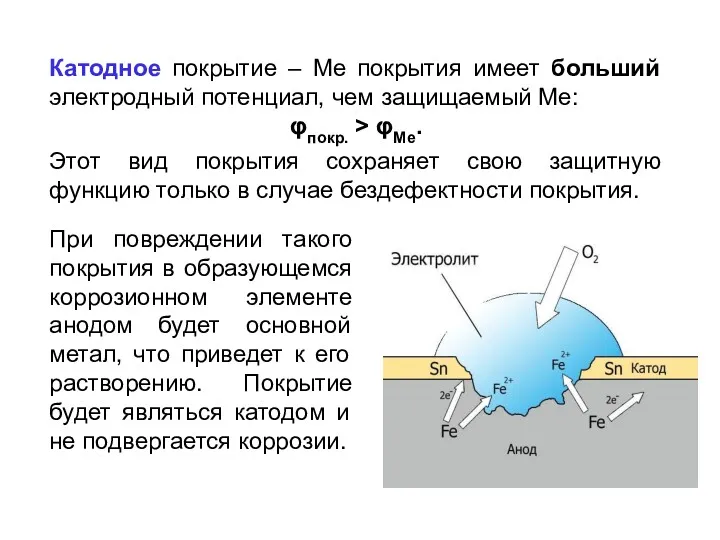
- 31. Катодное покрытие – Ме покрытия имеет больший электродный потенциал, чем защищаемый Ме: φпокр. > φМе. Этот
- 32. Пример: Железо покрыто хромом. Установите вид покрытия. Что происходит при нарушении цельности покрытия в условиях: влажного
- 33. Пример: Железо покрыто оловом. Установите вид покрытия. Что происходит при нарушении цельности покрытия в условиях: влажного
- 34. 3. Электрохимическая защита: протекторная; катодная. Защита от коррозии достигается тем, что защищаемая конструкция становится катодом в
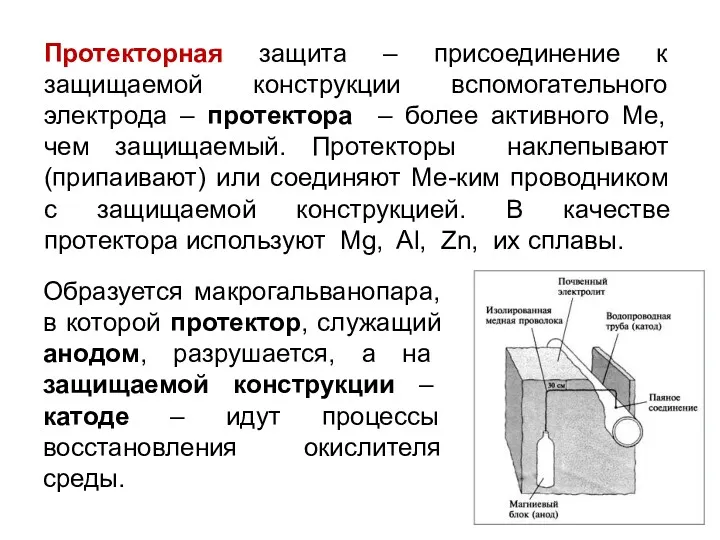
- 35. Протекторная защита – присоединение к защищаемой конструкции вспомогательного электрода – протектора – более активного Ме, чем
- 36. Эффективность протекторной защиты зависит от электрической проводимости среды, разности потенциалов между протектором и защищаемой конструкцией, способа
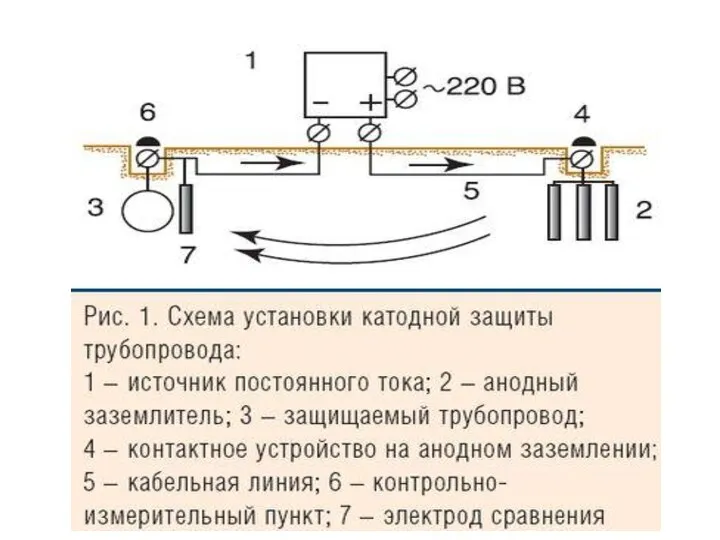
- 37. Катодная защита (электрозащита) по своей сути сводится к процессу электролиза водного р-ра электролита (подземные почвенные воды,
- 38. В результате создается электролизная система, в которой защищаемая конструкция является катодом, на нем идут процессы восстановления
- 41. Пример: Составьте схему катодной защиты стальной конструкции в условиях нейтральной почвы. К(–) Fе | Н2О, O2,
- 42. Пример: Составьте схему катодной защиты стального образца в условиях эксплуатации в растворе NaCl. К(–) Fе |
- 44. Скачать презентацию



































 Химия. Изучение жиров
Химия. Изучение жиров Электронное строение атома и Периодический закон
Электронное строение атома и Периодический закон Алкины. Ацетиленовые углеводороды
Алкины. Ацетиленовые углеводороды Кислоты
Кислоты Интересные факты о химических веществах
Интересные факты о химических веществах Простые вещества. Игра Счастливый случай
Простые вещества. Игра Счастливый случай Классификация химических веществ СГС
Классификация химических веществ СГС Элементарные частицы вещества
Элементарные частицы вещества Закон сохранения массы веществ. Урок вместе с умной колонкой
Закон сохранения массы веществ. Урок вместе с умной колонкой Загальні способи добування солей. Класифікація неорганічних речовин
Загальні способи добування солей. Класифікація неорганічних речовин Полимерные материалы, пластмассы и изделия из них
Полимерные материалы, пластмассы и изделия из них Гидроксикислоты (оксикислоты)
Гидроксикислоты (оксикислоты) Три правила взаимодействия элементов симметрии
Три правила взаимодействия элементов симметрии Фенолы
Фенолы Геохимия и космохимия: история возникновения и развития, основное содержание и задачи
Геохимия и космохимия: история возникновения и развития, основное содержание и задачи Закон сохранения массы вещества. Уравнения химических
Закон сохранения массы вещества. Уравнения химических Строение атома
Строение атома Електроліти
Електроліти Механика полимеров
Механика полимеров Фосфор и его соединения (9 класс)
Фосфор и его соединения (9 класс) Vi топ элементтері. Оттегі, күкірт қасиеттері және қосылыстары
Vi топ элементтері. Оттегі, күкірт қасиеттері және қосылыстары An introduction to the chemistry of alkenes
An introduction to the chemistry of alkenes Минерал хромдиопсид. Месторождения
Минерал хромдиопсид. Месторождения Сероводород и его свойства
Сероводород и его свойства Сполуки неметалічних елементів з Гідрогеном
Сполуки неметалічних елементів з Гідрогеном Количество вещества. Лекция №2
Количество вещества. Лекция №2 Азотсодержащие органические соединения. Амины
Азотсодержащие органические соединения. Амины Средние породы
Средние породы