Содержание
- 2. Генетический ряд кальция Ca CaO Ca(OH)₂ Ca₃(PO₄)₂ 2Са⁰ + О₂⁰ = 2Са⁺²О¯² Са⁺²О¯² + Н₂⁺О¯² =
- 3. Химические реакции Реакции, протекающие без изменения степени окисления Na+O-2H+ + H+N+5O-23 = Na+N+5O-23 + H+2O-2 2)
- 4. Степень окисления – условный заряд атомов химического элемента в соединении, рассчитанный исходя из условия, что все
- 5. Расчет степени окисления Следует запомнить: 1. Степени окисления атомов в простых веществах равны нулю: Na0; H20
- 6. Расчет степени окисления 1. Для веществ из двух элементов: -поставить постоянную степень окисления CO-2 -рассчитать степень
- 7. Расчет степени окисления 2. Для веществ из трех и более элементов: -поставить постоянные степени окисления H+1MnO4-2
- 8. Окислительно-восстановительные реакции Реакции, протекающие с изменением степени окисления, называются окислительно-восстановительными реакциями. Mn+4O2 + 4HCl-1 = Mn+2Cl2
- 9. Окислитель - частица (атом, ион), которая в ходе окислительно-восстановительного процесса принимает электроны Типичные окислители К ним
- 10. Восстановитель - частица (атом, ион), которая в ходе окислительно-восстановительного процесса отдает электроны Типичные восстановители К ним
- 11. Сочиняют дети… Окислитель, как отъявленный злодей, Как пират, бандит, агрессор, Бармалей, Отнимает электроны - и OK!
- 12. Восстановитель – это тот, Кто электроны отдает. Сам отдает грабителю, Злодею – окислителю!
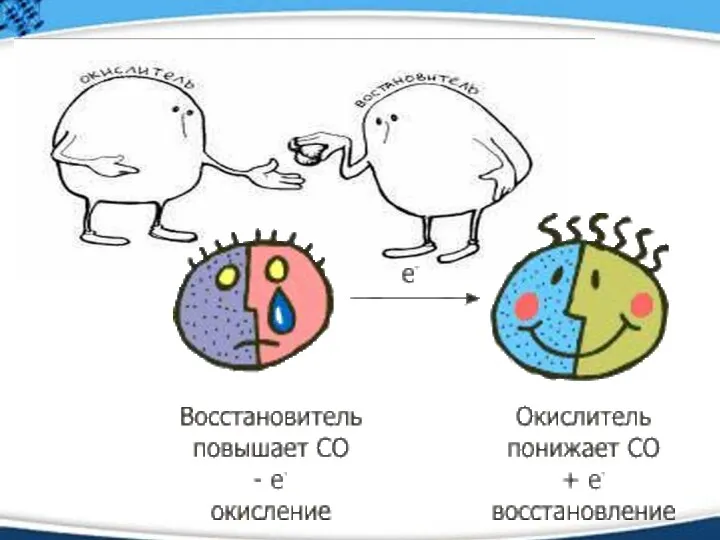
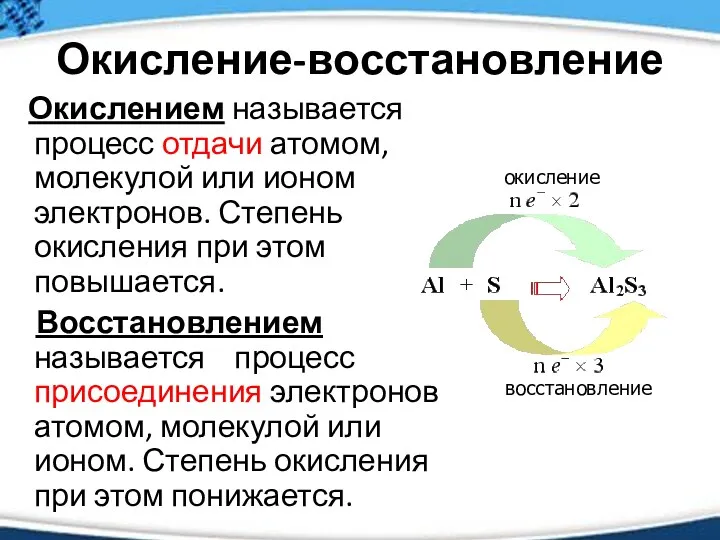
- 14. Окисление-восстановление Окислением называется процесс отдачи атомом, молекулой или ионом электронов. Степень окисления при этом повышается. Восстановлением
- 15. Окисление-процесс отдачи электронов H20 - 2ē 2H+ восстановитель S-2 - 2ē = S0 Al0 - 3ē
- 16. Восстановление –процесс присоединения электронов Mn+4 + 2ē Mn+2 окислитель S0 + 2ē = S-2 Cr+6 +3ē
- 17. Выполните задание: Расставьте СО. Определите какие реакции относятся к ОВР. Укажите окислитель и восстановитель, окислительный и
- 18. Домашнее задание: § 43 (стр. 229-231); задание 1.
- 19. Окислительно-восстановительные реакции Метод электронного баланса
- 21. Скачать презентацию















 Rates of reaction
Rates of reaction Пластмассалар, пластикалық материалдар
Пластмассалар, пластикалық материалдар Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки
Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки Азот. Аммиак (9 класс)
Азот. Аммиак (9 класс) Розрахункові задачі. Обчислення за хімічними рівняннями. Відносного виходу продукту реакції
Розрахункові задачі. Обчислення за хімічними рівняннями. Відносного виходу продукту реакції Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню
Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii
osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii Ароматические соединения
Ароматические соединения Строение электронных оболочек атомов химических элементов 8 класс
Строение электронных оболочек атомов химических элементов 8 класс Относительная атомная и молекулярная массы
Относительная атомная и молекулярная массы Кислоты. Состав, названия и определение кислот
Кислоты. Состав, названия и определение кислот Introduction to Periodic Table
Introduction to Periodic Table Алкилсульфонаттарды алу және технологиялық сызбанұсқасы
Алкилсульфонаттарды алу және технологиялық сызбанұсқасы Окисно-відновні реакції. 9 клас
Окисно-відновні реакції. 9 клас Етери та естери
Етери та естери Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1)
Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1) Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Вуглеводи. Класифікація вуглеводів
Вуглеводи. Класифікація вуглеводів Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров
Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров Аминокислоты N H2 – C H – C O O H
Аминокислоты N H2 – C H – C O O H Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички
Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички Азотная кислота
Азотная кислота Коррозия металлов. Классификация коррозионных процессов
Коррозия металлов. Классификация коррозионных процессов Подземное хранение газа и жидкости
Подземное хранение газа и жидкости Масса и формулы. Химия 8 класс
Масса и формулы. Химия 8 класс Метал конструкциялық материалдар
Метал конструкциялық материалдар Вуглеводи
Вуглеводи Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ