Содержание
- 3. КЕЙБІР МЕТАЛДАР Сілтілік металдар: Литий Натрий Калий Рубидий Цезий Франций Сітілік-жер металдар: Магний Кальций Стронций Барий
- 4. Амфотерлі (екідайлы) металдар: Алюминий Галлий Қорғасын Қалайы Бериллий Мырыш Бағалы металдар: Рутений Родий Палладий Осмий Иридий
- 5. МЕТАЛДАРДЫҢ ХИМИЯЛЫҚ ҚАСИЕТТЕРІ Жай заттармен: 2Mg + 02 = 2MgO + Q жану реакциясы Fe +
- 6. Күрделі заттармен: Сілтілік және сілтілік жер металдар сумен куатты әрекеттесіп, судағы сутекті ығыстырып шығарады. 2Na +
- 7. МЕТАЛДАРДЫ АЛУ ӘДІСТЕРІ Құрамында металл қосылыстары бар минералдар мен тау жыныстарынан металды өнеркөсіптік жолмен беліп алу
- 8. Металл аққыштығы– жүктеме берілу кезінде металдың пластикалық пішінсіздену қасиеті. Металл аққыштығы – жартылай өңделген өнімдерден дайындамалардың
- 9. Металдардың активтілік қатары Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La,
- 11. Скачать презентацию








 Таза зат және қоспа. Қоспаларды бөлу әдістері. Қосылыс Рure substances and mixtures . Мethods for separating mixtures. Compound
Таза зат және қоспа. Қоспаларды бөлу әдістері. Қосылыс Рure substances and mixtures . Мethods for separating mixtures. Compound Фуллерен С60 и его аналоги
Фуллерен С60 и его аналоги Кристаллические решётки и их виды
Кристаллические решётки и их виды Азотная кислота
Азотная кислота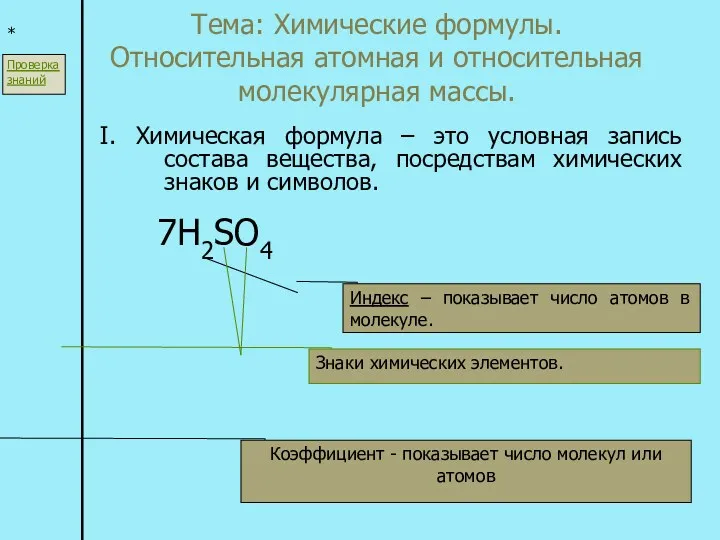 Химические формулы. Относительная атомная и относительная молекулярная массы
Химические формулы. Относительная атомная и относительная молекулярная массы Будова атома: ядро й електронна оболонка. Склад атомних ядер. Протонне та нуклонне число
Будова атома: ядро й електронна оболонка. Склад атомних ядер. Протонне та нуклонне число Получение и приминение этилена
Получение и приминение этилена Конструкционные полимеры: классификация, достижения и проблемы
Конструкционные полимеры: классификация, достижения и проблемы Дисперсные системы
Дисперсные системы Значення хімії у повсякденному житті
Значення хімії у повсякденному житті Получение спиртов. Применение
Получение спиртов. Применение Топливо. Классификация
Топливо. Классификация Лекция 6. Растворы электролитов
Лекция 6. Растворы электролитов Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню
Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню Строение, свойства и применение алкенов
Строение, свойства и применение алкенов Азот – простое вещество. Неметаллы
Азот – простое вещество. Неметаллы Дисперсные системы. Растворы
Дисперсные системы. Растворы Подготовка к ВПР по химии. 11 класс
Подготовка к ВПР по химии. 11 класс Типы расчетных задач, способы их решения. Задания 39-40
Типы расчетных задач, способы их решения. Задания 39-40 Курс хімії за 11 клас
Курс хімії за 11 клас Сера и её соединения
Сера и её соединения Группа веществ, изолируемых из биологического объекта путём минерализации (Металлические яды)
Группа веществ, изолируемых из биологического объекта путём минерализации (Металлические яды) Химические волокна
Химические волокна Сульфаттау және сульфирлеу процестері Сульфохлорлау арқылы алкилсульфонаттарды алу
Сульфаттау және сульфирлеу процестері Сульфохлорлау арқылы алкилсульфонаттарды алу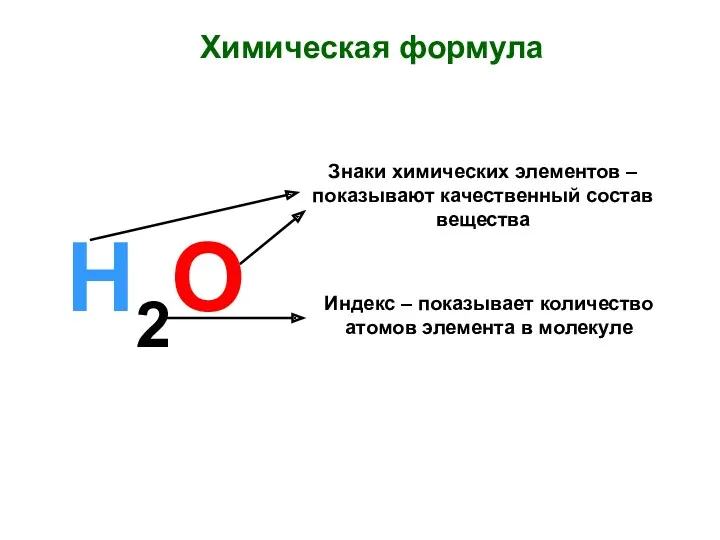 Химическая формула. Знаки химических элементов
Химическая формула. Знаки химических элементов Атом – сложная частица
Атом – сложная частица Основные синтетические полимеры
Основные синтетические полимеры Минерализация, иммобилизация, нитрификация және денитрификация процестері
Минерализация, иммобилизация, нитрификация және денитрификация процестері