Содержание
- 2. ЦЕЛЬ ЗАНЯТИЯ: ИЗУЧИТЬ СТРОЕНИЕ, СВОЙСТВА И ПРИМЕНЕНИЕ АЛКЕНОВ
- 3. 19.11.2022 Строение молекулы CnH2n Химические свойства Изомерия Физические свойства Проверка знаний Получение Номенклатура Применение План занятия:
- 4. 19.11.2022 Алкены – ациклические углеводороды, в молекуле которых кроме одинарных связей содержится одна двойная связь между
- 5. Номенклатура алкенов названия алкенов производят от названий соответствующих алканов (путем замены суффикса –ан на –ен: 2
- 6. Номенклатура алкенов Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение
- 7. Номенклатура алкенов Назовите следующие алкены: CH2=CH2 CH3—CH=CH2 CH3—CH3—CH=CH2 CH3—CH=CH—CH3 CH2=CH—CH=CH2 CH3—CH=CH2 | CH3 19.11.2022
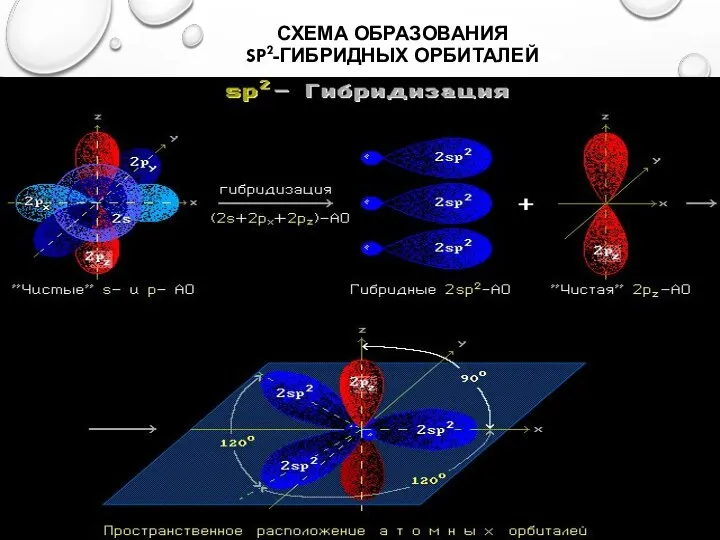
- 8. СХЕМА ОБРАЗОВАНИЯ SP2-ГИБРИДНЫХ ОРБИТАЛЕЙ
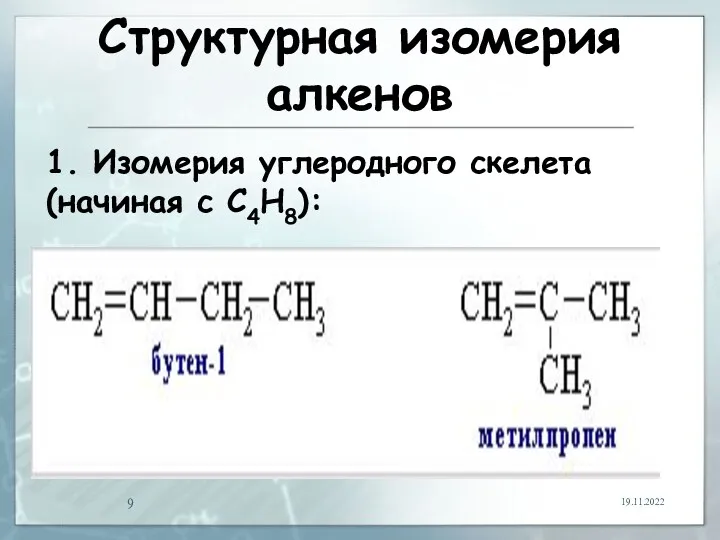
- 9. Структурная изомерия алкенов 19.11.2022 1. Изомерия углеродного скелета (начиная с С4Н8):
- 10. Структурная изомерия алкенов 19.11.2022 2. Изомерия положения двойной связи (начиная с С4Н8) :
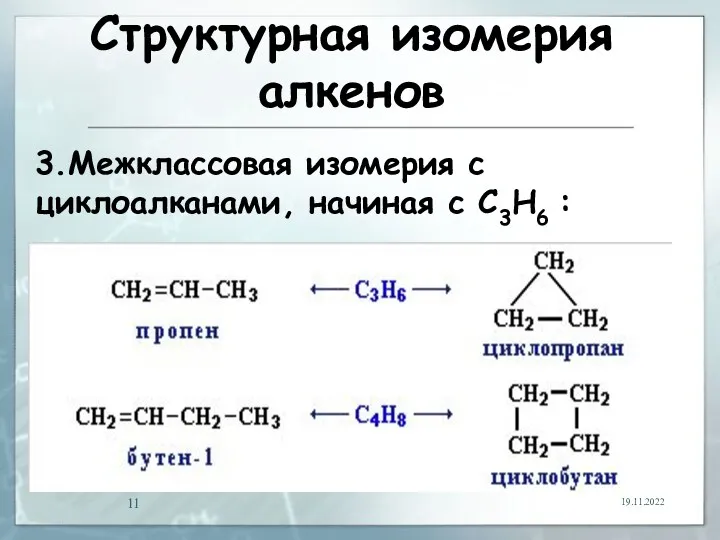
- 11. Структурная изомерия алкенов 19.11.2022 3.Межклассовая изомерия с циклоалканами, начиная с С3Н6 :
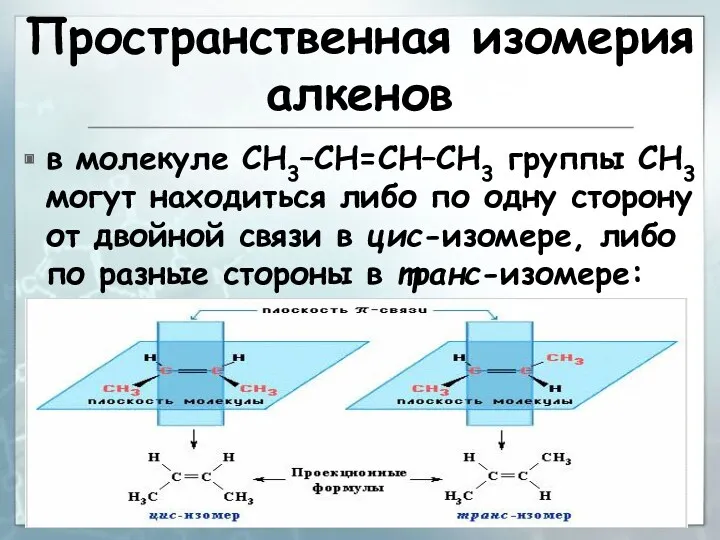
- 12. Пространственная изомерия алкенов в молекуле СН3–СН=СН–СН3 группы СН3 могут находиться либо по одну сторону от двойной
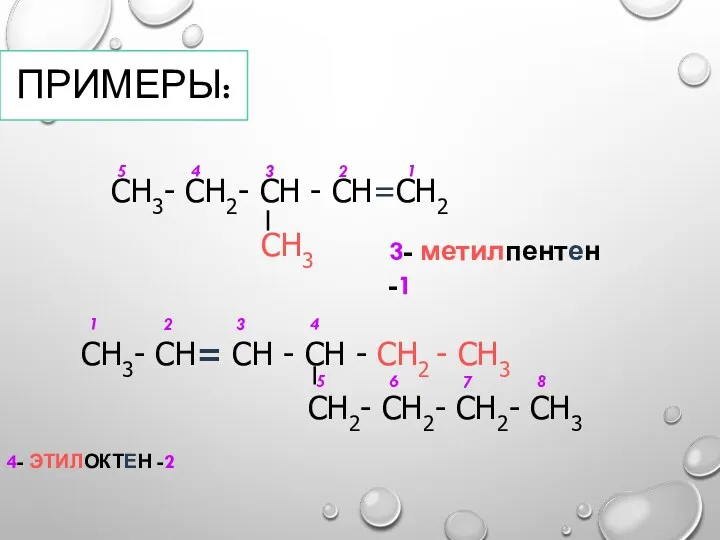
- 13. ПРИМЕРЫ: 4- ЭТИЛОКТЕН -2 СН3- СН2- СН - СН=СН2 СН3 СН3- СН= СН - СН -
- 14. ФИЗИЧЕСКИЕ СВОЙСТВА АЛКЕНОВ АЛКЕНЫ ПЛОХО РАСТВОРИМЫ В ВОДЕ, НО ХОРОШО РАСТВОРЯЮТСЯ В ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЯХ. С УВЕЛИЧЕНИЕМ
- 15. Химические свойства алкенов Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее
- 16. Галогенирование (присоединение галогенов) Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной
- 17. Опыт: обесцвечивание бромной воды этиленом 19.11.2022
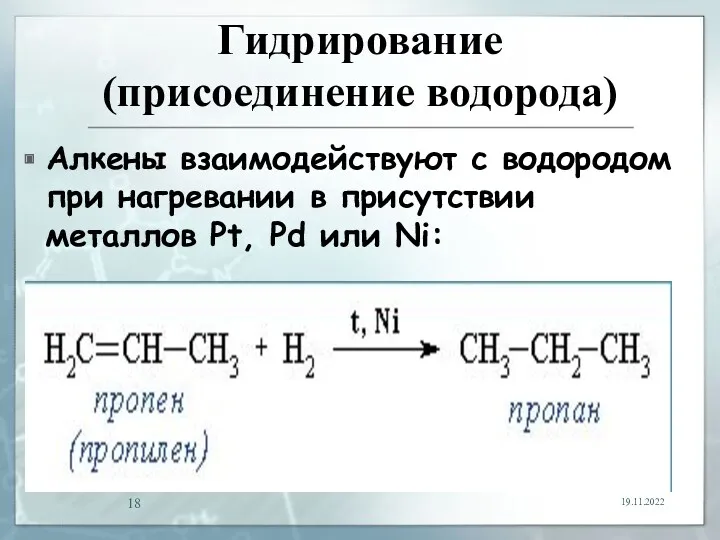
- 18. Гидрирование (присоединение водорода) Алкены взаимодействуют с водородом при нагревании в присутствии металлов Pt, Pd или Ni:
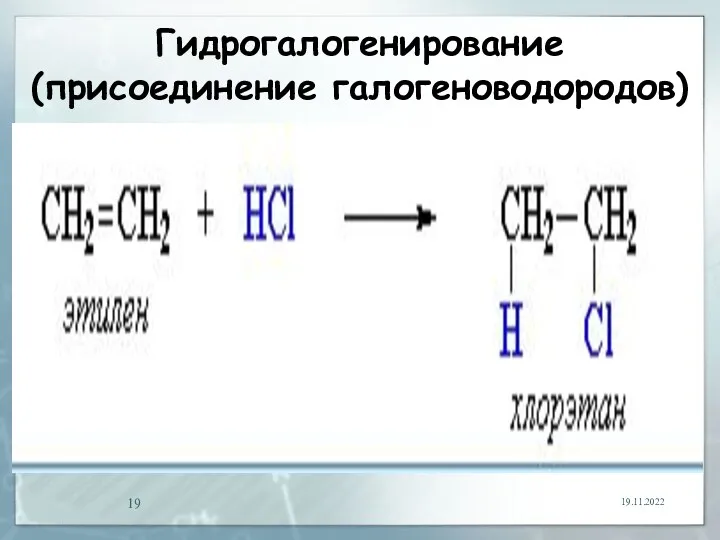
- 19. Гидрогалогенирование (присоединение галогеноводородов) 19.11.2022
- 20. Гидратация (присоединение воды) Гидратация происходит в присутствии минеральных кислот по механизму электрофильного присоединения: 19.11.2022
- 21. Полимеризация алкенов Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера)
- 22. Опыт: горение этилена 19.11.2022
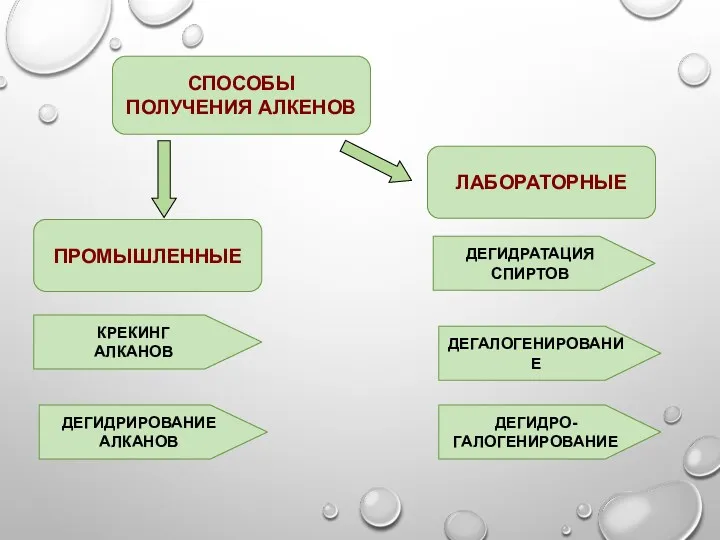
- 23. ПРОМЫШЛЕННЫЕ СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГАЛОГЕНИРОВАНИЕ ДЕГИДРО- ГАЛОГЕНИРОВАНИЕ
- 24. Получение алкенов Крекинг алканов: 19.11.2022
- 25. Получение алкенов II. Отщепление : дегидратация (при температуре менее 150°C в присутствии водоотнимающих реагентов ) 19.11.2022
- 26. Опыт: получение этилена дегидротацией спиртов 19.11.2022
- 27. Получение алкенов II. Отщепление : Дегидрогалогенирование (Дегидрогалогенирование моногалогеналканов при действии спиртового раствора щелочи) 19.11.2022
- 28. Применение алкенов Алкены применяются в качестве исходных продуктов в производстве полимерных материалов (пластмасс, каучуков, пленок) и
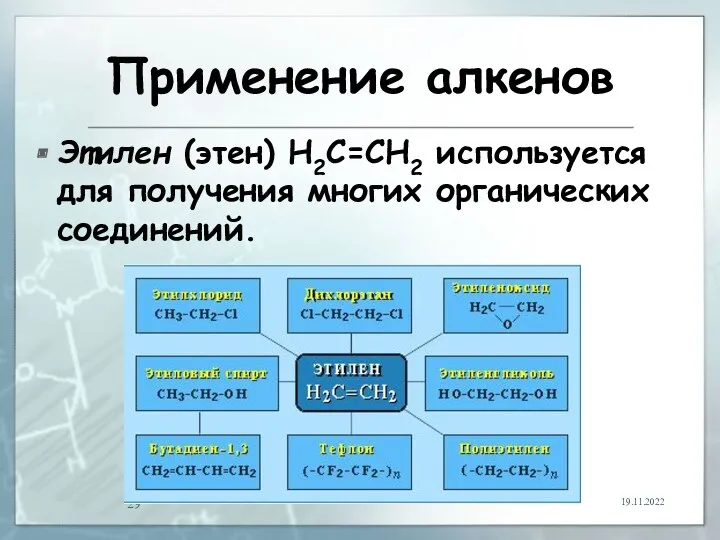
- 29. Применение алкенов Этилен (этен) Н2С=СН2 используется для получения многих органических соединений. 19.11.2022
- 30. Применение алкенов Пропилен (пропен) Н2С=СН2–СН3 и бутилены (бутен-1 и бутен-2) используются для получения спиртов и полимеров.
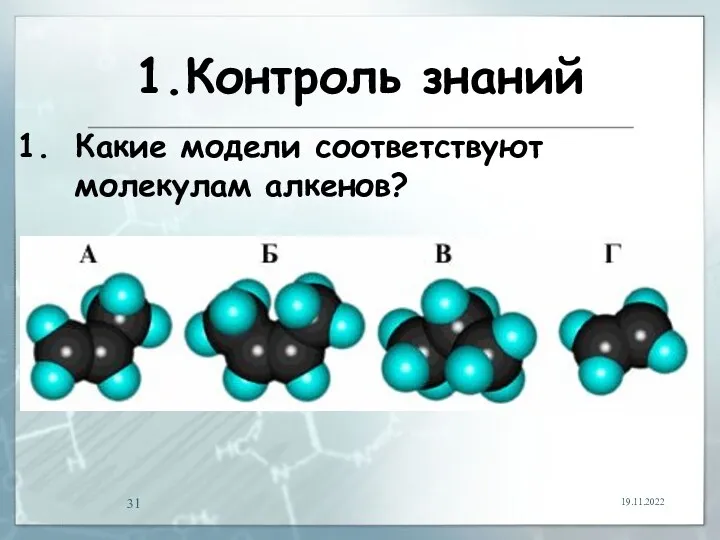
- 31. 1.Контроль знаний 19.11.2022 Какие модели соответствуют молекулам алкенов?
- 32. 2. Контроль знаний 19.11.2022 Дайте названия следующих алкенов, полученных из алканов: - пропан - декан -
- 33. 3. Контроль знаний 19.11.2022 Назовите соединение: Ответ 1: 3-метил-4-этилпентен-2 Ответ 2: 3-метил-2-этилпентен-3 Ответ 3: 3,4-диметилгексен-2 Ответ
- 34. 4. Контроль знаний 19.11.2022 Сколько изомерных алкенов соответствует формуле С4Н8 ? Ответ 1: изомеров нет Ответ
- 35. 5. Контроль знаний 19.11.2022 Двойная связь является сочетанием . . . Ответ 1: двух σ-связей Ответ
- 36. 6. Контроль знаний 19.11.2022 Какова гибридизация атомов углерода в молекуле алкена: Ответ 1: 1 и 4
- 37. 7. Контроль знаний 19.11.2022 Наиболее характерными реакциями алкенов являются: Ответ 1: реакции замещения Ответ 2: реакции
- 39. Скачать презентацию

























 Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Алкани
Алкани Алкени і алкіни
Алкени і алкіни Химический состав клетки
Химический состав клетки Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов Современные тенденции развития химии
Современные тенденции развития химии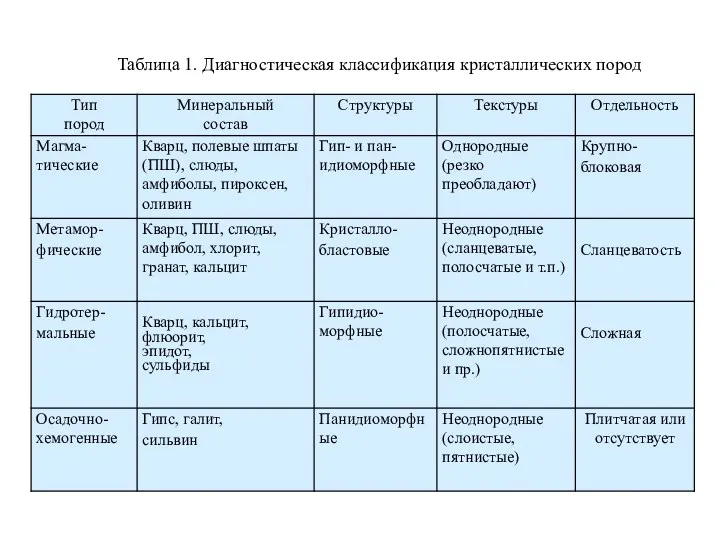 Диагностика метаморфических и гидротермальных горных пород
Диагностика метаморфических и гидротермальных горных пород Химический элемент, минерал, горная порода. (Лекция 6)
Химический элемент, минерал, горная порода. (Лекция 6) Подготовка пробы к анализу. Использование химических и физико-химических методов для идентификации вещества. (Лекция 11)
Подготовка пробы к анализу. Использование химических и физико-химических методов для идентификации вещества. (Лекция 11) Метасоматические горные породы
Метасоматические горные породы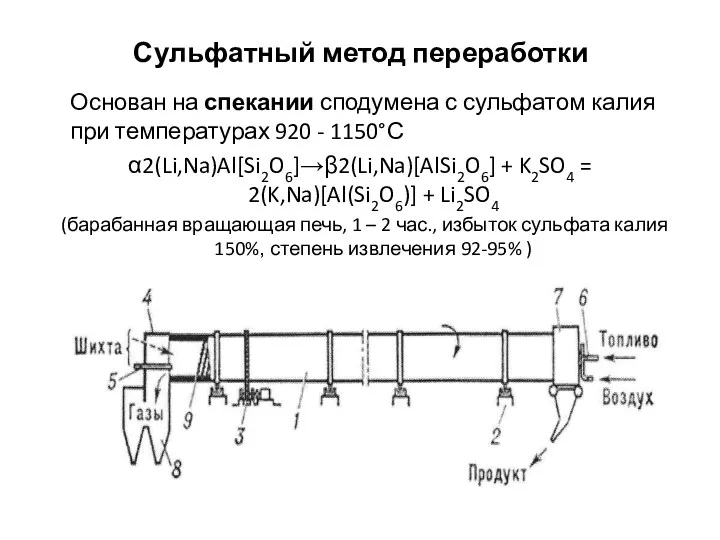 Сульфатный метод переработки
Сульфатный метод переработки Закон триад. Открытие периодического закона
Закон триад. Открытие периодического закона Галогены
Галогены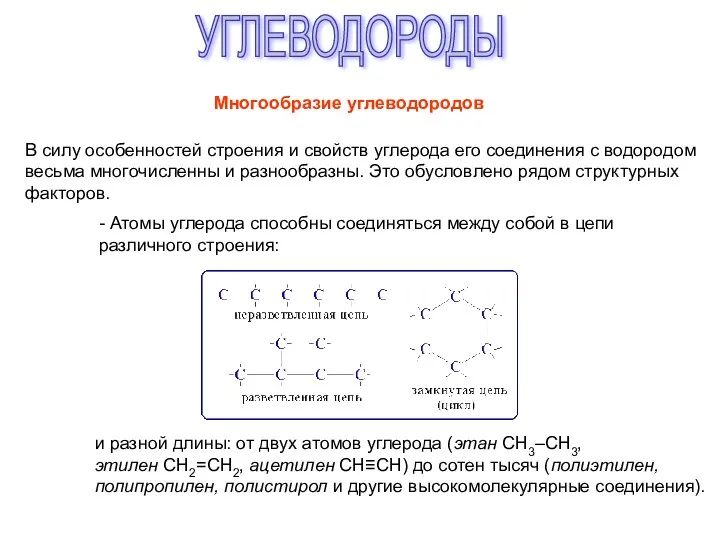 Углеводороды. Многообразие углеводородов
Углеводороды. Многообразие углеводородов Мембранное материаловедение
Мембранное материаловедение Природный и синтетический каучуки. Резина
Природный и синтетический каучуки. Резина Кислородсодержащие соединения серы SO2
Кислородсодержащие соединения серы SO2 Промышленная очистка воды
Промышленная очистка воды Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Щелочные металлы
Щелочные металлы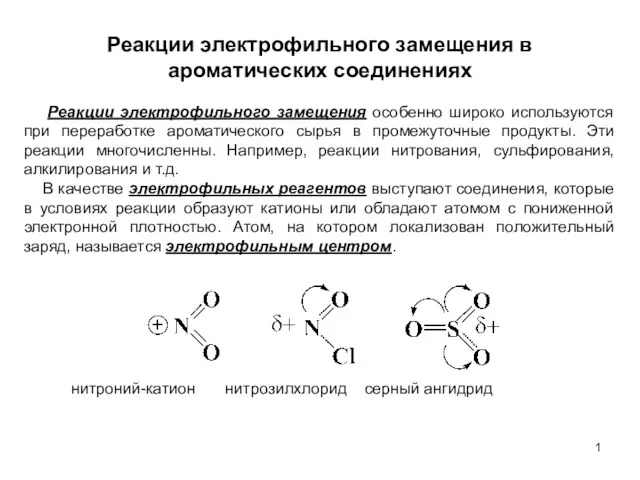 Реакции электрофильного замещения в ароматических соединениях. (Лекция 6)
Реакции электрофильного замещения в ароматических соединениях. (Лекция 6) Алкены. Этилен
Алкены. Этилен Уравнения химических реакций
Уравнения химических реакций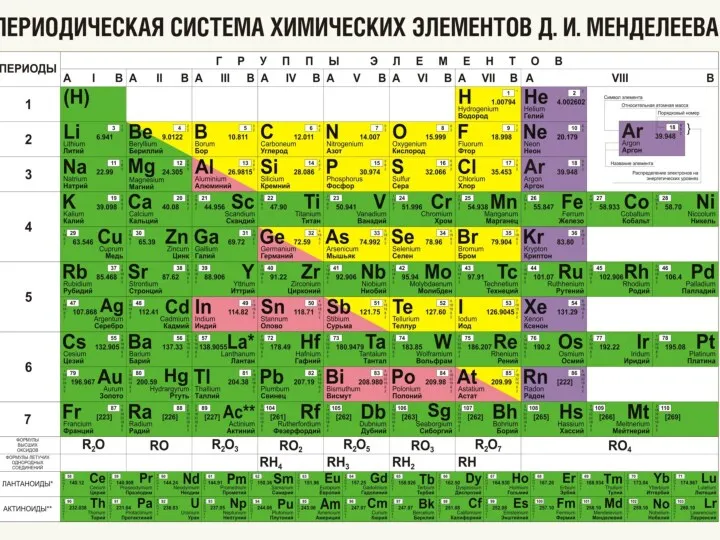 ОВР – окислительно-восстановительные реакции. Тема 4
ОВР – окислительно-восстановительные реакции. Тема 4 Реакции ионного обмена
Реакции ионного обмена Көмірсутектер.Олардың жіктелуі, құрылысы,изомериясы және номенклатурасы
Көмірсутектер.Олардың жіктелуі, құрылысы,изомериясы және номенклатурасы Относительная атомная и относительная молекулярная масса
Относительная атомная и относительная молекулярная масса Происхождение рибосомы, белкового синтеза и генетического кода
Происхождение рибосомы, белкового синтеза и генетического кода