Содержание
- 2. Происхождение названий щелочных металлов Li (1817) лат. " литос" - камень Na (1807) араб. "натрум" -сода
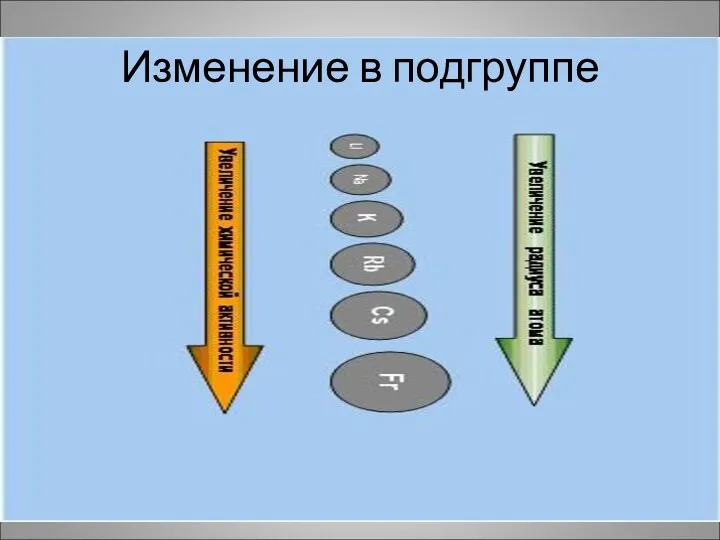
- 3. Положение в периодической системе химических элементов Д.И.Менделеева I группа главная подгруппа. Увеличивается радиус атомов , растет
- 4. Изменение в подгруппе
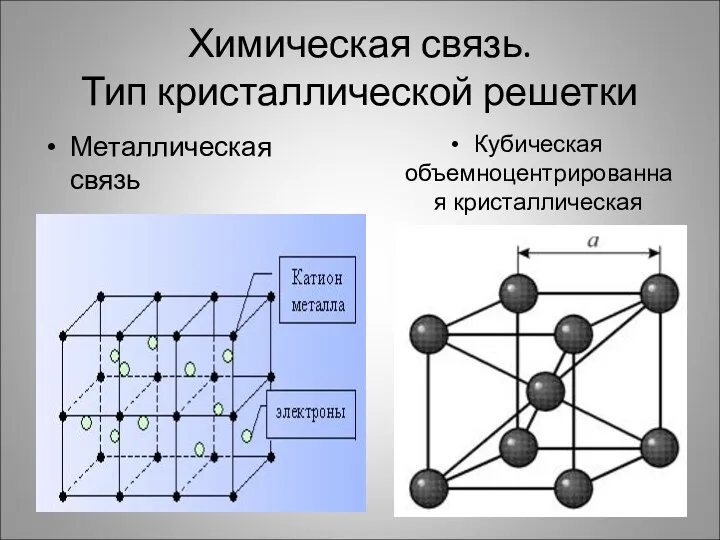
- 6. Химическая связь. Тип кристаллической решетки Металлическая связь Кубическая объемноцентрированная кристаллическая решетка
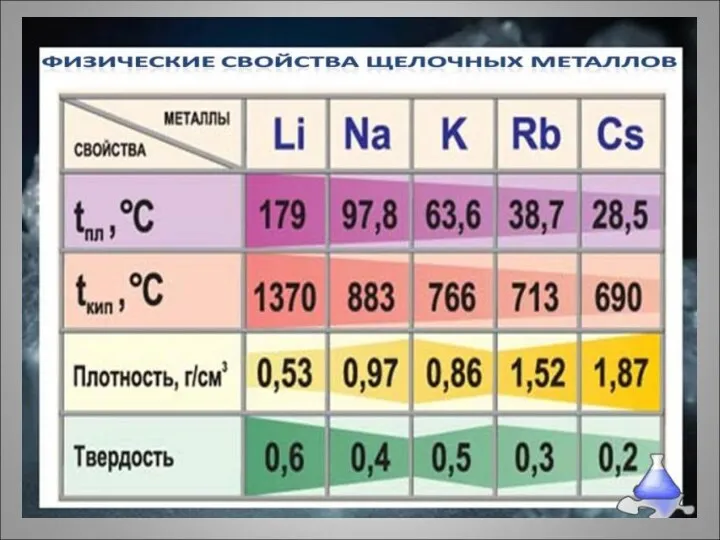
- 9. Щелочные металлы – простые вещества Литий Натрий Литий и натрий - мягкие щелочные металлы серебристо-белого цвета
- 10. Щелочные металлы Калий Рубидий Калий и рубидий мягкие щелочные металлы серебристо-белого цвета
- 11. Щелочные металлы цезий Цезий 99,99999% в ампуле Мягкий щелочной металл золотисто-белого цвета
- 12. Франций Франций - щелочной металл, обладающий как радиоактивностью, так и высокой химической активностью . Не имеет
- 13. Химические свойства щелочных металлов Типичные металлы, очень сильные восстановители. В соединениях проявляют единственную степень окисления +1.
- 14. Химические свойства 2Na + Cl2 = 2NaCl (в атмосфере F2 и Cl2 щелочные Me самовоспламеняются) 4Li
- 15. Качественное определение щелочных металлов Li+ Na+ K+ Для распознавания соединений щелочных металлов по окраске пламени исследуемое
- 16. Получение щелочных металлов 1) Электролиз расплавов соединений щелочных металлов: 2МеCl = 2Ме + Cl2 4МеOH =
- 17. Применение щелочных металлов БИОЛОГИЧЕСКАЯ РОЛЬ И ПРИМЕНЕНИЕ СОЕДИНЕНИЙ КАЛИЯ И НАТРИЯ
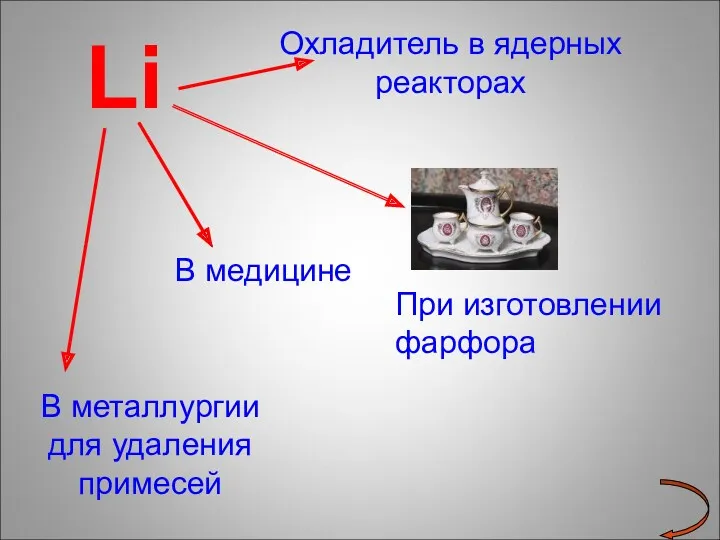
- 18. Li Охладитель в ядерных реакторах В медицине В металлургии для удаления примесей При изготовлении фарфора
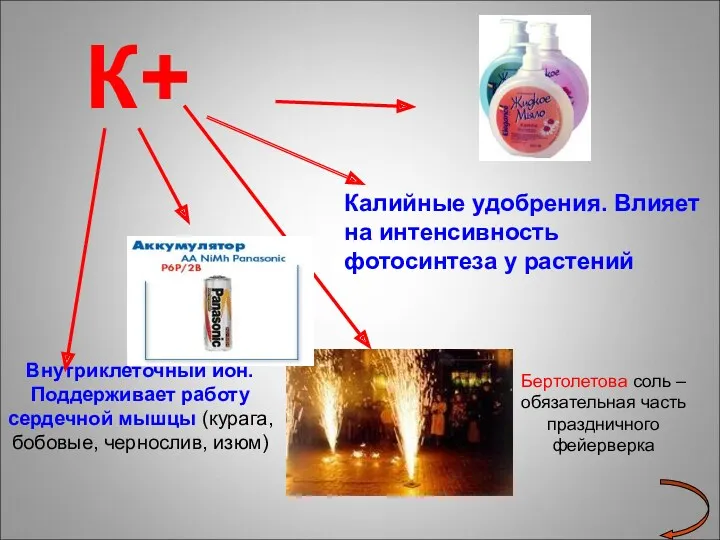
- 19. К+ Внутриклеточный ион. Поддерживает работу сердечной мышцы (курага, бобовые, чернослив, изюм) Калийные удобрения. Влияет на интенсивность
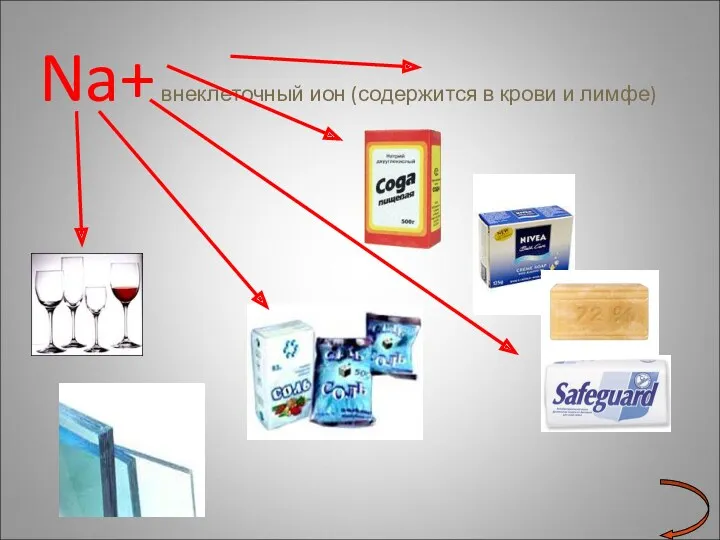
- 20. Na+ внеклеточный ион (содержится в крови и лимфе)
- 21. Сподуменн
- 22. Галит
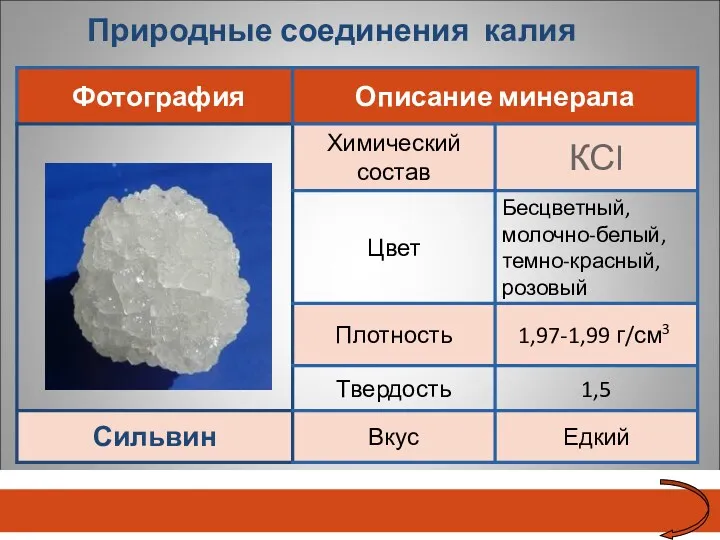
- 23. Природные соединения калия Сильвин
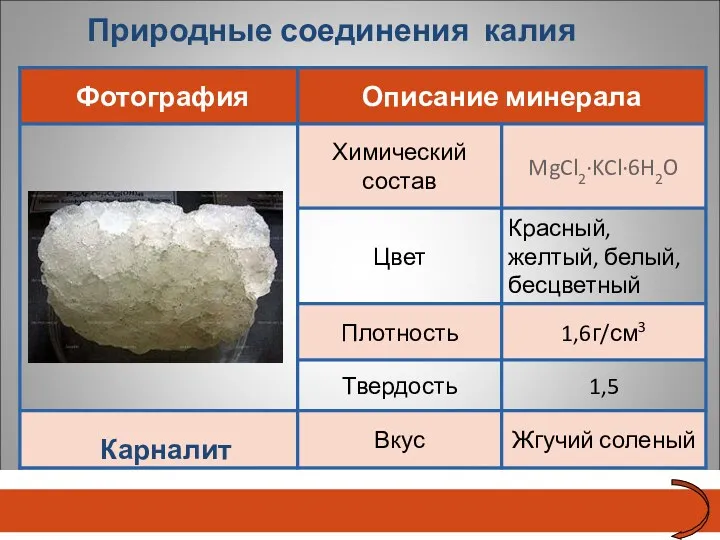
- 24. Природные соединения калия Карналит
- 26. Скачать презентацию















 Карбоновые кислоты
Карбоновые кислоты Сульфиды. Занятие 7
Сульфиды. Занятие 7 Свойства смесей ПАВ
Свойства смесей ПАВ Кислотно-основні рівноваги в біосистемах. Колігативні властивості біологічних рідин
Кислотно-основні рівноваги в біосистемах. Колігативні властивості біологічних рідин Игра по химии В рамках периодической таблицы
Игра по химии В рамках периодической таблицы Классификация химических элементов. Составитель. 8 класс
Классификация химических элементов. Составитель. 8 класс Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Химический состав нефтей. Ненасыщенные углеводороды. Алкены и алкадиены
Химический состав нефтей. Ненасыщенные углеводороды. Алкены и алкадиены Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод
Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод Типичные реакции органических соединений
Типичные реакции органических соединений Типы химических реакций
Типы химических реакций Лужні метали
Лужні метали Галогенопроизводные углеводородов
Галогенопроизводные углеводородов Методы исследования взаимодействий с участием белков (Co-IP, equilibrium microdialysis, ITC, MST, SPR, BLI, QСM)
Методы исследования взаимодействий с участием белков (Co-IP, equilibrium microdialysis, ITC, MST, SPR, BLI, QСM) Магматические формации
Магматические формации Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации Основные понятия химии. Законы стехиометрии
Основные понятия химии. Законы стехиометрии Азотистая кислота
Азотистая кислота Химические волокна
Химические волокна Важнейшие классы бинарных соединений – оксиды и летучие соединения
Важнейшие классы бинарных соединений – оксиды и летучие соединения Получение порошков автоклавным осаждением
Получение порошков автоклавным осаждением Углерод и его соединения
Углерод и его соединения Икаит Ca[CO3]·6 (H2O)
Икаит Ca[CO3]·6 (H2O) Чистые вещества и смеси. Растворы
Чистые вещества и смеси. Растворы Подземное хранение газа и жидкости
Подземное хранение газа и жидкости Карбоновые кислоты и их функциональные производные. Хроматографические методы исследования
Карбоновые кислоты и их функциональные производные. Хроматографические методы исследования Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Геохимия
Геохимия