Содержание
- 2. 1 14.09.2016 Урок 9M класса. Электролитическая диссоциация.
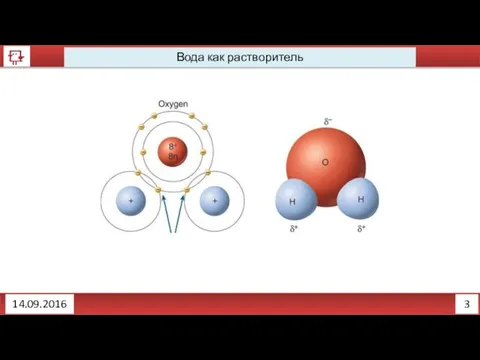
- 3. 2 Вода как растворитель 14.09.2016
- 4. 3 Вода как растворитель 14.09.2016
- 5. 4 Вода как растворитель 14.09.2016 Вещества с какой связь лучше будут растворяться в воде? С ковалентной
- 6. 5 Правило растворимости 14.09.2016 Подобное растворяется в подобном, то есть полярный растворитель подходит к полярному веществу.
- 7. 6 Гидратация 14.09.2016 Гидратация – присоединение воды к ионам, атомам или молекулам. Продукты такого процесса называют
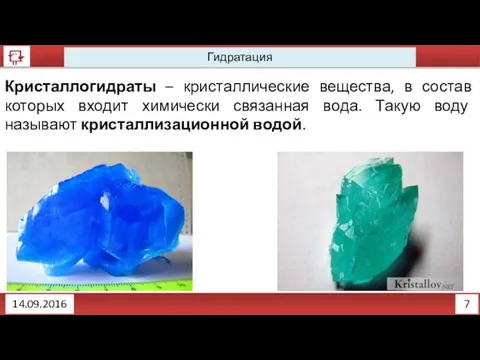
- 8. 7 Гидратация 14.09.2016 Кристаллогидраты – кристаллические вещества, в состав которых входит химически связанная вода. Такую воду
- 9. 1 15.09.2016 Урок 9M класса. Электролитическая диссоциация.
- 10. 2 Основные положения электролитической диссоциации 15.09.2016 Основные положения теории электролитической диссоциации: Электролиты при растворении или плавлении
- 11. 3 Диссоциация разных веществ 15.09.2016 Диссоциировать могут соли, кислоты, щелочки. Наиболее хорошо диссоцируют вещества с ионной
- 12. 4 Диссоциация кислот 15.09.2016 Кислоты – такие вещества, при диссоциации в водных растворах которых в качестве
- 13. 5 Диссоциация кислот 15.09.2016 H2SO4 HSO4- + H+ HSO4- SO42- + H+ H3PO4 H+ +H2PO4- H2PO4-
- 14. 6 Диссоциация щелочей 15.09.2016 Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы
- 15. 7 Диссоциация солей 15.09.2016 Соли – сложные вещества, которые в водных растворах диссоциируют на катионы металлов
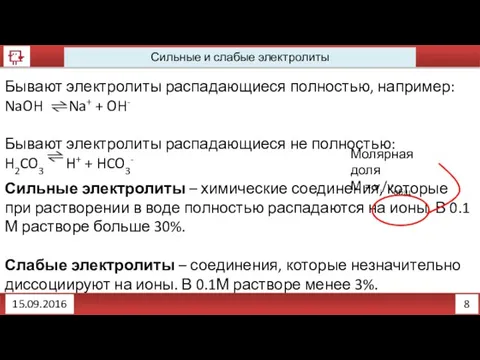
- 16. 8 Сильные и слабые электролиты 15.09.2016 Бывают электролиты распадающиеся полностью, например: NaOH Na+ + OH- Бывают
- 17. 8 Сильные и слабые электролиты 15.09.2016 Бывают электролиты распадающиеся полностью, например: NaOH Na+ + OH- Бывают
- 18. 9 Степень диссоциации 15.09.2016 Различить слабые электролиты и сильные электролиты помогает показатель степень диссоциации (α). Степень
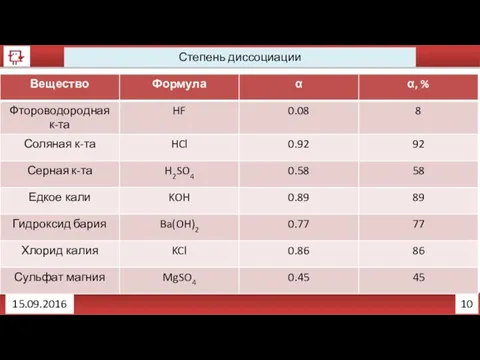
- 19. 10 Степень диссоциации 15.09.2016
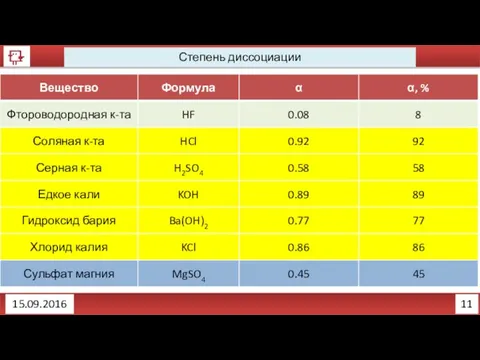
- 20. 11 Степень диссоциации 15.09.2016
- 21. 12 Степень диссоциации 15.09.2016 Нужно отметить, что при диссоциации электролита происходит увеличение количества частиц в растворе.
- 22. 13 Степень диссоциации 15.09.2016 Давайте считать! Взяли 154 г. Ba(OH)2, потом растворили в воде. Сколько частиц
- 24. Скачать презентацию














 Углерод. Аллотропные модификации углерода
Углерод. Аллотропные модификации углерода Поделочные камни
Поделочные камни Удобрения и их классификация
Удобрения и их классификация Единство химической организации живых организмов
Единство химической организации живых организмов Токсикология пестицидов
Токсикология пестицидов Растворы: состав и их коллигативные свойства
Растворы: состав и их коллигативные свойства Азотсодержащие соединения
Азотсодержащие соединения Занимательная химия. Химический элемент. 8 класс
Занимательная химия. Химический элемент. 8 класс Алкены. Этилен
Алкены. Этилен Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Потенциометрия
Потенциометрия Подгруппа меди. Элементы 11 группы (Cu,Ag,Au)
Подгруппа меди. Элементы 11 группы (Cu,Ag,Au) Карбонові кислоти
Карбонові кислоти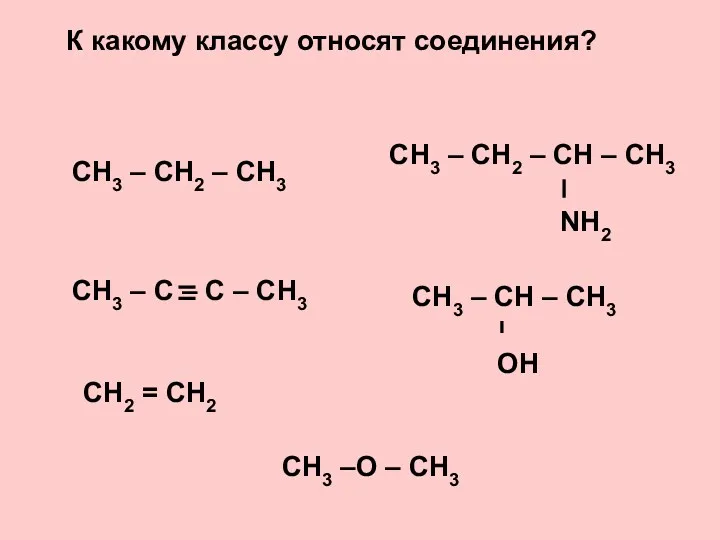 16_OP_05_Alkany
16_OP_05_Alkany Строение атома
Строение атома Сложноэфирная конденсация Кляйзена-Шмидта
Сложноэфирная конденсация Кляйзена-Шмидта Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Химические свойства металлов
Химические свойства металлов Пурины. Строение пурина
Пурины. Строение пурина Гидролиз. Классификация солей
Гидролиз. Классификация солей Свойства минералов
Свойства минералов Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Подготовка к ГИА. В1. Периодический закон Д.И. Менделеева
Подготовка к ГИА. В1. Периодический закон Д.И. Менделеева Ионное произведение воды. Водородный показатель воды
Ионное произведение воды. Водородный показатель воды Периодический закон и строение атома
Периодический закон и строение атома Предмет и история геохимии
Предмет и история геохимии Загадочный Менделеев
Загадочный Менделеев Простые и сложные вещества
Простые и сложные вещества