Слайд 2

Особенности реакции
В качестве катализаторов используют алкоголяты спиртов. Металлический натрий используют в
качестве катализатора, так как сложные эфиры, полученные реакцией этерификации, содержат небольшое количество спирта. Если спиртов в сложных эфирах нет, то под действием металлического натрия происходит ацилоиновая конденсация.
В качестве катализаторов могут выступать амиды натрия и калия, трифенилметилнатрий и т.д.
Слайд 3

Механизм реакции
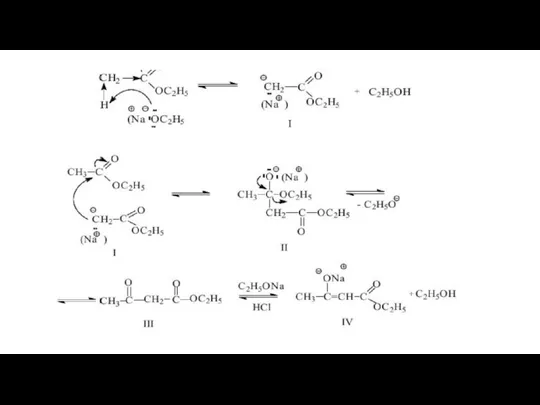
Образующийся карбанион I,я вляющийся сильным нуклеофилом, атакует электрофильный атом углерода
карбонильной группы второй молекулы этилацетата с образованием интермедиата II. При отщеплении этоксидного аниона образуется этиловый эфир 3-оскобутановой кислоты или ацетоуксусный эфир (III), который в присутствии этоксида натрия отщепляет атом водорода метиленовой группы и образуется анион. При подкислении смеси образуется ацетоуксусный эфир (III).
Слайд 4
Слайд 5

В анионе натрийацетоуксусного эфира отрицательный заряд не локализован ни на атоме
углерода или кислорода, а делокализован, рассредоточен по системе связей O-C-C-C-O.
Аналогичные сложноэфирные конденсации протекают между сложными эфирами, имеющими в α-положении в карбонильной группе подвижные атомы водорода.
Возможны перекрёстные конденсации, протекающие между двумя различными сложными эфирами. Может образоваться 4 продукта. По этому выгоднее использовать конденсацию Кляйзена только тогда, когда сложный эфир не имеет подвижного атома водорода.
Слайд 6

Синтезы на основе ацетоуксусного эфира
Используются для синтеза различных органических соединений- кетонов
и карбоновых кислот.
Одним из таких превращений является способность ацетоуксусного эфира подвергаться кетонному расщеплению под действием разбавленных щелочей и оснований. Гидролизуется сложноэфирная группа и образуется неустойчивая ацетоуксусная кислота. При нагревании она декарбоксилируется с образованием ацетона.
Слайд 7

При воздействии на ацетоуксусный эфир конецентрированой щёлочи происходит его кислотное расщепление
Слайд 8

Гидроксид-анион атакует атом углерода карбонильной группы ацетоуксусного эфира с образованием интермедиата,
из которого в результате отщепления C2-C3 связи образуется две молекулы натриевой соли уксусной кислоты.
Для препаративных синтезеов используют алькильные и ацильные производные ацетоуксусного эфира.







 Типичные окислители
Типичные окислители Количество вещества. 8 класс
Количество вещества. 8 класс Химическая связь. Взаимное влияние атомов в молекуле
Химическая связь. Взаимное влияние атомов в молекуле Основания. Классификация оснований
Основания. Классификация оснований Водородный показатель
Водородный показатель Химические свойства металлов. Взаимодействие с простыми веществами
Химические свойства металлов. Взаимодействие с простыми веществами Молярный объем газов. 8 класс
Молярный объем газов. 8 класс Использование технологии уровневой дифференциации на уроках химии
Использование технологии уровневой дифференциации на уроках химии Кристаллические решётки и их виды
Кристаллические решётки и их виды Алкалоиды, производные тропана
Алкалоиды, производные тропана Термохимия. Термохимические уравнения
Термохимия. Термохимические уравнения Общие представления о фазовых состояниях и фазовых переходах полимеров
Общие представления о фазовых состояниях и фазовых переходах полимеров фосфор и его соединения
фосфор и его соединения Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Закон триад. Открытие периодического закона
Закон триад. Открытие периодического закона Жидкое и растворимое стекло
Жидкое и растворимое стекло Основы химической термодинамики и кинетики химических реакций
Основы химической термодинамики и кинетики химических реакций O-alkylation catalysts
O-alkylation catalysts Электролитическая диссоциация
Электролитическая диссоциация Мінеральні добрива та їх класифікація
Мінеральні добрива та їх класифікація Псевдоморфозы. Образование псевдоморфоз
Псевдоморфозы. Образование псевдоморфоз Құрамында белгілі қоспасы бар басқа заттың массасын (көлемін) реакция теңдеуі бойынша есептеу
Құрамында белгілі қоспасы бар басқа заттың массасын (көлемін) реакция теңдеуі бойынша есептеу Топырақ биоремедиациясы
Топырақ биоремедиациясы Равновесие в растворах электролитов
Равновесие в растворах электролитов Галогены. Свойства галогенов
Галогены. Свойства галогенов Ртуть
Ртуть Циклоалканы. 10 класс
Циклоалканы. 10 класс Фенолы. Классификация и номенклатура фенолов
Фенолы. Классификация и номенклатура фенолов