Содержание
- 2. Лекция № 1 Основы химической термодинамики и кинетики химических реакций
- 3. Понятие о химической термодинамике Термодинамика – наука, изучающая взаимные превращения различных видов энергии Химическая термодинамика –
- 4. Биоэнергетика изучает превращение энергии в биосистемах Энергия окисления пищевых продуктов, идет на поддержание температуры тела и
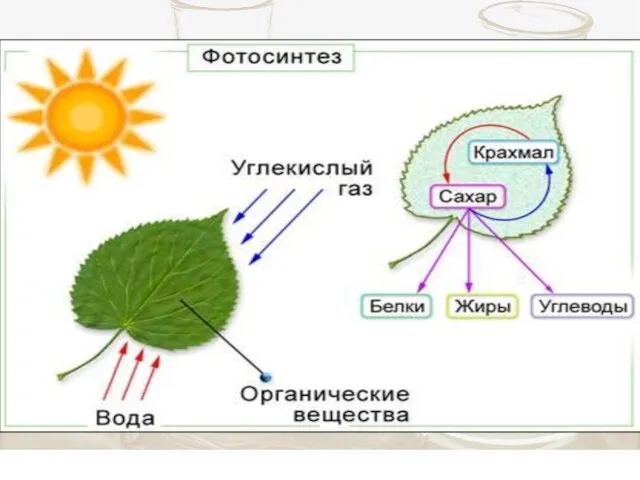
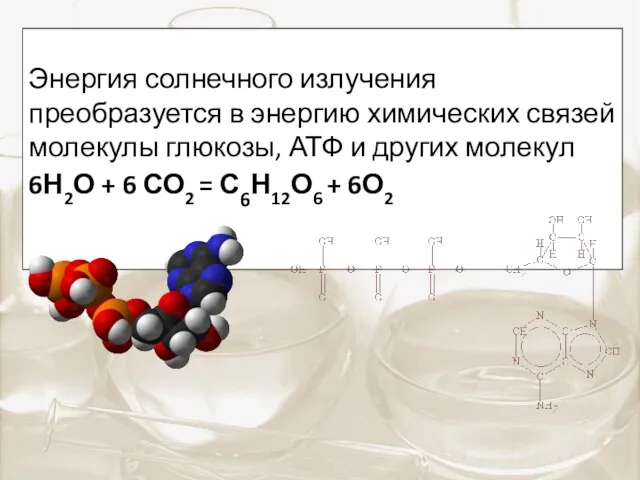
- 6. Энергия солнечного излучения преобразуется в энергию химических связей молекулы глюкозы, АТФ и других молекул 6Н2О +
- 7. 40 ккал Еда, 30 мин 30 ккал Ходьба, 10 мин 110 ккал Работа, 1 час 70
- 8. Задача Потребность в энергии у студентов составляет 11732 кДж в сутки. Можно ли рекомендовать студенту следующий
- 9. Термодинамическая система это тело или группа тел, отделенные от окружающей среды реальной или воображаемой поверхностью раздела.
- 10. Термодинамические параметры общие Функции состояния основные давление (Р) температура (Т) объем (V) измеряемые Измеряются абсолютные значения
- 11. Первый закон термодинамики Подведенное к системе тепло идет на увеличение внутренней энергии системы и на совершение
- 12. Внутренняя энергия Е – сумма всех видов энергии частиц, составляющих систему. Энтальпия Н – теплосодержание системы.
- 13. Основной закон термохимии – закон Гесса. Тепловой эффект реакции не зависит от пути протекания реакции, а
- 14. Энтропия S – мера хаотичности, беспорядка Второй закон термодинамики: В изолированных системах энтропия самопроизвольно протекающего процесса
- 15. Энергия Гиббса G Изобарно-изотермический потенциал – максимальная полезная работа, совершаемая системой при постоянных давлении и температуре.
- 16. Критерии самопроизвольности процесса ∆Н ∆S> 0 – энтропийный фактор ∆G ∆G= 0 – термодинамическое равновесие
- 17. Термодинамическое равновесное состояние – постоянство свойств системы во времени, потоки вещества и энергии отсутствуют. Стационарное состояние
- 18. Факторы, определяющие ход процесса
- 19. Сопряженные реакции Глюкоза+Фруктоза=Сахароза+Н2О +20,9кДж/моль, Эндергонический процесс ∆G > 0 ведомая реакция АTФ + Н2О = AДФ
- 20. Кинетика – учение о скоростях и механизмах химических реакций.
- 21. Скорость реакции число элементарных актов реакции, происходящих в единицу времени в единице объема (в случае гомогенной
- 22. Обратимые реакции протекают одновременно в прямую и обратную стороны Необратимые реакции - протекают в одну сторону
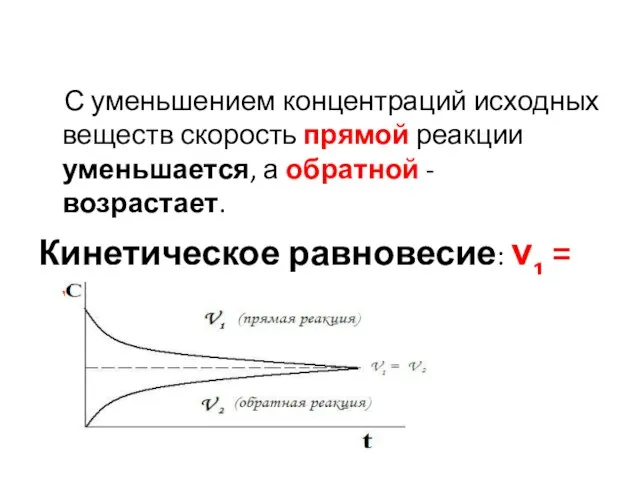
- 23. С уменьшением концентраций исходных веществ скорость прямой реакции уменьшается, а обратной - возрастает. Кинетическое равновесие: ν1
- 24. Скорость химической реакции зависит от - природы реагирующих веществ; - концентрации; - температуры; - давления (для
- 25. Влияние концентрации Закон Гульдберга и Вааге (1867) mA+nB=dD , где: k – константа скорости реакции; –
- 26. для гетерогенной реакции Горение угля С + О2 = СО2 ν = k[O2] Константа скорости реакции
- 27. Влияние давления Р СН 2, СI2 ν1
- 28. Влияние температуры. С увеличением Т скорость любой реакции возрастает Правило Вант – Гоффа При повышении температуры
- 29. Влияние катализатора Катализаторы - вещества, влияющие на скорость протекания термодинамически возможных химических реакций, но остающиеся неизменными
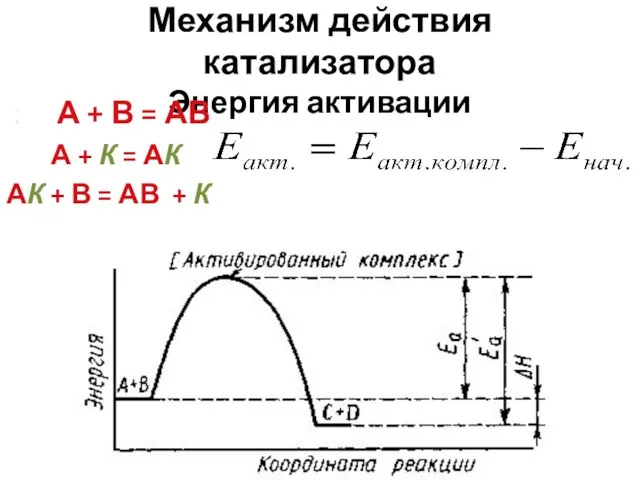
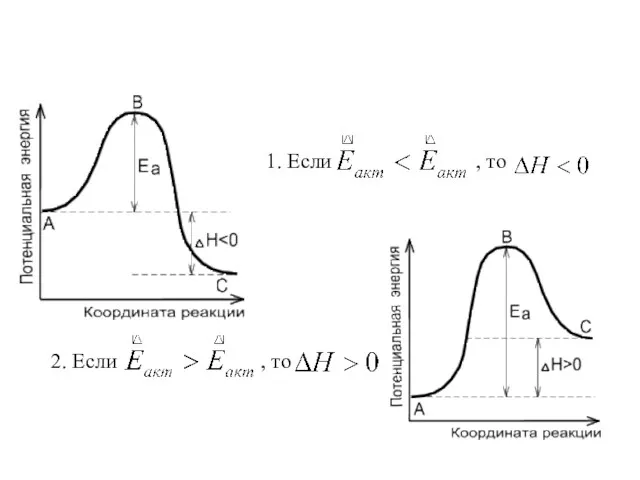
- 30. Механизм действия катализатора Энергия активации : А + В = АВ А + К = АК
- 31. 1. Если , то 2. Если , то
- 32. Механизм действия катализатора Энергия активации Еакт ν1 ν2 К1 К2 Катализатор в равной степени изменяет скорости
- 33. Биокатализаторы
- 34. Особенности ферментов как биокатализаторов Высокая эффективность действия; Избирательность (селективность); Высокая чувствительность к условиям среды (t, pH
- 36. Кинетические параметры: ν, k, Кравн. Константа скорости реакции (k) зависит от: природы реагирующих веществ; температуры; катализатора
- 37. Уравнение Аррениуса. где: k – константа скорости реакции; R – универсальная газовая постоянная (8,31 Дж/моль.К); Т
- 38. Константа равновесия В условиях равновесия для любого обратимого гомогенного процесса mA + nB pC + qD
- 39. природа реагирующих веществ; температура; Кравн. k - катализатор; концентрация; - давление (для газов); V
- 40. Принцип Ле - Шателье Равновесие в системе всегда смещается в сторону того процесса, протекание которого уменьшает
- 41. Термодинамика химического равновесия связь Кравн. со свободной энергией Гиббса: самопроизвольный процесс термодинамическое равновесие реакция не протекает
- 43. Скачать презентацию



































 Сапалық талдау. Сапалық аналитикалық реакциялар
Сапалық талдау. Сапалық аналитикалық реакциялар Классификация сталей
Классификация сталей Характеристика спиртов
Характеристика спиртов Псевдоморфозы. Образование псевдоморфоз
Псевдоморфозы. Образование псевдоморфоз Кислородсодержащие соединения. Тема 1: спирты
Кислородсодержащие соединения. Тема 1: спирты Устойчивость дисперсных систем
Устойчивость дисперсных систем Способы и степень дробления
Способы и степень дробления Бензол қатарындағы гетерофункционалды туындылары дәрі-дәрмек ретінде
Бензол қатарындағы гетерофункционалды туындылары дәрі-дәрмек ретінде Химический элемент таблицы Менделеева - Азот
Химический элемент таблицы Менделеева - Азот Электродные потенциалы
Электродные потенциалы Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Ароматические кислоты и их соли
Ароматические кислоты и их соли Кислород/водород. Повторение
Кислород/водород. Повторение Химические свойства металлов
Химические свойства металлов Методы осаждения. Аналитическая химия
Методы осаждения. Аналитическая химия Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Металлы в живой приподе
Металлы в живой приподе Неоднородные системы (процессы и аппараты химической технологии, 8 лекция)
Неоднородные системы (процессы и аппараты химической технологии, 8 лекция) Металлы в природе. Получение
Металлы в природе. Получение Хімія елементів VIIВ групи (Mn, Tc, Re)
Хімія елементів VIIВ групи (Mn, Tc, Re) Тяжелые металлы
Тяжелые металлы Степени окисления атомов и формулы веществ
Степени окисления атомов и формулы веществ Поликонденсация. Фенолформальдегидные смолы
Поликонденсация. Фенолформальдегидные смолы Алкоголь
Алкоголь Хром и его соединения
Хром и его соединения Количественный анализ. Гравиметрия
Количественный анализ. Гравиметрия Основания. Классификация оснований
Основания. Классификация оснований Характер химического элемента по кислотно- основным свойствам. (Амфотерные соединения)
Характер химического элемента по кислотно- основным свойствам. (Амфотерные соединения)