Содержание
- 2. Вспомните, какие вещества мы называем углеводородами? УГЛЕВОДОРОДЫ –это органические соединения, состоящие из двух химических элементов –
- 3. АЛКАНЫ Строение, номенклатура, изомерия и физические свойства.
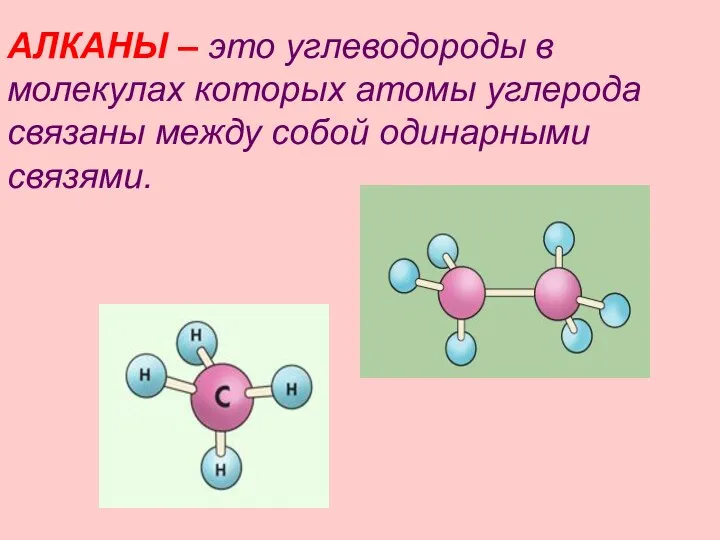
- 4. АЛКАНЫ – это углеводороды в молекулах которых атомы углерода связаны между собой одинарными связями.
- 5. Все алканы отвечают общей формуле СnН2n+2 где n=1, 2, 3…+∞
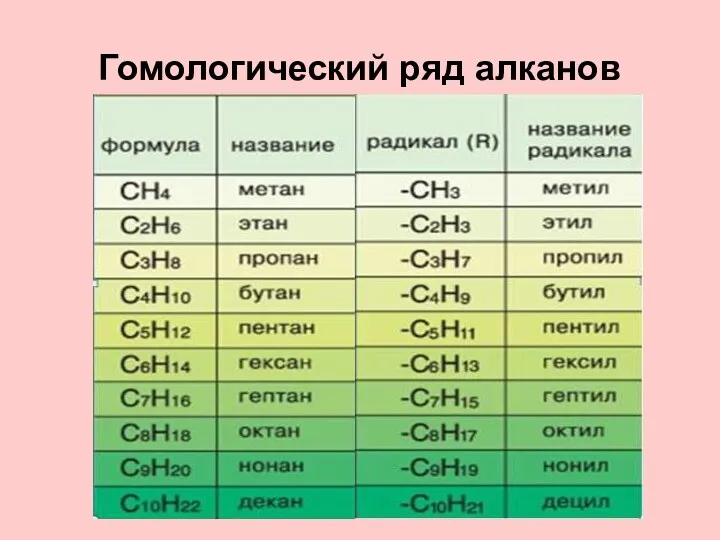
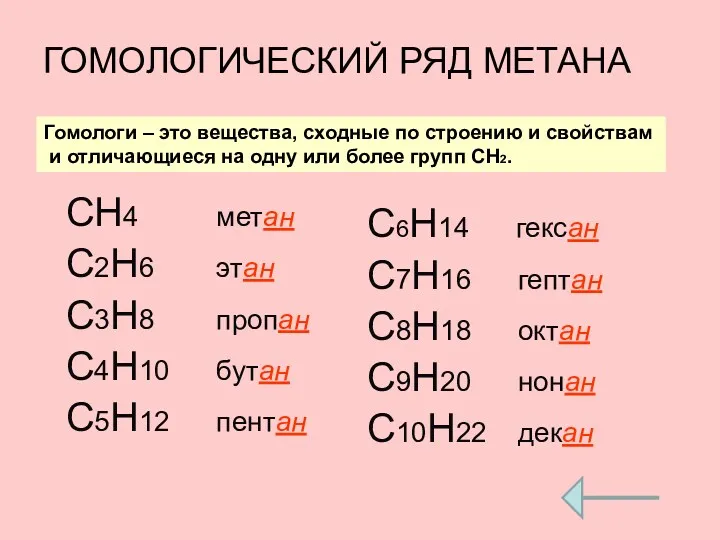
- 6. Гомологический ряд алканов
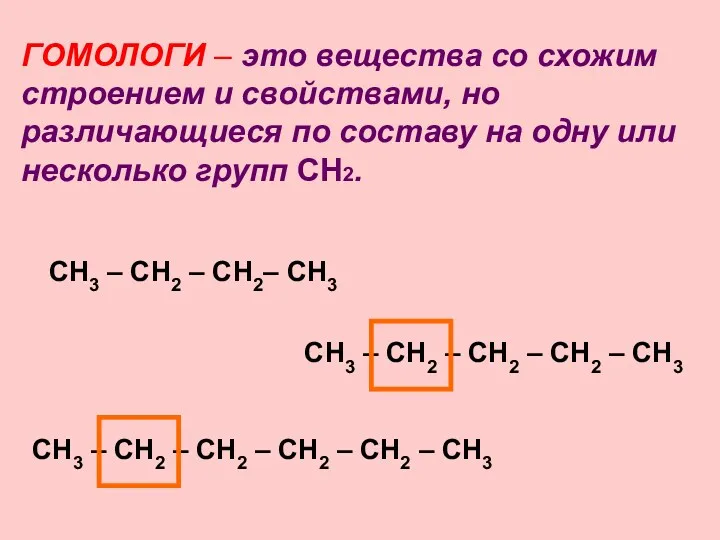
- 7. ГОМОЛОГИ – это вещества со схожим строением и свойствами, но различающиеся по составу на одну или
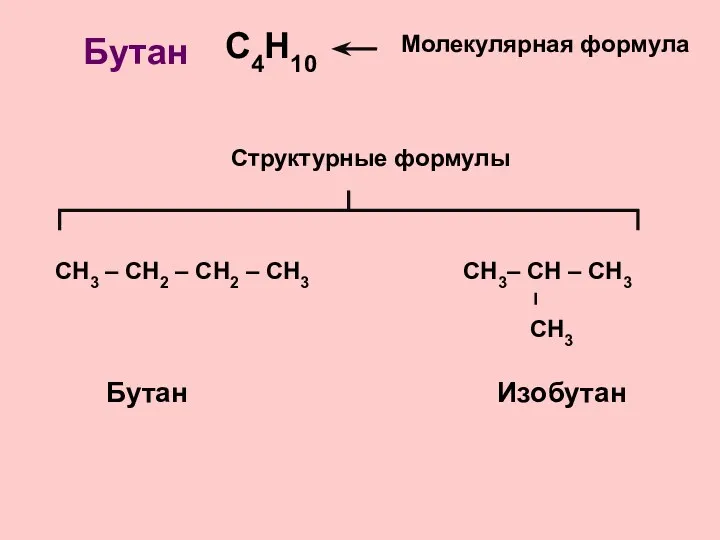
- 8. С4Н10 СН3 – СН2 – СН2 – СН3 Молекулярная формула Структурные формулы Бутан Бутан Изобутан
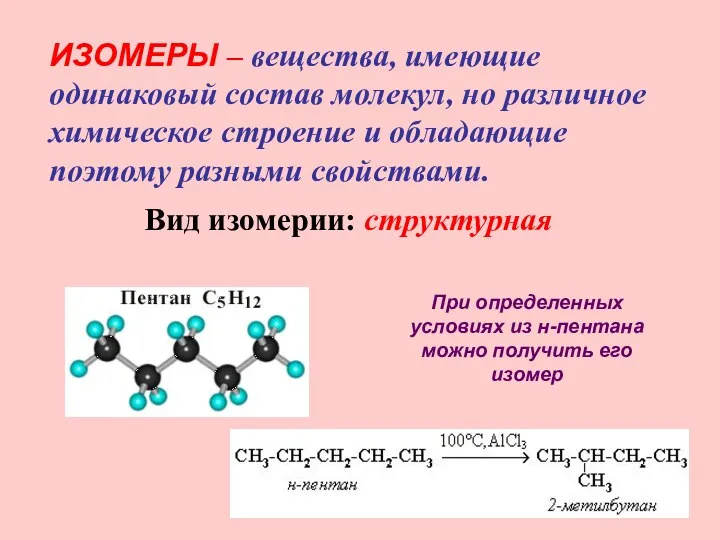
- 9. ИЗОМЕРЫ – вещества, имеющие одинаковый состав молекул, но различное химическое строение и обладающие поэтому разными свойствами.
- 10. ГОМОЛОГИЧЕСКИЙ РЯД МЕТАНА СН4 метан С2H6 этан C3H8 пропан C4H10 бутан C5H12 пентан C6H14 гексан C7H16
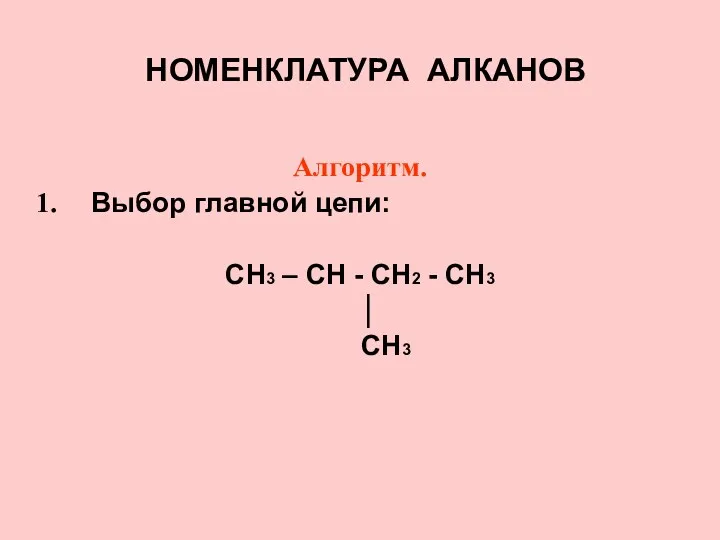
- 11. НОМЕНКЛАТУРА АЛКАНОВ Алгоритм. Выбор главной цепи: CH3 – CH - CH2 - CH3 │ CH3
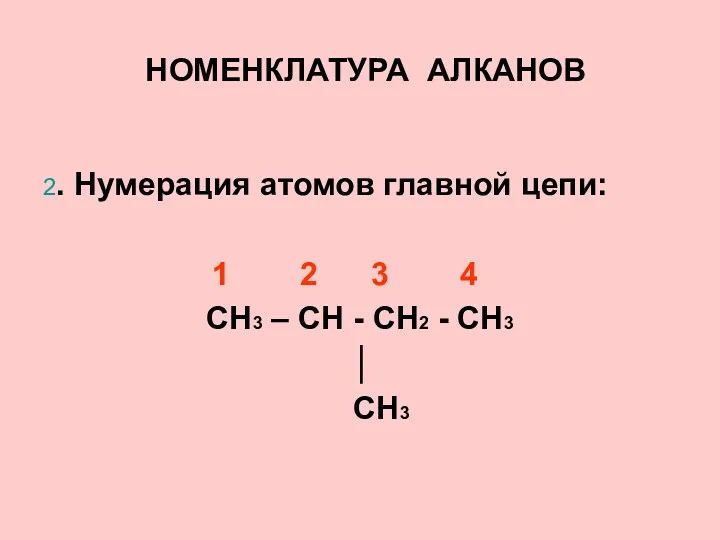
- 12. НОМЕНКЛАТУРА АЛКАНОВ 2. Нумерация атомов главной цепи: 1 2 3 4 CH3 – CH - CH2
- 13. НОМЕНКЛАТУРА АЛКАНОВ 3. Формирование названия: 1 2 3 4 CH3 – CH - CH2 - CH3
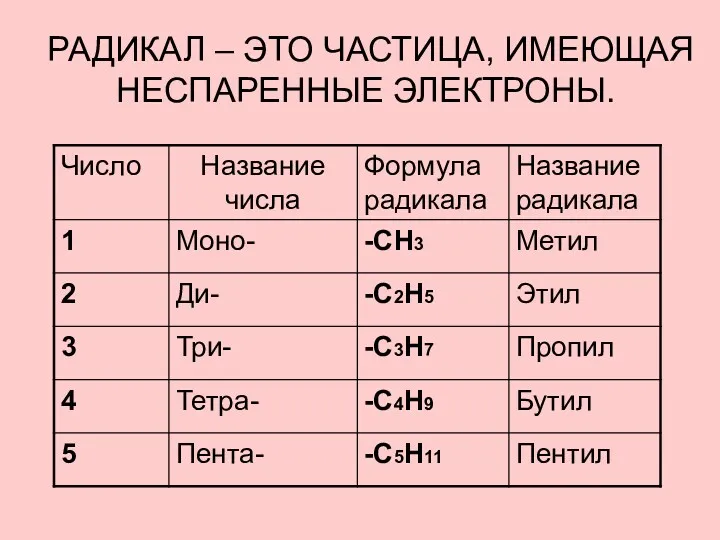
- 14. РАДИКАЛ – ЭТО ЧАСТИЦА, ИМЕЮЩАЯ НЕСПАРЕННЫЕ ЭЛЕКТРОНЫ.
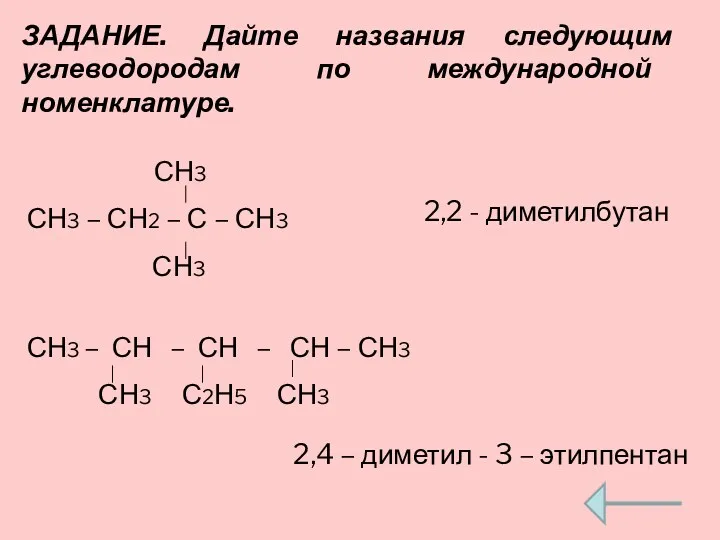
- 15. ЗАДАНИЕ. Дайте названия следующим углеводородам по международной номенклатуре. СН3 СН3 – СН2 – С – СН3
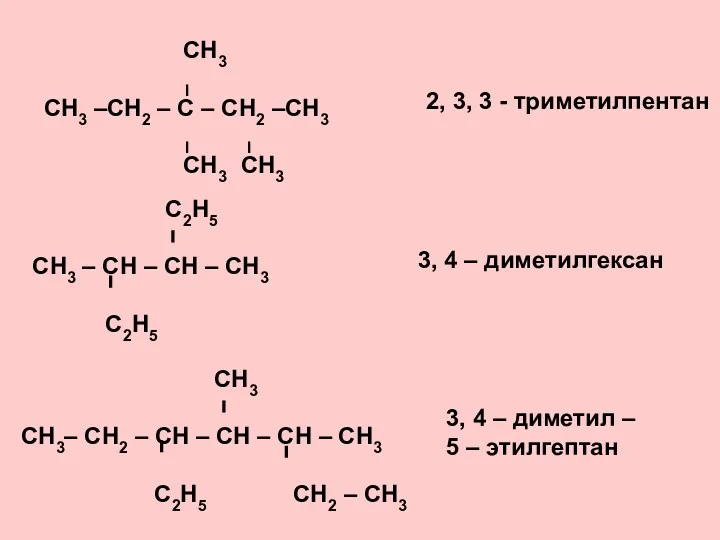
- 16. СН3 І СН3 –СН2 – С – СН2 –СН3 І І СН3 СН3 2, 3, 3
- 17. Составте структурные формулы следующих веществ и укажите первичные, вторичные и третичные атомы. А) 2,3 – диметилпентан
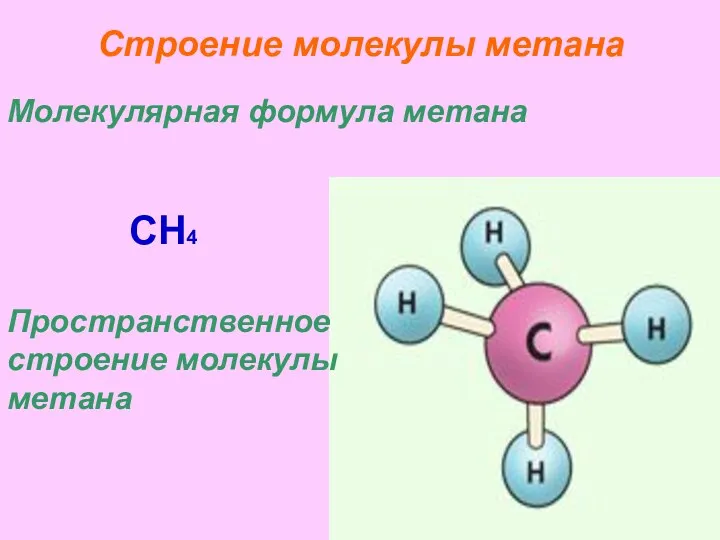
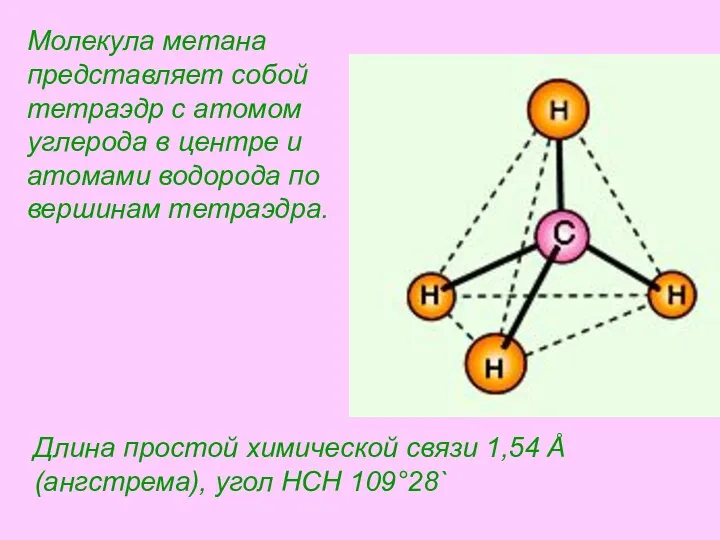
- 18. Строение молекулы метана Молекулярная формула метана CH4 Пространственное строение молекулы метана
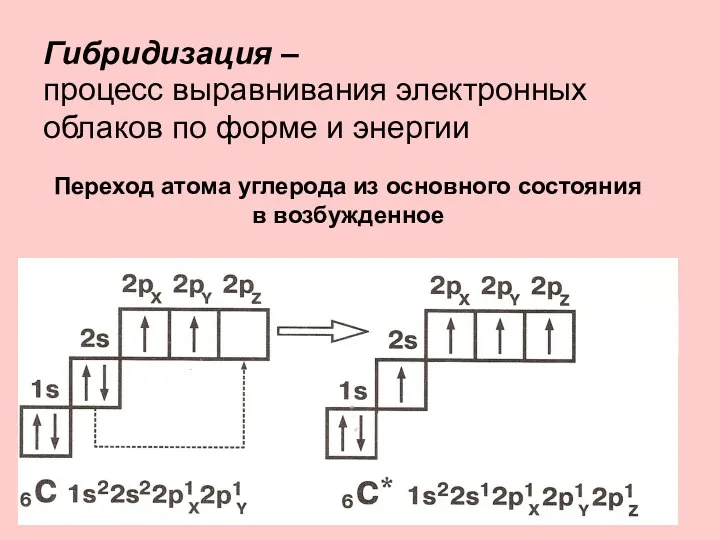
- 19. Гибридизация – Переход атома углерода из основного состояния в возбужденное процесс выравнивания электронных облаков по форме
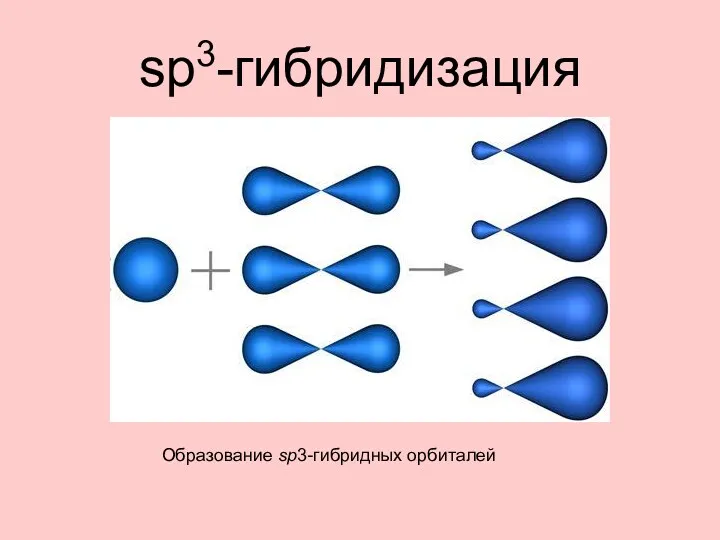
- 20. sp3-гибридизация Образование sp3-гибридных орбиталей
- 21. Модель атома с sp3-гибридными орбиталями
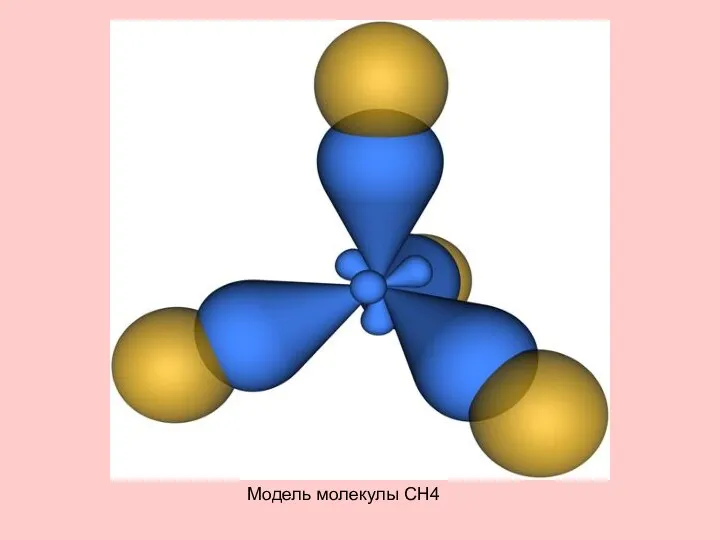
- 22. Модель молекулы CH4
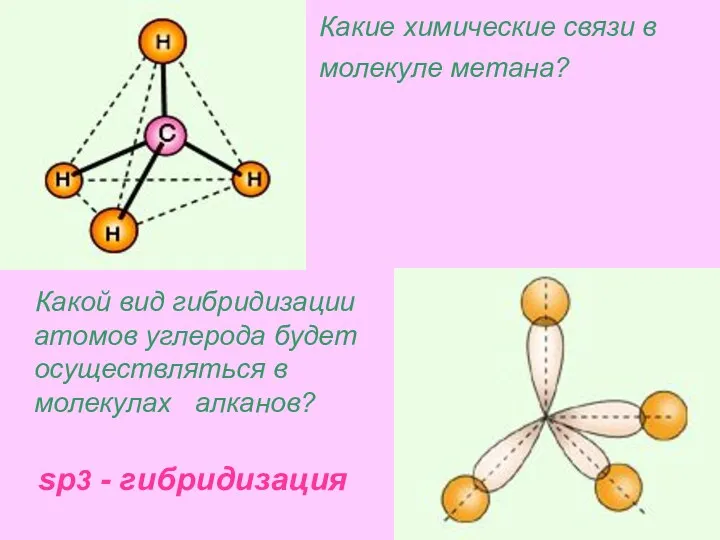
- 23. Какие химические связи в молекуле метана? Какой вид гибридизации атомов углерода будет осуществляться в молекулах алканов?
- 24. Длина простой химической связи 1,54 Å (ангстрема), угол HCH 109°28` Молекула метана представляет собой тетраэдр с
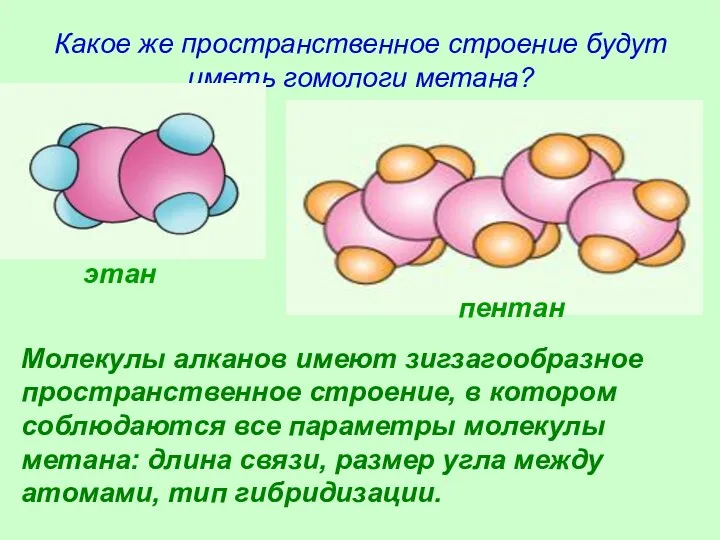
- 25. Какое же пространственное строение будут иметь гомологи метана? Молекулы алканов имеют зигзагообразное пространственное строение, в котором
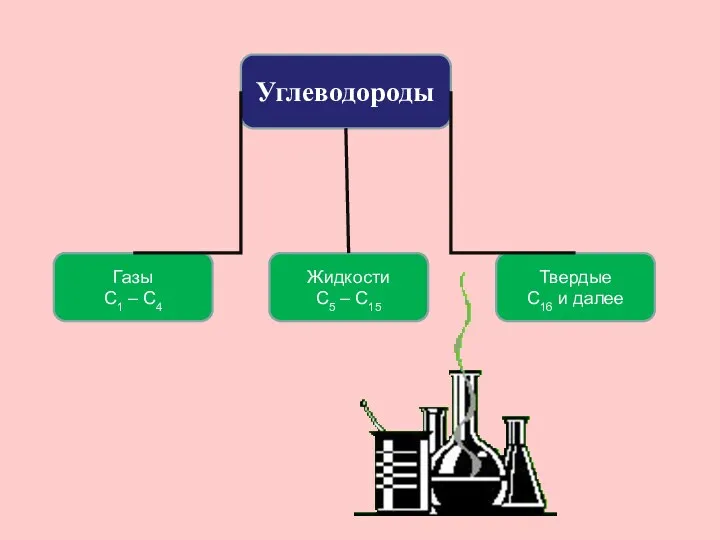
- 26. Углеводороды Жидкости С5 – С15 Газы С1 – С4 Твердые С16 и далее
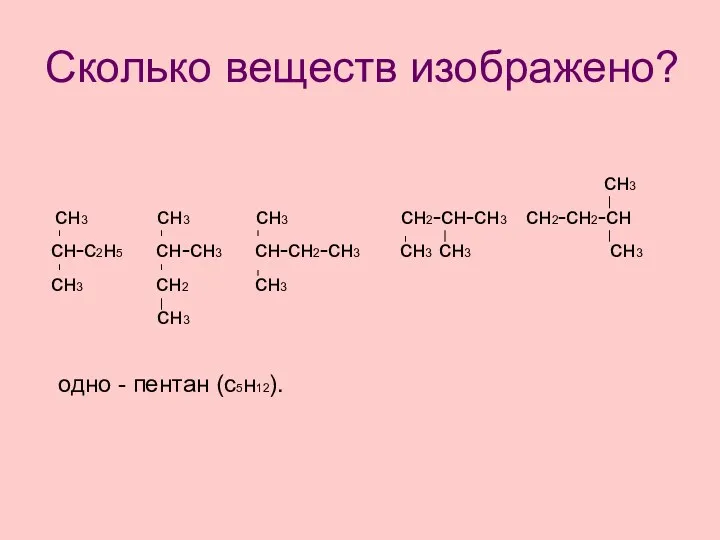
- 27. сн3 сн3 сн3 сн3 сн2-сн-сн3 сн2-сн2-сн сн-с2н5 сн-сн3 сн-сн2-сн3 сн3 сн3 сн3 сн3 сн2 сн3 сн3
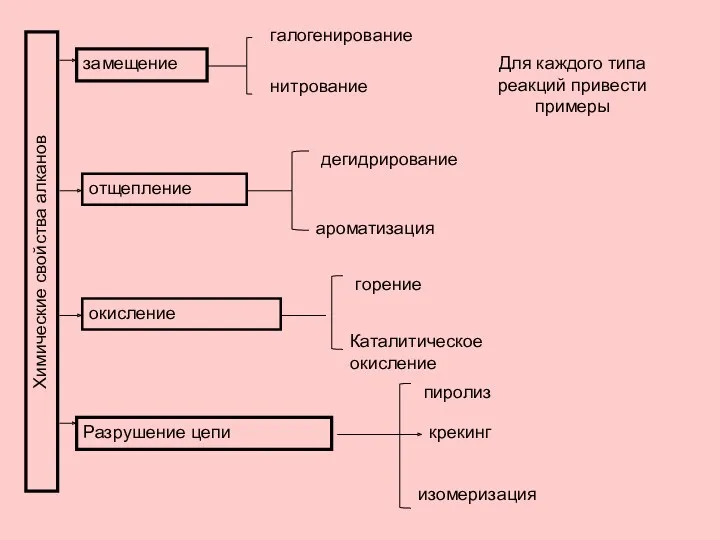
- 28. Химические свойства алканов замещение галогенирование нитрование Для каждого типа реакций привести примеры отщепление дегидрирование ароматизация окисление
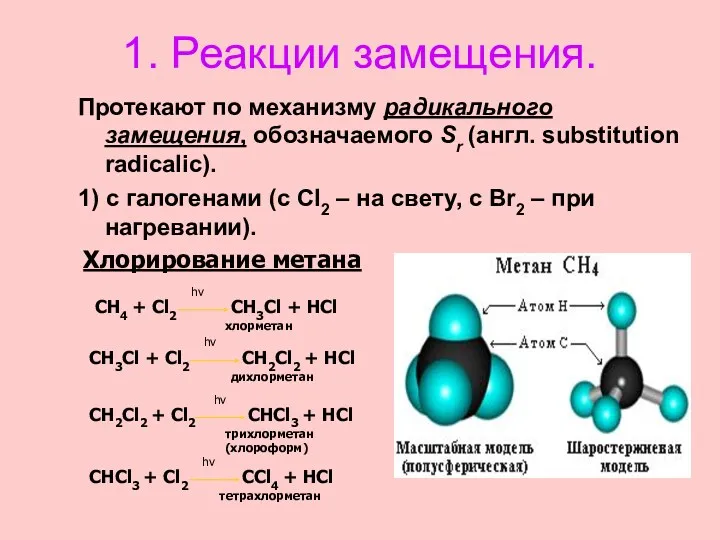
- 29. 1. Реакции замещения. Протекают по механизму радикального замещения, обозначаемого Sr (англ. substitution radicalic). 1) с галогенами
- 30. Механизм реакции замещения Состоит из 3 стадий: -зарождение цепи Cl2 2Cl· -развитие цепи CH4 + Cl·
- 31. СН4 + Сl2 CH3Cl + HCl + Q t Реакции протекают по радикальному механизму. С Н
- 32. 2. Реакции отщепления. а) дегидрирование: CH3 – CH3 Pt,t° CH2=CH2 + H2 этилен 2СН4 Н -
- 33. 3. Реакции окисления. а) все алканы горят с образованием углекислого газа и воды : б) при
- 34. Горение алканов:
- 35. РЕАКЦИЯ ГОРЕНИЯ: CH4 + 2O2 → CO2 + 2H2O + Q
- 36. 4. Разрушение цепи. а) для метана характерен пиролиз: 2CH4 C2H2 + 3H2 ацетилен 1500° C СН4
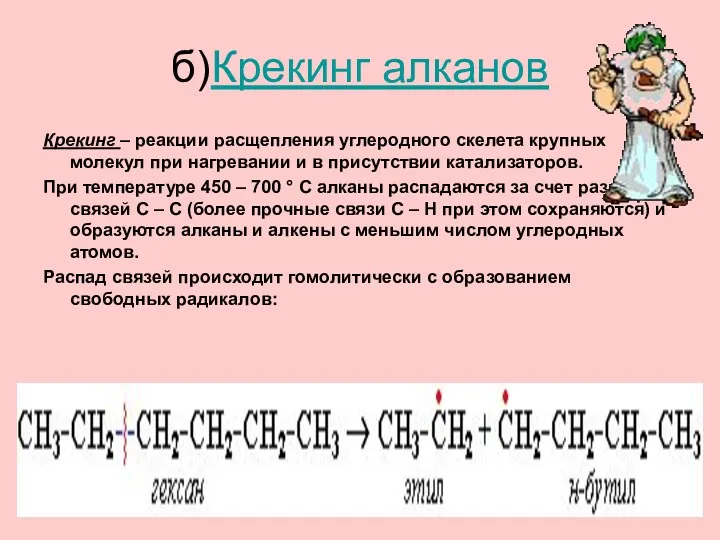
- 37. б)Крекинг алканов Крекинг – реакции расщепления углеродного скелета крупных молекул при нагревании и в присутствии катализаторов.
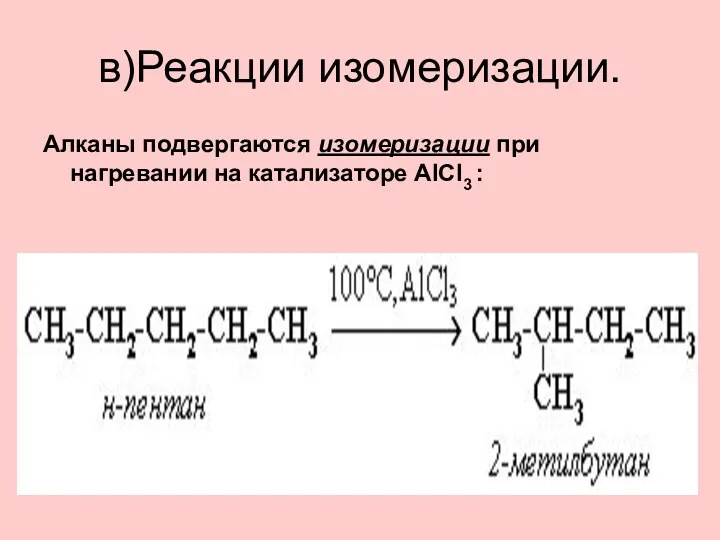
- 38. в)Реакции изомеризации. Алканы подвергаются изомеризации при нагревании на катализаторе AlCl3 :
- 39. Получение алканов
- 40. ДОМАШНЕЕ ЗАДАНИЕ: конспект Желаю удачи!
- 41. МЕТАН – газ, без цвета и запаха, почти в 2 раза легче воздуха, мало растворим в
- 43. Скачать презентацию
















 Электронный помощник по химии (8 класс)
Электронный помощник по химии (8 класс) Застосування радіонуклідів у медицині, тваринництві та археології
Застосування радіонуклідів у медицині, тваринництві та археології Химическая промышленность России
Химическая промышленность России Массовая и объемная доля компонентов смеси
Массовая и объемная доля компонентов смеси Галогенопроизводные углеводородов 1
Галогенопроизводные углеводородов 1 Подгруппа серы и ее соединения
Подгруппа серы и ее соединения Алотропні модифікації фосфору
Алотропні модифікації фосфору Коллигативные свойства растворов
Коллигативные свойства растворов Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Соединения химических элементов
Соединения химических элементов Карбоновые кислоты. 10 класс
Карбоновые кислоты. 10 класс Водородная связь (11 класс)
Водородная связь (11 класс) Решение комбинированных задач. Задачи на смеси
Решение комбинированных задач. Задачи на смеси Смещение химического равновесия
Смещение химического равновесия Вода - вещество обычное или необычное
Вода - вещество обычное или необычное Оксиди: поняття, склад і назви, фізичні властивості, поширеність у природі, використання
Оксиди: поняття, склад і назви, фізичні властивості, поширеність у природі, використання Синтетические моющие средства
Синтетические моющие средства Интересные факты об углеводородах
Интересные факты об углеводородах Водород. Свойства водорода
Водород. Свойства водорода Хроматографические методы, используемые в фармацевтическом анализе
Хроматографические методы, используемые в фармацевтическом анализе Закон сохранения массы веществ
Закон сохранения массы веществ Відносна молекулярна маса речовини, її обчислення за хімічною формулою
Відносна молекулярна маса речовини, її обчислення за хімічною формулою Непредельные углеводороды. Этилен и его гомологи
Непредельные углеводороды. Этилен и его гомологи Состав веществ. Причины многообразия веществ
Состав веществ. Причины многообразия веществ Химическая взрывчатка
Химическая взрывчатка Минералы и их свойства
Минералы и их свойства Омыватель лобового стекла
Омыватель лобового стекла Вуглеводи
Вуглеводи