Содержание
- 2. Конфуций сказал: «Учиться, а время от времени повторять изученное, разве неприятно?»
- 3. Задание 1.Выписать оксиды и распределить их в два столбика: оксиды металлов и неметаллов. Дать названия. Na2O,
- 4. Оксиды Металлов: Na2O оксид натрия CuO оксид меди(II) Cu2O оксид меди(I) Неметаллов: N2O5 оксид азота SO2
- 5. Задание 2. «Четвертый лишний» (уберите лишнее вещество и объясните свой выбор) HNO3, NaOH, HCl, H2SO4
- 6. Кислоты HNO3, HCl, H2SO4
- 7. Задание 3. Выпишите формулы щелочей и нерастворимых оснований в два столбика NaOH, Fe(OH)2, Fe(OH)3, KOH, H2SO4,
- 8. Основания: Растворимые(Щелочи): NaOH KOH Ba(OH)2 Нерастворимые: Fe(OH) 2 Fe(OH) 3 Cu(OH) 2 Zn(OH) 2
- 9. Хлорид натрия NaCl
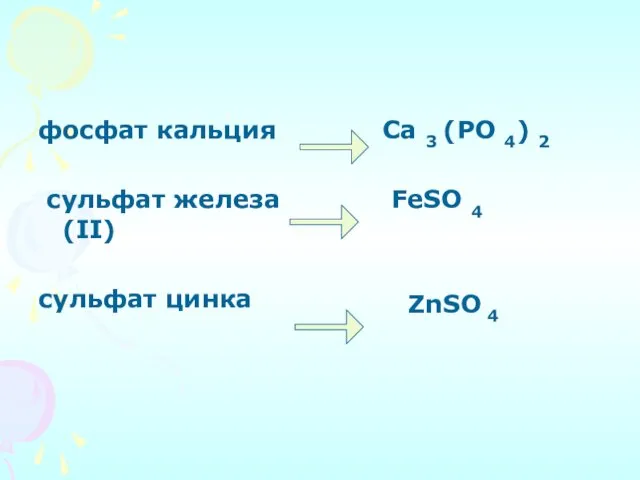
- 10. 4. Составьте формулы солей, входящих в состав поливитамина «Компливит»: фосфат кальция сульфат железа (II) сульфат цинка
- 11. фосфат кальция сульфат железа (II) сульфат цинка Ca 3 (PO 4) 2 FeSO 4 ZnSO 4
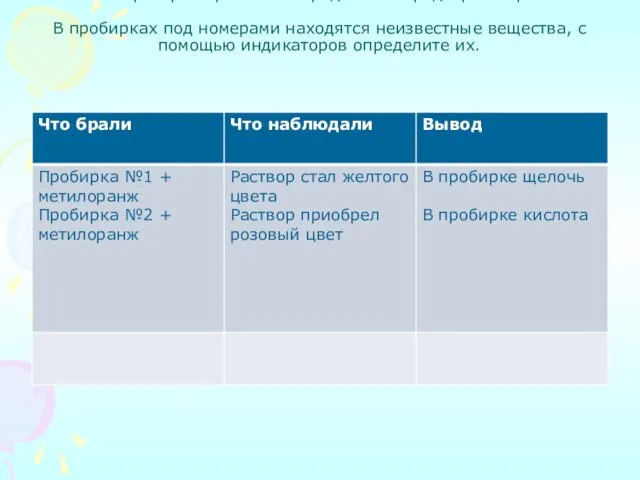
- 12. 5. Лабораторная работа «Определение среды раствора» В пробирках под номерами находятся неизвестные вещества, с помощью индикаторов
- 13. Лабораторная работа «Определение среды раствора» В пробирках под номерами находятся неизвестные вещества, с помощью индикаторов определите
- 14. 6.Определить степень окисления химического элемента в соединениях : CaCI2, Fe2O3, H2S AICI3, Na2O, BaO
- 15. Игра “Найдите соответствие” кислоты Соляная Серная Угольная Азотная Сероводородная Фосфорная соли Сульфаты Фосфаты Сульфиды Нитраты Хлориды
- 16. 7. Игра “Найдите соответствие” кислоты Соляная Серная Угольная Азотная Сероводородная Фосфорная соли Сульфаты Фосфаты Сульфиды Нитраты
- 17. Найдите лишнее
- 18. Домашнеее задание Рабочая тетрадь по химии Стр. 71 задание №5
- 20. Скачать презентацию












 Моя будущая профессия
Моя будущая профессия Физическая химия. Химическая термодинамика
Физическая химия. Химическая термодинамика Йод в нашей жизни
Йод в нашей жизни Химическая кинетика. Закон действующих масс для скорости реакции
Химическая кинетика. Закон действующих масс для скорости реакции Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10)
Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10) Многоатомные спирты
Многоатомные спирты Получение и свойства азота
Получение и свойства азота Галогени. Хімічні властивості
Галогени. Хімічні властивості Аммиак
Аммиак Открытие периодического закона
Открытие периодического закона Гидролиз солей
Гидролиз солей Хром. Строение атома
Хром. Строение атома Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Производство извести
Производство извести Обобщающий урок по теме Металлы
Обобщающий урок по теме Металлы Жиры
Жиры Карбоновые кислоты. Классификация карбоновых кислот
Карбоновые кислоты. Классификация карбоновых кислот Токсикология пестицидов
Токсикология пестицидов Степень окисления
Степень окисления Щелочи
Щелочи Биотестирование токсичности снега в окрестностях школы по проросткам кресс - салата
Биотестирование токсичности снега в окрестностях школы по проросткам кресс - салата Масс-Спектроскопия
Масс-Спектроскопия Кислоты в свете теории электролитической диссоциации (ТЭД), 8 класс
Кислоты в свете теории электролитической диссоциации (ТЭД), 8 класс Химические связи в органических соединениях
Химические связи в органических соединениях Химические опасности. Токсичные элементы. Мышьяк. Свинец. Ртуть
Химические опасности. Токсичные элементы. Мышьяк. Свинец. Ртуть Биоразлагаемые ПАВ. Лекция 2
Биоразлагаемые ПАВ. Лекция 2 Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4)
Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4)