Слайд 2

Вопрос 1
В ряду химических элементов
Li → Na → K →
Rb
увеличивается число электронов во внешнем слое атома
уменьшается число электронных слоёв в атомах
уменьшается число протонов в ядрах атомов
усиливаются металлические свойства
увеличивается радиус атома
Слайд 3

Вопрос 2
В порядке усиления основных свойств гидроксиды расположены в ряду
RbOH–KOH–NaOH
Mg(OH)2–NaOH–KOH
NaOH–Mg(OH)2–Al(OH)3
Ba(OH)2–Sr(OH)2–Mg(OH)2
Ca(OH)2–Sr(OH)2–RbOH
Слайд 4

Вопрос 3
В ряду химических элементов
Li → Be → B →
C
увеличивается число электронов во внешнем слое атома
уменьшается число электронных слоёв в атомах
увеличивается значение высшей валентности
уменьшается число протонов в ядрах атомов
уменьшается электроотрицательность
Слайд 5

Вопрос 4
В ряду химических элементов
As → P → N
увеличивается радиус
атомов
увеличивается электроотрицательность
усиливаются кислотные свойства высших оксидов
возрастает значение высшей степени окисления
увеличивается число электронов во внешнем электронном слое атомов
Слайд 6

Вопрос 5
В ряду химических элементов
Cl → Br → I
увеличиваются радиусы
атомов
уменьшается электроотрицательность атомов
усиливаются неметаллические свойства
возрастает значение высшей степени окисления элементов
увеличивается число электронов во внешнем электронном слое атомов
Слайд 7

Вопрос 6
В каких рядах химические элементы расположены в порядке уменьшения кислотных
свойств высших оксидов?
B → C → N
P →Si → Al
Cl → Br → I
P → S → Cl
Ca → Mg → Be
Слайд 8

Вопрос 7
В порядке уменьшения числа электронов во внешнем слое расположены химические
элементы следующих рядов:
N – O – F
C – Si – Ge
Al – Mg – Na
C – N – O
Br – Se – As
Слайд 9

Вопрос 8
Общим для натрия и алюминия является
наличие 12 протонов в ядрах
их атомов
нахождение валентных электронов в третьем электронном слое
образование простых веществ-металлов
существование в природе в виде двухатомных молекул
образование ими высших оксидов с общей формулой Э2О
Слайд 10

Вопрос 9
В ряду химических элементов
Ge → Si → C
увеличиваются радиусы
атомов
увеличивается электроотрицательность
усиливаются кислотные свойства их высших оксидов
возрастает значение высшей степени окисления
увеличивается число электронов во внешнем электронном слое атомов
Слайд 11

Вопрос 10
Значения высших степеней окисления элементов увеличиваются в рядах:
Al → P
→ Cl
Se → S → O
C → Si → Ge
Ge → As → Se
Be → Mg → Ca










 Побочная подгруппа VIII группы периодической системы
Побочная подгруппа VIII группы периодической системы Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования
Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования Хімічні властивості металів
Хімічні властивості металів Techniques for preparation of gaseous samples with a desired concentration of analyte
Techniques for preparation of gaseous samples with a desired concentration of analyte НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Гидроксид магния. Mg(OH)2
Гидроксид магния. Mg(OH)2 Общие сведения о полезных ископаемых. (Лекция 2)
Общие сведения о полезных ископаемых. (Лекция 2) Вуглеводи
Вуглеводи Cromatografia ionică
Cromatografia ionică Аналитические методы
Аналитические методы Каталитический риформинг
Каталитический риформинг циклоалканы170
циклоалканы170 Современные тенденции развития химии
Современные тенденции развития химии Термодинамика
Термодинамика Комплексные соединения
Комплексные соединения Алкины. Ацетилен (Этин) – С2Н2
Алкины. Ацетилен (Этин) – С2Н2 Катализ и катализаторы
Катализ и катализаторы Тепловой эффект химической реакции. 11 класс
Тепловой эффект химической реакции. 11 класс Непредельные углеводороды ряда этилена
Непредельные углеводороды ряда этилена Предмет аналитической химии, ее структура
Предмет аналитической химии, ее структура Ионы. Проверочная работа
Ионы. Проверочная работа Применение здм к кислотно-основным равновесиям и их роль в аналитической химии
Применение здм к кислотно-основным равновесиям и их роль в аналитической химии Химическая связь
Химическая связь Аммиак
Аммиак Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Алкины. 10 класс
Алкины. 10 класс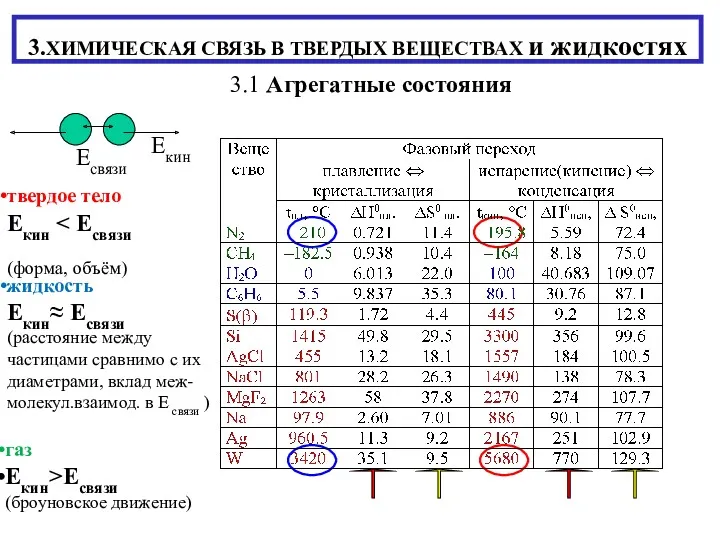 Химическая связь в твердых веществах и жидкостях
Химическая связь в твердых веществах и жидкостях ae2db93272ef42dba476a56bbc56b895
ae2db93272ef42dba476a56bbc56b895