Слайд 2

ЧТО ТАКОЕ ОСНОВАНИЯ?
Основания- сложные вещества, состоящие из атома металла, связанного с
одной или несколькими гидроксогруппами -ОН.
Слайд 3

Слайд 4

Общая формула оснований:
Ме(ОН)n, где
Ме - металл
n-число гидроксогрупп и одновременно валентность
металла.
Слайд 5

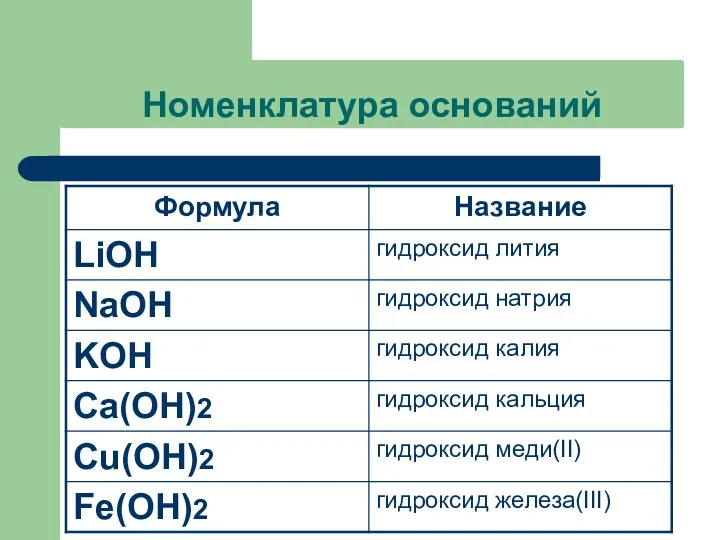
Номенклатура оснований
Название оснований=
Гидроксид + название металла в родительном падеже +
валентность римскими цифрами (переменная)
Слайд 6
Слайд 7

Например:
Fе(ОН)3
Гидроксид железа (ΙΙΙ)
Ва(ОН)2
Гидроксид бария
Слайд 8

Дайте названия гидроксидам:
LiOH
Ba(OH)2
Fe(OH)2
Al(OH)3
NaOH
гидроксид лития
гидроксид бария
гидроксид железа (II)
гидроксид алюминия
гидроксид натрия
Слайд 9
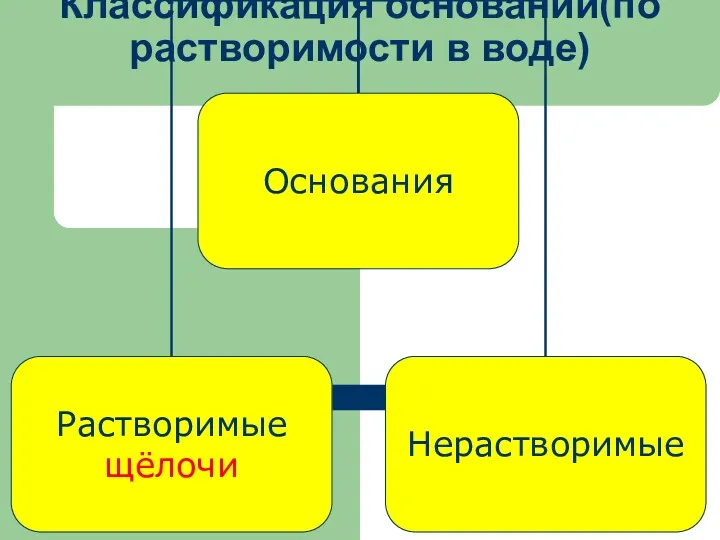
Классификация оснований(по растворимости в воде)
Слайд 10
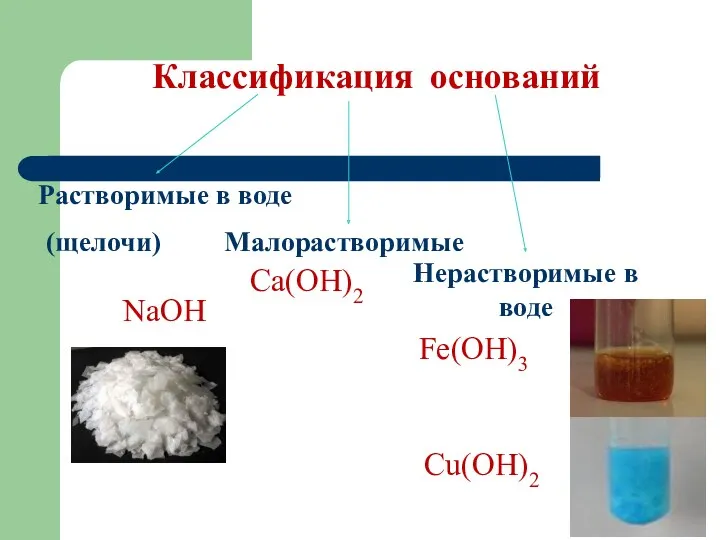
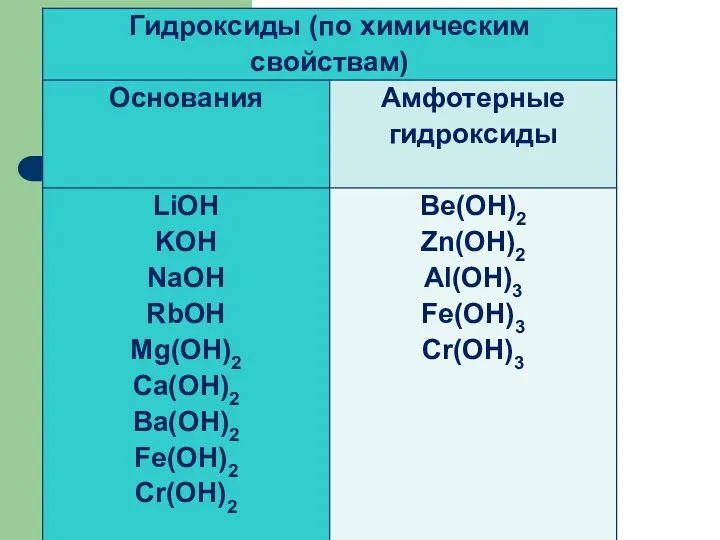
Классификация оснований
Растворимые в воде
(щелочи) Малорастворимые
Нерастворимые в воде
NaOH
Ca(OH)2
Fe(OH)3
Сu(OH)2
Слайд 11
Слайд 12
Слайд 13
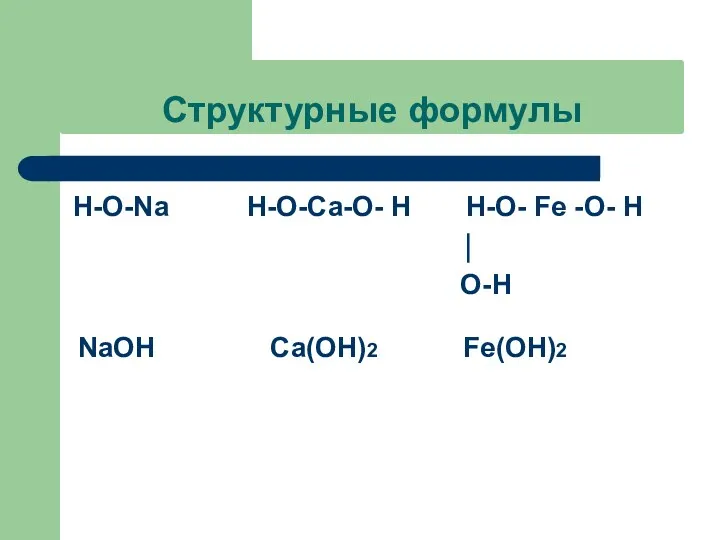
Структурные формулы
Н-О-Na Н-О-Ca-О- Н Н-О- Fe -О- Н
⏐
О-Н
NaOH
Ca(OH)2
Слайд 14

Физические свойства
Основания - твердые кристаллические вещества.
В воде растворимы щелочи:
LiOH , NaOH, KOH, CsOH, RbOH, Ca(OH)2, Sr(OH)2,Ba(OH)2,
другие - малорастворимы.
Слайд 15

Физические свойства
Основания – твердые вещества.
Щелочи растворяются в воде ( к
ним относят основания металлов 1 и 2 а подгрупп, кроме магния и бериллия), мылки на ощупь.
Щелочи очень едкие вещества, могут разъедать ткани и кожу, поэтому обращаться с ними нужно очень осторожно. При попадании на кожу щелочь нейтрализуются слабым раствором уксусной, борной кислот и смывают большим количеством воды.
Слайд 16
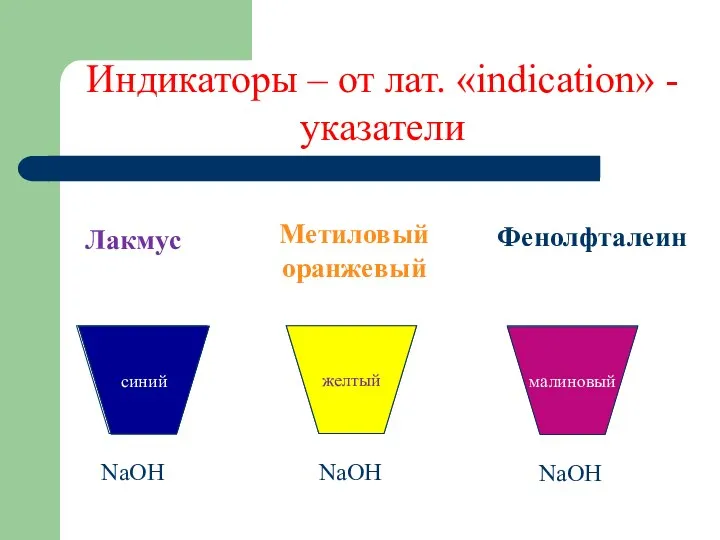
Индикаторы – от лат. «indication» - указатели
NaOH
NaOH
NaOH
Лакмус
Метиловый оранжевый
Фенолфталеин
желтый
малиновый
синий
Слайд 17
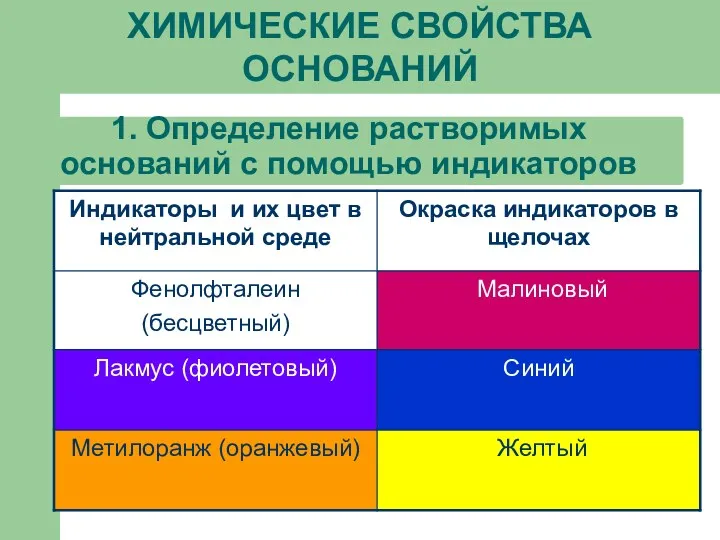
1. Определение растворимых оснований с помощью индикаторов
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
Слайд 18

Важнейшие представители и их применение
NaOH, KOH, Ca(OH)2:
твердые, очень едкие вещества,
растворимые в воде, мылкие на ощупь. При попадании на кожу их следует нейтрализовать слабым раствором борной или уксусной кислоты и смыть водой.
NaOH - гидроксид натрия или едкий натр. Используют при производстве мыла, в кожевенной и фармацевтической промышленности.
KOH - гидроксид калия или едкое кали. Применяют при производстве жидкого мыла, стекла.
Ca(OH)2 - гидроксид кальция или гашеная известь. Немного растворимо в воде. Прозрачный раствор гидроксида кальция называется известковой водой. Ее используют для обнаружения углекислого газа (при пропускании СО2 известковая вода мутнеет, т.к. образуется нерастворимый карбонат кальция) Гидроксид кальция применяется в строительстве, для побелки, получения дезинфицирующего средства (хлорной извести)

















 Теплота згоряння. Температура горіння
Теплота згоряння. Температура горіння Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Лекция 6. Желтые пигменты
Лекция 6. Желтые пигменты Полимеры. Пластмассы. Волокна
Полимеры. Пластмассы. Волокна Електролітична дисоціація. Гідроліз солей
Електролітична дисоціація. Гідроліз солей Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ
Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ Зерттеу әдістері
Зерттеу әдістері Хлороводород..Соляная кислота
Хлороводород..Соляная кислота Фазовое равновесие
Фазовое равновесие Сероводород
Сероводород Франций (Francium)
Франций (Francium) Роль хімії у суспільстві
Роль хімії у суспільстві Кислородсодержащие органические вещества. Фенолы
Кислородсодержащие органические вещества. Фенолы Разнообразие неметаллов
Разнообразие неметаллов Минералогия с основами кристаллографии
Минералогия с основами кристаллографии Фізичні властивості та хімічний склад природних вод
Фізичні властивості та хімічний склад природних вод Припекание взаимно растворимых твердых тел
Припекание взаимно растворимых твердых тел Металл цирконий (ZR)
Металл цирконий (ZR) Азотсодержащие гетероциклические соединения
Азотсодержащие гетероциклические соединения Химия в повседневной жизни человека
Химия в повседневной жизни человека Alyuminiy_ego_soedinenia
Alyuminiy_ego_soedinenia Углерод. Общая характеристика элементов подгруппы углерода
Углерод. Общая характеристика элементов подгруппы углерода Физические и химические свойства алкенов
Физические и химические свойства алкенов Тип соли. Задачи к вопросу 34 по спецификации ЕГЭ-2019
Тип соли. Задачи к вопросу 34 по спецификации ЕГЭ-2019 Особенности органических веществ. Теория химического строения А.М.Бутлерова
Особенности органических веществ. Теория химического строения А.М.Бутлерова Химия нефти и газа
Химия нефти и газа Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Кислоты, их классификация и свойства
Кислоты, их классификация и свойства