Содержание
- 2. Алканами чи парафінами називаються насичені вуглеводні з відкритим ланцюгом, у молекулах яких атоми карбону зв’язані одинарним
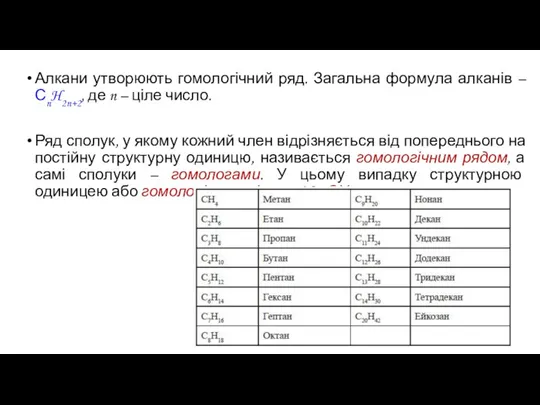
- 3. Алкани утворюють гомологічний ряд. Загальна формула алканів – СnH2n+2, де n – ціле число. Ряд сполук,
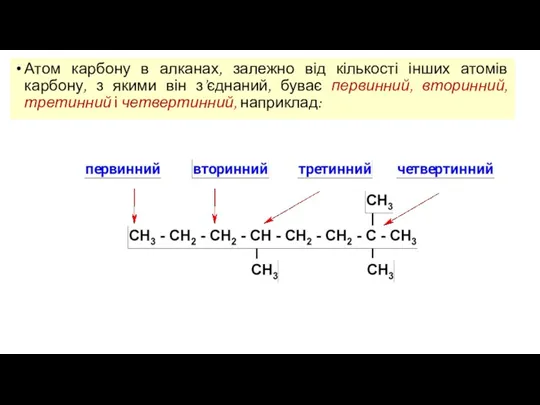
- 4. Атом карбону в алканах, залежно від кількості інших атомів карбону, з якими він з’єднаний, буває первинний,
- 5. Ізомерія – це явище, при якому декілька сполук – ізомери – мають однаковий склад і однакову
- 6. Назвіть речовини:
- 7. Складіть структурну формулу речовин з назвою: а) 4-етил-3,3-диметилгептан; б) 3-етил-2,3,5-триметилнонан; в) 2,2-диметилоктану; г) 3,4-диетил-2,5-диметилгексану; д) 2,3,3-триметилгептану;
- 8. Гідрування вугілля (метод Ф. Бергіуса, 1925) Методи одержання алканів
- 9. З галогенопохідних (Вюрц, 1855) Методи одержання алканів
- 10. Метан синтезують дією води на карбід алюмінію. Реакція Дюма — сплавлення натрієвих або калієвих солей карбонових
- 11. алкани можна отримати гідруванням ненасичених вуглеводнів (алкенів та алкінів): Методи одержання алканів метан та інші алкани
- 12. Фізичні властивості алканів С1-С4 – гази С5-С15 – рідини від С16 – тверді Температура кипіння і
- 13. Хімічні властивості алканів Алкани за своєю природою є насиченими сполуками й тому не вступають у реакції
- 14. Хімічні властивості алканів 1. Реакція горіння (повного окиснення). Усі алкани горять. При цьому утворюються вуглекислий газ
- 15. Хімічні властивості алканів 3. Реакції розкладу (дегідрування). При сильному нагріванні без доступу кисню алкани розкладаються на
- 16. Хімічні властивості алканів 4. Реакції галогенування. З фтором насичені вуглеводні реагують з вибухом, з хлором і
- 17. Хімічні властивості алканів 5. Реакції крекінгу. При високих температурах відбувається розщеплення молекул алканів з розривом зв'язків
- 18. Нітрування алканів Для нітрування алканів застосовують розбавлену нітратну кислоту (метод М. Коновалова, 1899): Хімічні властивості алканів
- 19. Реакції розщеплення Дегідрування алканів (розщеплення зв’язку С-Н і відщеплення гідрогену) дозволяє з насичених вуглеводнів отримати ненасичені.
- 20. 1. Загальна формула алканів А)CnH2n Б) CnH2n+2 В) CnH2n-2 Г)CnH2n-6 2. Який тип гібридизації притаманний алканам:
- 22. Скачать презентацию

















 Электронное строение элементов главной подгруппы III группы
Электронное строение элементов главной подгруппы III группы ЕГЭ Химия. Задание №5
ЕГЭ Химия. Задание №5 Проблема содержания нитратов в пищевых продуктах
Проблема содержания нитратов в пищевых продуктах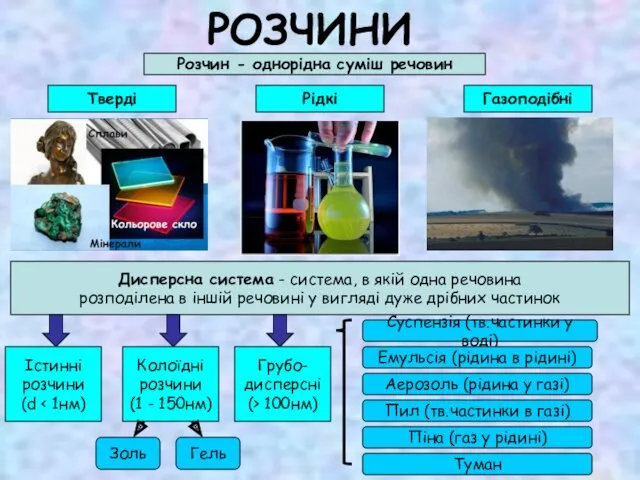 Розчини
Розчини Металлы и сплавы, их строение. Классификация и маркировка сталей. Влияние химических элементов на свариваемость
Металлы и сплавы, их строение. Классификация и маркировка сталей. Влияние химических элементов на свариваемость Розв’язування розрахункових хімічних задач. Методичні рекомендації для вчителів хімії та школярів
Розв’язування розрахункових хімічних задач. Методичні рекомендації для вчителів хімії та школярів Химия в быту
Химия в быту Чистые вещества и смеси
Чистые вещества и смеси Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Хлороводород и соляная кислота
Хлороводород и соляная кислота Фибоначчи. Закономерности химических элементов ряда
Фибоначчи. Закономерности химических элементов ряда Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью
Циклоалканы. Предельные углеводороды с замкнутой (циклической) углеродной цепью Электрохимическая коррозии. Катодные процессы электрохимической коррозии
Электрохимическая коррозии. Катодные процессы электрохимической коррозии Органическая химия
Органическая химия III А – топтың элементтері
III А – топтың элементтері Агрегатные состояния вещества
Агрегатные состояния вещества Азотсодержащие органические соединения
Азотсодержащие органические соединения Азотсодержащие гетероциклические соединения
Азотсодержащие гетероциклические соединения Фосфор и его соединения. 11 класс
Фосфор и его соединения. 11 класс Обед под микроскопом. Минеральные вещества
Обед под микроскопом. Минеральные вещества Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Моя будущая профессия
Моя будущая профессия Кислород. 9 класс
Кислород. 9 класс Теория электролитической диссоциации
Теория электролитической диссоциации Managing chemicals. Green chemistry for every laboratory
Managing chemicals. Green chemistry for every laboratory Фосфор и его соединения
Фосфор и его соединения Предмет органической химии
Предмет органической химии Гидродинамические модели реакторов. Лекция № 2
Гидродинамические модели реакторов. Лекция № 2