Характеристика химического элемента по его положению в периодической системе химических элементов Д.И. Менделеева презентация
Содержание
- 2. Другого ничего в природе нет Ни здесь, ни там, в космических глубинах: Все - от песчинок
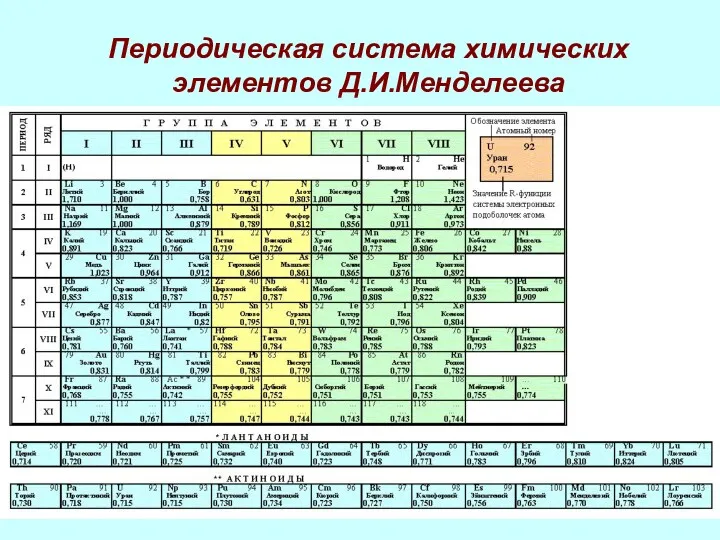
- 3. Периодическая система химических элементов Д.И.Менделеева
- 4. Мы шагаем по Периодической… Характеристика химического элемента по его положению в периодической системе химических элементов Д.И.
- 5. Цели урока: Изучить план характеристики химического элемента и научиться применять его на практике. Обобщить и закрепить
- 6. Кроссворд
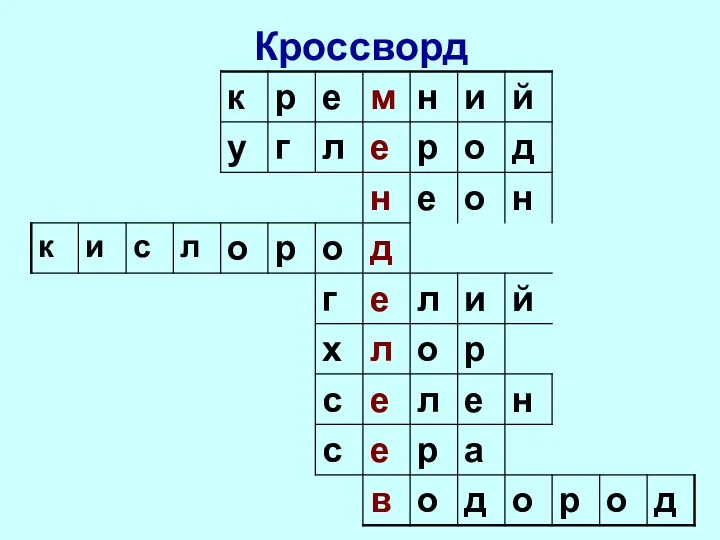
- 7. Кроссворд
- 8. Д.И.Менделеев (1834-1907)-великий русский учёный. Открыл периодический закон химических элементов. Автор классического труда «Основы химии», фундаментальных исследований
- 9. Пусть имя Д.И. Менделеева будет нашей путеводной звездой
- 10. Периодическая система и строение атома Периодическая система- это…. Физический смысл номера: элемента периода группы Причины изменения
- 11. Закономерности В периодах слева направо число электронов на внешнем электронном слое ….., число электронных слоёв …..
- 12. План характеристики элемента. 1. Положение элемента в ПС (номер, период, группа, подгруппа). 2.Строение атома . Степени
- 13. Первая остановка - государство металлов Чтобы узнать какой элемент нас встречает, откроем черный ящик Характеристика элемента
- 14. План характеристики элемента. 1. Положение элемента в ПС (номер, период, группа, подгруппа). 2.Строение атома . Степени
- 15. Характеристика металла натрия 1.Натрий (Na)- элемент 3 периода, 1группы, главной подгруппы, порядковый номер -11, относительная атомная
- 16. Вторая остановка- государство неметаллов 1.Задача. Элемент образует высший оксид состава ЭО3. С водородом этот элемент образует
- 17. План характеристики элемента. 1. Положение элемента в ПС (номер, период, группа, подгруппа). 2.Строение атома . Степени
- 19. Характеристика неметалла серы Сера(S)- элемент 3 периода, 6 А группы, порядковый номер -16, относительная атомная масса
- 20. Лабораторная работа В трех пробирках даны вещества: Соляная кислота, серная кислота, гидроксид натрия. Определите каждое из
- 21. Третья остановка- государство переходных элементов Письмо: В тринадцатой квартире живу, известный в мире как проводник прекрасный,
- 23. План характеристики элемента. 1. Положение элемента в ПС (номер, период, группа, подгруппа). 2.Строение атома . Степени
- 24. Характеристика алюминия Алюминий ( Al)- элемент 3 периода, 3А группы, порядковый номер -13, относительная атомная масса
- 25. Выводы : Химические элементы делятся на……. Атомы металлов на внешнем уровне содержат……электронов. При химических реакциях металлы
- 26. 6.Атомы неметаллов на внешнем уровне содержат…… электронов. Атомы неметаллов могут присоединять и отдавать электроны, т.е. проявляют
- 27. Проанализируйте стихотворение Гладкова с т.з. химии Пусть зимний день с метелями Не навевает грусть- Таблицу Менделеева
- 28. Человек рождается на свет, Чтоб творить, дерзать- и не иначе, Чтоб оставить в жизни добрый след
- 29. Я узнал … Я запомнил … Полученные на уроке знания мне пригодятся……. Мне понравилось … Выскажите
- 30. Домашнее задание Характеристика элемента по плану с порядковыми номерами: 7, 12.
- 32. Скачать презентацию


























 Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды Массовая доля вещества в растворе
Массовая доля вещества в растворе Металлы подгруппы железа Fe, Co, Ni
Металлы подгруппы железа Fe, Co, Ni АЛКАНЫ 9 класс
АЛКАНЫ 9 класс Поддержание заданного качества свинцового теплоносителя для энергетических ядерных реакторов
Поддержание заданного качества свинцового теплоносителя для энергетических ядерных реакторов Гониометрическое исследование кристаллов
Гониометрическое исследование кристаллов Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Растворы. Смеси веществ
Растворы. Смеси веществ Полистирол өндірісі
Полистирол өндірісі Степень загрязнения почвы по химическому составу снежного покрова на разном удалении от источника загрязнения
Степень загрязнения почвы по химическому составу снежного покрова на разном удалении от источника загрязнения Электролиз. Коррозия и защита металлов
Электролиз. Коррозия и защита металлов Коррозия металлов. Методы защиты металлов от коррозии
Коррозия металлов. Методы защиты металлов от коррозии Химия в повседневной жизни
Химия в повседневной жизни Химические формулы
Химические формулы Драгоценные камни
Драгоценные камни Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ
Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ Нано-порошки. Способы получения нано-порошков
Нано-порошки. Способы получения нано-порошков Полимеры и пластические массы
Полимеры и пластические массы Anionic Polymerization
Anionic Polymerization Физико-химические свойства аммиака. Производство аммиака
Физико-химические свойства аммиака. Производство аммиака Обмен липидов
Обмен липидов Кислотно-основные свойства органических соединений. (Лекция 3)
Кислотно-основные свойства органических соединений. (Лекция 3) Массовая доля элемента в сложном веществе
Массовая доля элемента в сложном веществе Типы химических реакций
Типы химических реакций Кислоты. Растворы всех кислот
Кислоты. Растворы всех кислот Периодический закон Д.И. Менделеева. Строение атома. Химическая связь
Периодический закон Д.И. Менделеева. Строение атома. Химическая связь Алюминий
Алюминий Применение спиртов
Применение спиртов