Содержание
- 2. As I этап Предварительное исследование (отрицательное значение) р. Зангер-Блека As2Hg3 Условия: 1) купированный Zn и SnCl2;
- 3. Примечание: к условиям реакции Зангера-Блека К дробному анализу мышьяка Условия проведения реакции Зангер-Блека 1) SnCl2 –
- 4. 2) Уксусно-свинцовая вата [Pb(CH3COO)2 – для связывания примеси (H2S)] а) H2SO4 + 8[H] → H2S↑ +
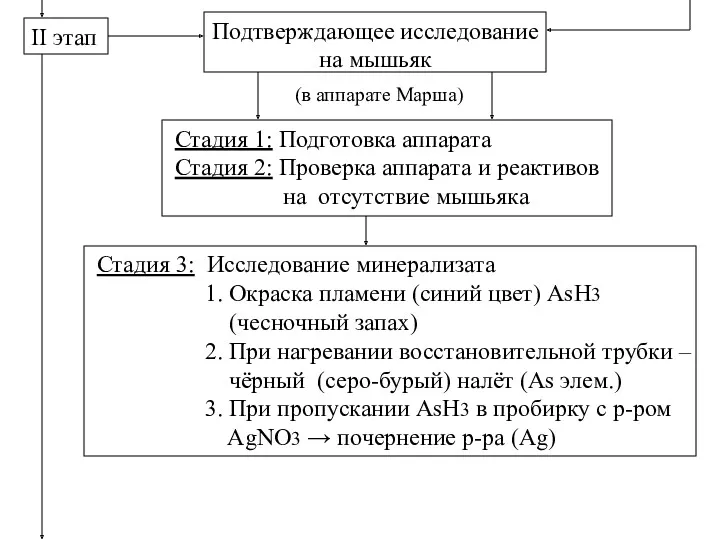
- 5. II этап Подтверждающее исследование на мышьяк (в аппарате Марша) Стадия 1: Подготовка аппарата Стадия 2: Проверка
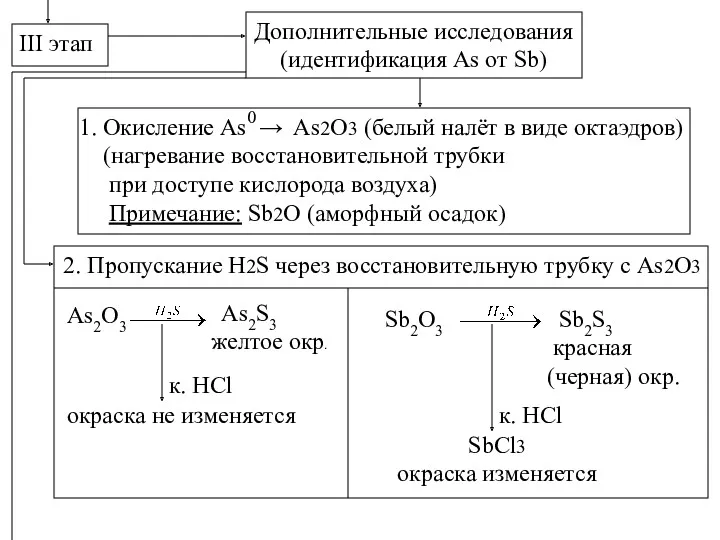
- 6. III этап Дополнительные исследования (идентификация As от Sb) 1. Окисление As → As2O3 (белый налёт в
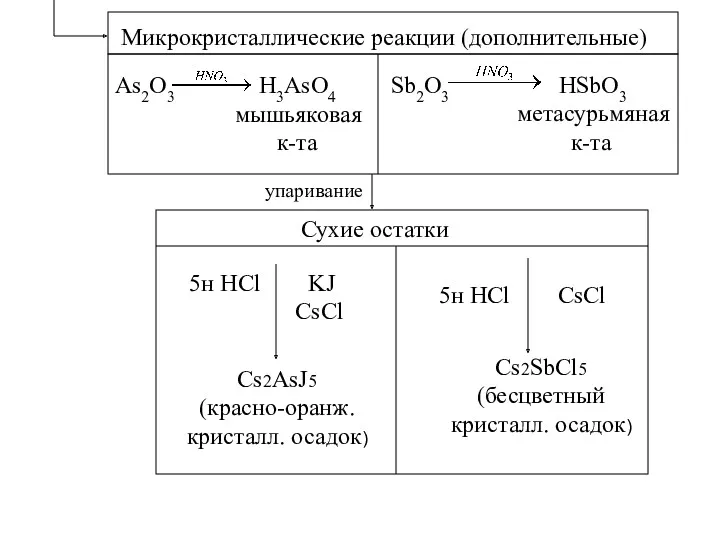
- 7. Микрокристаллические реакции (дополнительные) As2O3 H3AsO4 мышьяковая к-та Sb2O3 HSbO3 метасурьмяная к-та упаривание Сухие остатки 5н HCl
- 8. 2. Химико-токсикологическое доказательство ртути в биологическом материале. А. Изолирование ртути из биологического материала. При изолировании ртути
- 9. 1. А.Н. Крылова [1968 г] - Деструктивный метод изолирования ртути из тканей внутренних органов 1.1. А.А.
- 10. Сущность метода, предложенного авторами, заключается в том, что в процессе деструкции биологического материала происходит только частичное
- 11. Таким образом, деструкция объекта проходит в мягких условиях, без существенного повышения температуры, при этом важную роль
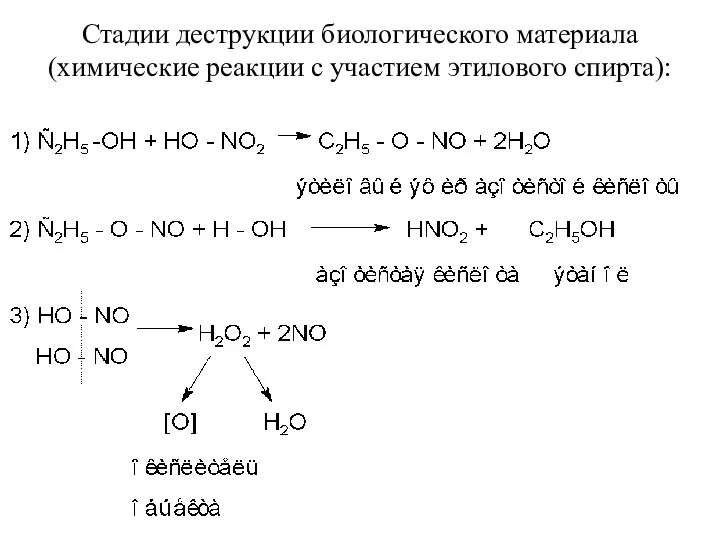
- 12. Стадии деструкции биологического материала (химические реакции с участием этилового спирта):
- 13. Б. Изолирование ртути из биологической жидкости (мочи). А.Ф. Рубцов и А.Н. Крылова [НИИСМ, 1975 г] предложили
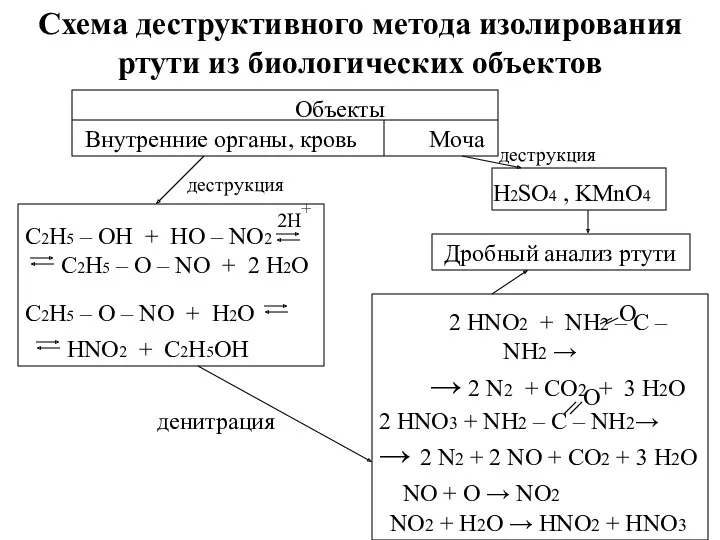
- 14. Схема деструктивного метода изолирования ртути из биологических объектов Объекты Внутренние органы, кровь Моча деструкция C2H5 –
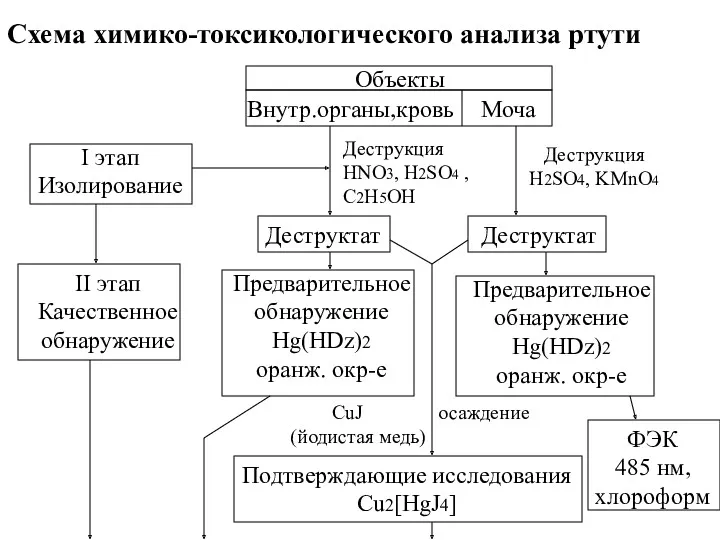
- 15. Объекты Внутр.органы,кровь Моча I этап Изолирование Деструкция HNO3, H2SO4 , C2H5OH Деструкция H2SO4, KMnO4 Деструктат Деструктат
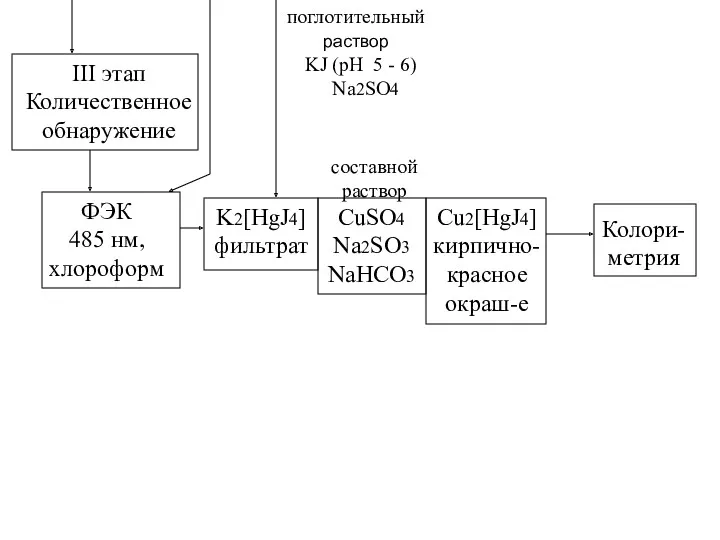
- 16. III этап Количественное обнаружение ФЭК 485 нм, хлороформ поглотительный раствор KJ (рН 5 - 6) Na2SO4
- 18. Скачать презентацию


![2) Уксусно-свинцовая вата [Pb(CH3COO)2 – для связывания примеси (H2S)] а)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/217338/slide-3.jpg)

![1. А.Н. Крылова [1968 г] - Деструктивный метод изолирования ртути](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/217338/slide-8.jpg)



 Protein and amino acid metabolism
Protein and amino acid metabolism Спирты. Лекция
Спирты. Лекция Свойства НЦ
Свойства НЦ Марганец. Железо
Марганец. Железо Фосфор и его соединения
Фосфор и его соединения Основні класи неорганічних сполук
Основні класи неорганічних сполук Спектроскопия лазерных кристаллов
Спектроскопия лазерных кристаллов Соли: карбонаты, галоиды, сульфаты
Соли: карбонаты, галоиды, сульфаты Основы электрохимии
Основы электрохимии Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Теплові прояви механічної, електричної та хімічної енергії
Теплові прояви механічної, електричної та хімічної енергії Окислительно-восстановительные реакции. Лабораторная работа
Окислительно-восстановительные реакции. Лабораторная работа Получение высокодисперсных проводящих оксидов - носителей платинового катализатора для низкотемпературных топливных элементов
Получение высокодисперсных проводящих оксидов - носителей платинового катализатора для низкотемпературных топливных элементов Смог и его виды
Смог и его виды Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Каменный уголь. Фенол
Каменный уголь. Фенол Оксиды. Бинарное соединение. Степень окисления у неметаллов
Оксиды. Бинарное соединение. Степень окисления у неметаллов Алкадиены
Алкадиены Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Электрохимические накопители энергии
Электрохимические накопители энергии Непредельные углеводороды
Непредельные углеводороды Mercury. Mercury cycle
Mercury. Mercury cycle Валентність хімічних елементів
Валентність хімічних елементів Реакции ионного обмена
Реакции ионного обмена Коллоидная химия
Коллоидная химия Природный и попутный нефтяные газы
Природный и попутный нефтяные газы Алкины. Гомологический ряд
Алкины. Гомологический ряд Физические и химические явления. Условия течения и признаки химических реакций
Физические и химические явления. Условия течения и признаки химических реакций