Содержание
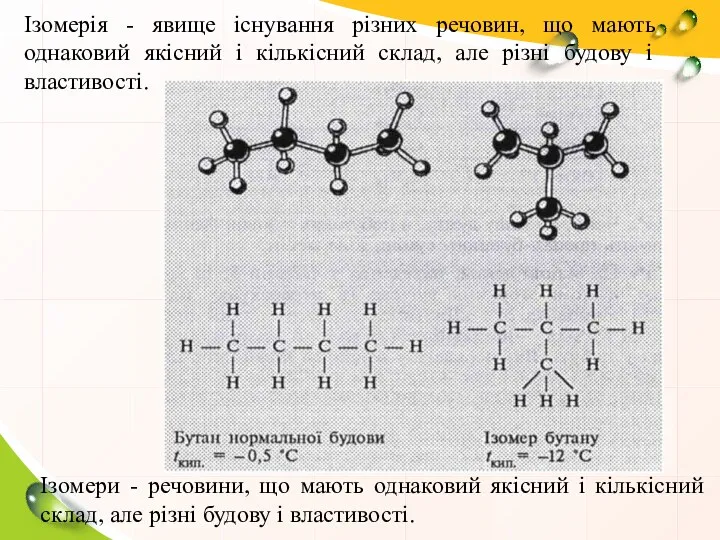
- 2. Ізомерія - явище існування різних речовин, що мають однаковий якісний і кількісний склад, але різні будову
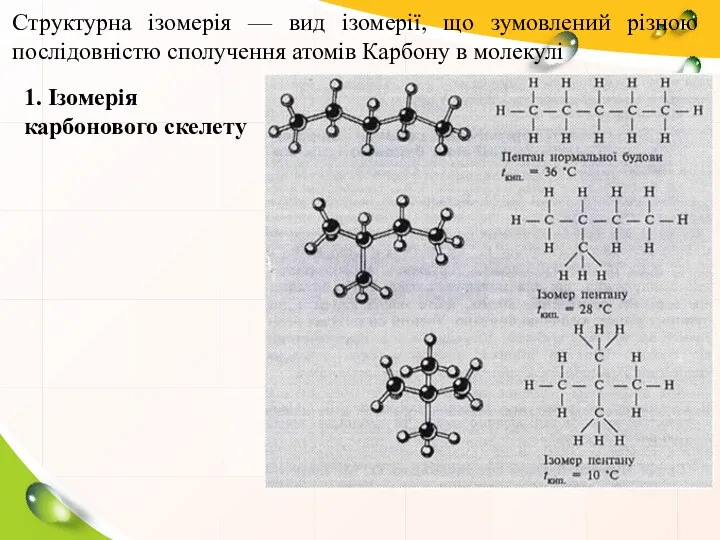
- 3. Структурна ізомерія — вид ізомерії, що зумовлений різною послідовністю сполучення атомів Карбону в молекулі 1. Ізомерія
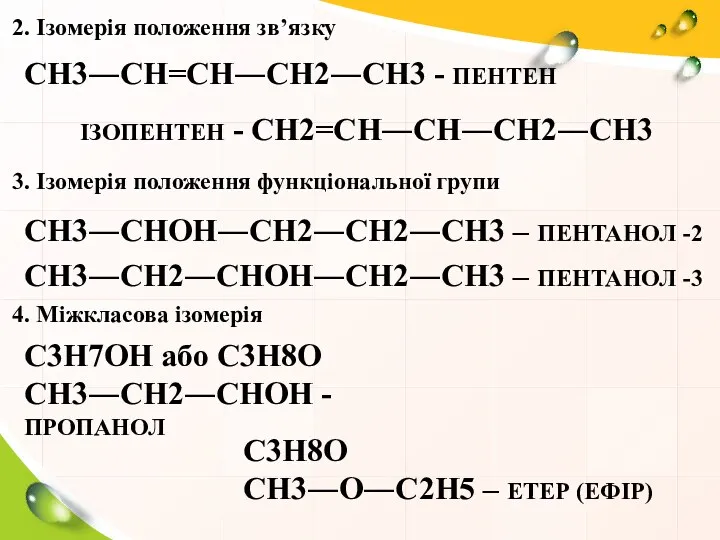
- 4. 2. Ізомерія положення зв’язку СН3―СН=СН―СН2―СН3 - ПЕНТЕН ІЗОПЕНТЕН - СН2=СН―СН―СН2―СН3 3. Ізомерія положення функціональної групи СН3―СНОН―СН2―СН2―СН3
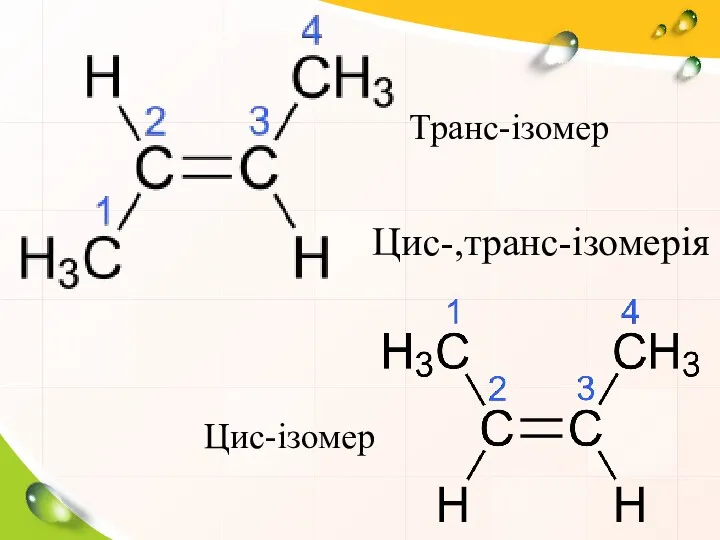
- 5. Цис-,транс-ізомерія Транс-ізомер Цис-ізомер
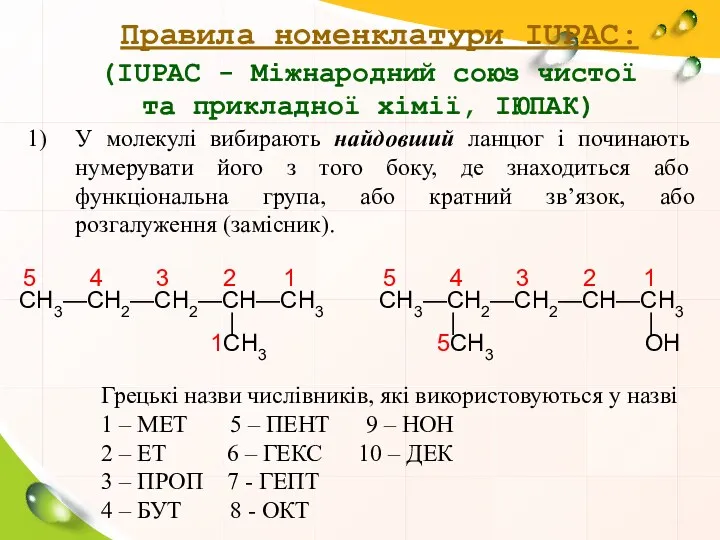
- 7. Правила номенклатури IUPAC: (IUPAC - Міжнародний союз чистої та прикладної хімії, ІЮПАК) У молекулі вибирають найдовший
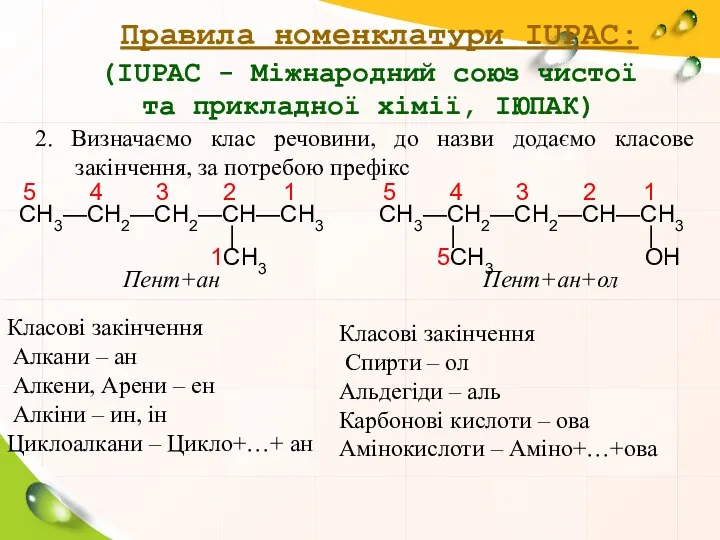
- 8. Правила номенклатури IUPAC: (IUPAC - Міжнародний союз чистої та прикладної хімії, ІЮПАК) 2. Визначаємо клас речовини,
- 9. Правила номенклатури IUPAC: (IUPAC - Міжнародний союз чистої та прикладної хімії, ІЮПАК) Головний ланцюг не обов’язково
- 10. Правила номенклатури IUPAC: (IUPAC - Міжнародний союз чистої та прикладної хімії, ІЮПАК) Замісник не може бути
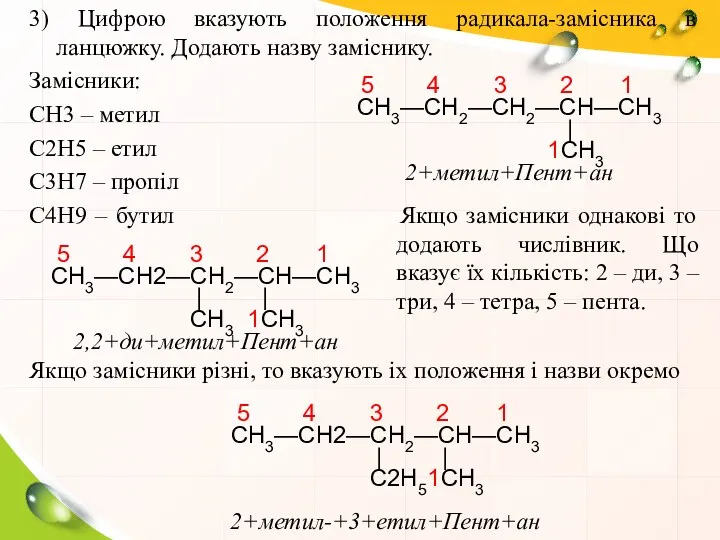
- 11. 3) Цифрою вказують положення радикала-замісника в ланцюжку. Додають назву заміснику. Замісники: СН3 – метил С2Н5 –
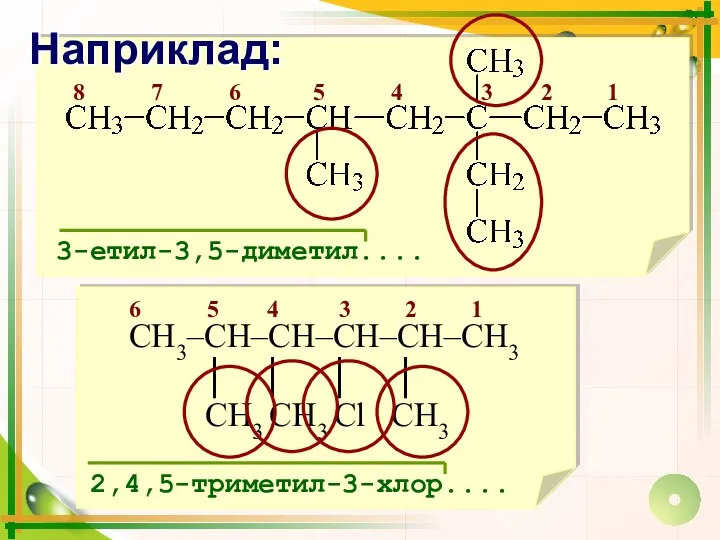
- 12. 8 7 6 5 4 3 2 1 3-етил-3,5-диметил.... 6 5 4 3 2 1 2,4,5-триметил-3-хлор....
- 14. Скачать презентацию



 Термодинамическое равновесие
Термодинамическое равновесие Химический состав клетки
Химический состав клетки Простые спектры 1Н ЯМР
Простые спектры 1Н ЯМР Алкины. Строение алкинов
Алкины. Строение алкинов Элементы подгруппы углерода
Элементы подгруппы углерода Галогены. Их роль в нашей жизни
Галогены. Их роль в нашей жизни Генетическая связь между классами неорганических веществ. Химический тренажёр
Генетическая связь между классами неорганических веществ. Химический тренажёр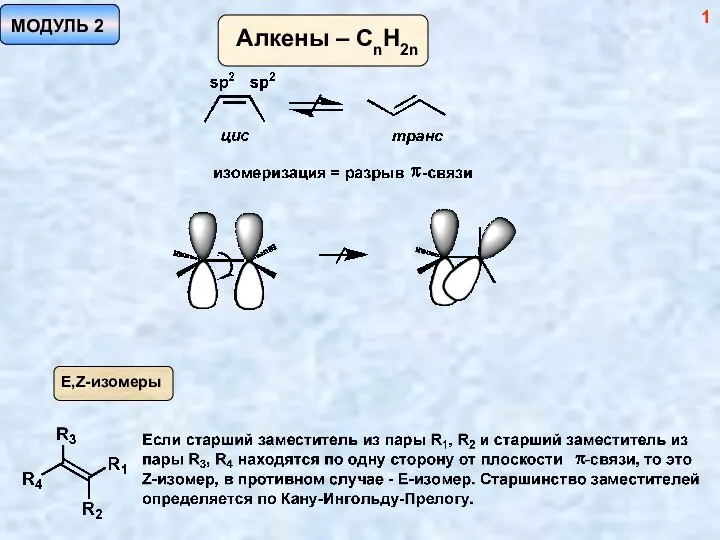 Методы синтеза алкенов. (Модуль 2)
Методы синтеза алкенов. (Модуль 2) Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Розділення неоднорідної суміші. Практична робота № 2
Розділення неоднорідної суміші. Практична робота № 2 Соли
Соли Электрохимия. Электропроводность растворов. Электродные потенциалы. Гальванические элементы
Электрохимия. Электропроводность растворов. Электродные потенциалы. Гальванические элементы Предмет химии. Вещества и их физические свойства
Предмет химии. Вещества и их физические свойства Углеводы, липиды
Углеводы, липиды Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2)
Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2) Влияние катализатора на скорость химической реакции. Катализ
Влияние катализатора на скорость химической реакции. Катализ Кислородные соединения азота
Кислородные соединения азота Характеристика элементов VI группы .Кислород. Озон
Характеристика элементов VI группы .Кислород. Озон Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод
Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод Эксплуатационные материалы
Эксплуатационные материалы Пена и пенообразователи. Назначение, виды, состав и свойства
Пена и пенообразователи. Назначение, виды, состав и свойства Електролітична дисоціація. Гідроліз солей
Електролітична дисоціація. Гідроліз солей Ароматты комирсутектер Бензол
Ароматты комирсутектер Бензол Оксиды. Классификация и химические свойства
Оксиды. Классификация и химические свойства Химический состав и пищевая ценность плодов и овощей
Химический состав и пищевая ценность плодов и овощей Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева Строение атома. Химическая связь
Строение атома. Химическая связь Алюминий
Алюминий