Содержание
- 2. ЕЛЕКТРОЛІТИЧНА ДИСОЦІАЦІЯ Хімічні сполуки, за їх здатністю проводити електричний струм поділяють, на електроліти, які проводять струм
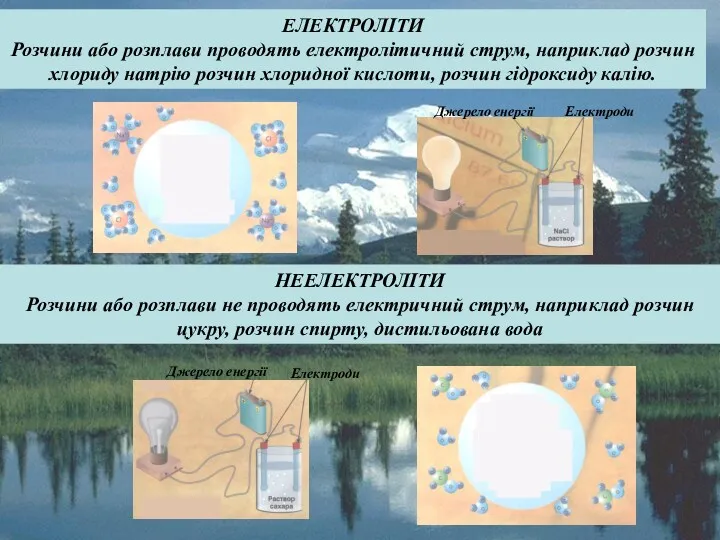
- 3. ЕЛЕКТРОЛІТИ Розчини або розплави проводять електролітичний струм, наприклад розчин хлориду натрію розчин хлоридної кислоти, розчин гідроксиду
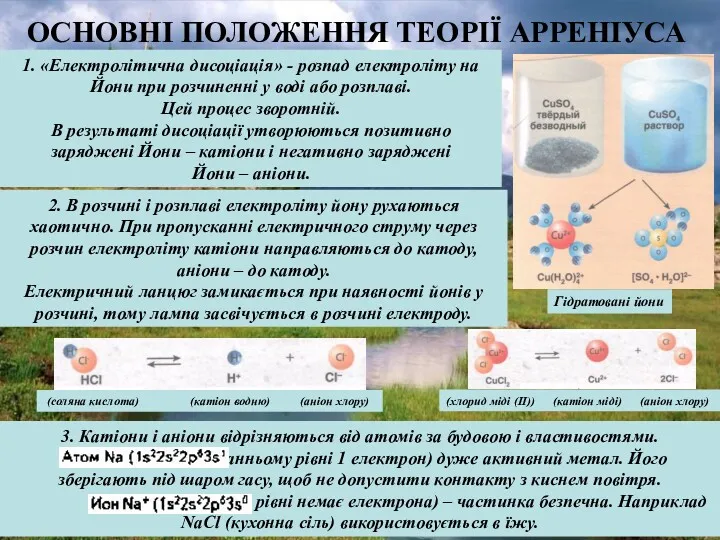
- 4. ОСНОВНІ ПОЛОЖЕННЯ ТЕОРІЇ АРРЕНІУСА 1. «Електролітична дисоціація» - розпад електроліту на Йони при розчиненні у воді
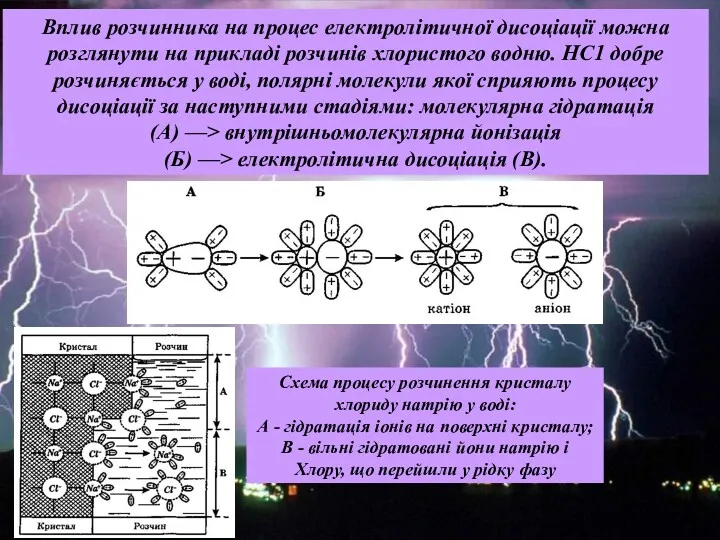
- 5. Вплив розчинника на процес електролітичної дисоціації можна розглянути на прикладі розчинів хлористого водню. НС1 добре розчиняється
- 6. Запис рівнянь електролітичної дисоціації неорганічних речовин – кислот, основ та солей
- 7. Умови перебігу реакцій обміну до кінця (правило Бертолле)
- 8. СКЛАДАННЯ ЙОННО-МОЛЕКУЛЯРНИХ РІВНЯНЬ При складанні йонно-молекулярних рівнянь дотримуються таких правил: а) малорозчинні, малодисоційовані і газуваті речовини
- 9. ХАРАКТЕРИСТИКА КИСЛОТНОСТІ СЕРЕДОВИЩА ТА КИСЛОТНО-ОСНОВНІ ІНДИКАТОРИ Якісною характеристикою кислотності розчинів є поділ їх на кислотні, нейтральні
- 10. Співвідношення між реакцією середовища, концентраціями йонів і значенням водневого показника мають вигляд: Шкала pH Визначення pH
- 12. ВИМІРЮВАННЯ pH За допомогою pH-метра можна точно виміряти концентрацію йонів гідроксонію. Пристрій показує: рН=5,83 Цифровий рН-метр
- 13. ОБЧИСЛЕННЯ рH РОЗЧИНІВ СИЛЬНИХ І СЛАБКИХ ЕЛЕКТРОЛІТІВ
- 14. ХАРАКТЕРИСТИКА ДЕЯКИХ КИСЛОТНО-ОСНОВНИХ ІНДИКАТОРІВ Індикаторами називають органічні речовини, які змінюють своє забарвлення, залежно від концентрації гідроген-іонів,
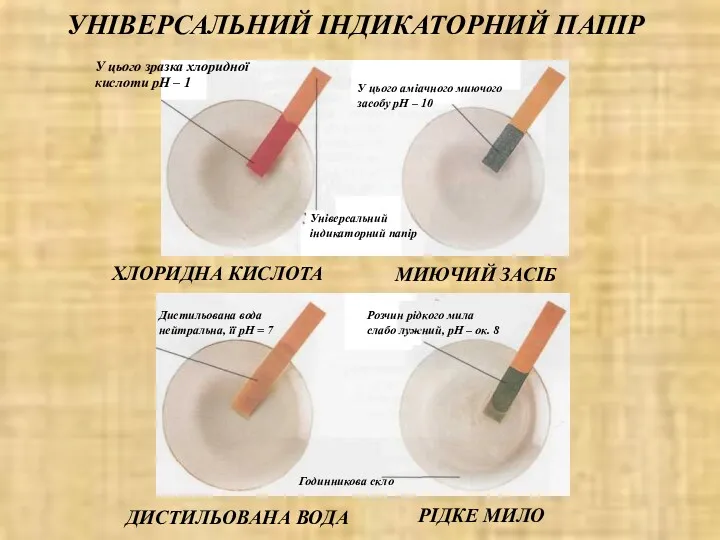
- 15. УНІВЕРСАЛЬНИЙ ІНДИКАТОРНИЙ ПАПІР У цього зразка хлоридної кислоти рН – 1 У цього аміачного миючого засобу
- 16. СИЛА КИСЛОТ І ОСНОВ Силу кислот і основ (згідно теорії Арреніуса) визначають за значеннями їхніх констант
- 17. Як кожна оборотна реакція, процес дисоціації характеризується станом рівноваги. Рівновага, в свою чергу, характеризується ступенем дисоціації,
- 18. До розчинів слабких електролітів, як до рівноважних гомогенних систем, може бути застосовано закон діючих мас, на
- 19. ПРОТОННА ТЕОРІЯ КИСЛОТ І ОСНОВ Протонна теорія кислот і основ була запропонована в 1923 р. Й.
- 20. Згідно протонної теорії кислотою називають сполуку, яка віддає протони, тобто є донором протонів. Основою називають сполуку,
- 21. Продуктом кислотно-основної взаємодії є нова кислота й нова основа, а не сіль, як за теорією Арреніуса,
- 22. Амфоліти можуть реагувати як з кислотами, так і з основами. Наприклад, взаємодію цинк гідроксиду з кислотами
- 23. Співставлення різних визначень кислот і основ
- 24. Малорозчинні електроліти, які в таблиці розчинності кислот, основ та солей якісно оцінюють як малорозчинні (м) і
- 25. αкαа = ДА У насиченому розчині важкорозчинної сполуки добуток активностей йонів за сталих температури і тиску
- 26. ДР хрому аргентуму становитиме: Насичений розчин хромату аргентуму характеризується такою рівновагою: ДОБУТОК АКТИВНОСТІ (ДА) Внаслідок сповільнення
- 27. БУФЕРНІ РОЗЧИНИ В окремих випадках протікання технологічних, біохімічних або інших процесів вимагає сталості рН середовища. Для
- 28. 2. Додавання сильної кислоти. При додаванні невеликої кількості сильної кислоти відбувається реакція: 3. Додавання лугу. Доданий
- 29. Стандартні буферні розчини
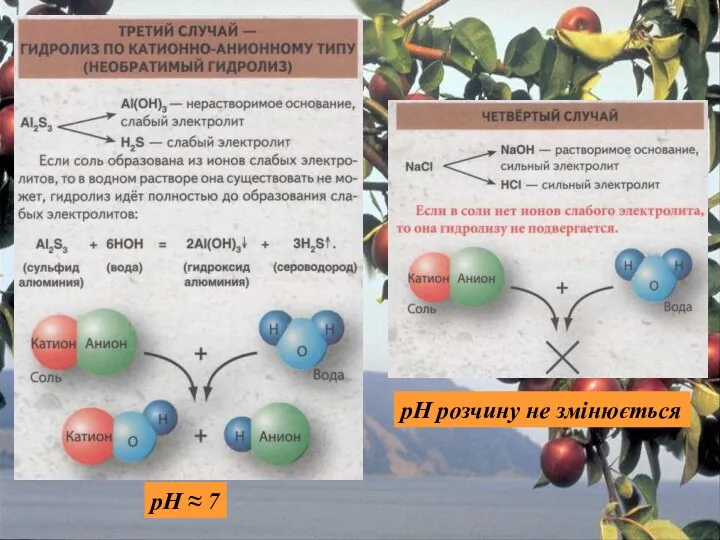
- 30. ГІДРОЛІЗ СОЛЕЙ Гідроліз — це обмінна реакція йонів солі з водою, що призводить до утворення слабкого
- 31. рН pH > 7
- 32. рН ≈ 7 pH розчину не змінюється
- 33. При складанні рівнянь гідролізу враховують наступне: 1. Здебільшого гідроліз є оборотним процесом, крім випадків, коли продукти
- 34. ДЛЯ ЧОГО ПОТРІБЕН ГІДРОЛІЗ Гідроліз – це реакція між речовинами і водою. Таке визначення охоплює гідроліз
- 36. Скачать презентацию




























 Фенолы+
Фенолы+ Классификация химических реакций
Классификация химических реакций Механизмы органических реакций
Механизмы органических реакций Химия в повседневной жизни человека
Химия в повседневной жизни человека Водород
Водород Нуклеозиды. Нуклеиновые кислоты
Нуклеозиды. Нуклеиновые кислоты Классы неорганических веществ. Классификация неорганических веществ
Классы неорганических веществ. Классификация неорганических веществ Поширення металів у природі
Поширення металів у природі Кислоты. Химические свойства кислот
Кислоты. Химические свойства кислот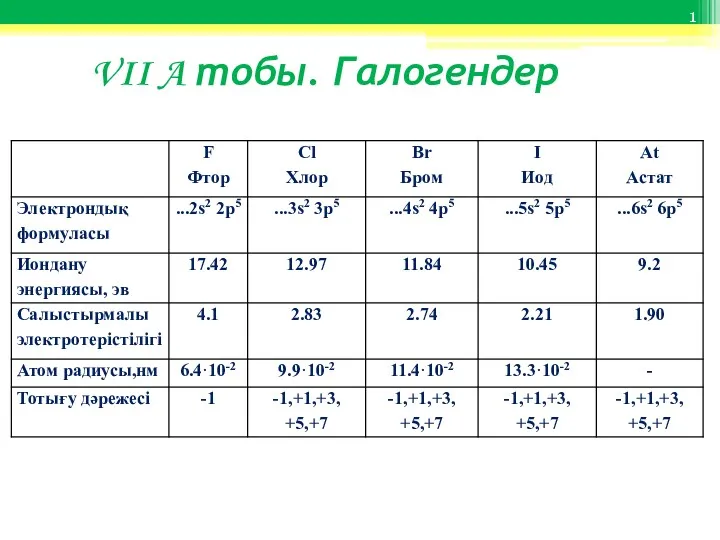 VII A тобы. Галогендер
VII A тобы. Галогендер Агрегатные состояния вещества
Агрегатные состояния вещества Технология производства бутилкаучука
Технология производства бутилкаучука Природные источники углеводородов, их переработка, применение и экологические проблемы. 10 класс
Природные источники углеводородов, их переработка, применение и экологические проблемы. 10 класс Разделение углеводородных газов
Разделение углеводородных газов Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов
Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов Будова електронних оболонок атомів
Будова електронних оболонок атомів Свойства химических элементов и закономерность их изменения
Свойства химических элементов и закономерность их изменения Значение органической химии в жизни человека
Значение органической химии в жизни человека Органічні сполуки (9 клас)
Органічні сполуки (9 клас) Майлардың анықтамасы
Майлардың анықтамасы Харчові добавки
Харчові добавки Реакции ионного обмена
Реакции ионного обмена Хімічні властивості оксидів
Хімічні властивості оксидів Колоїдний захист
Колоїдний захист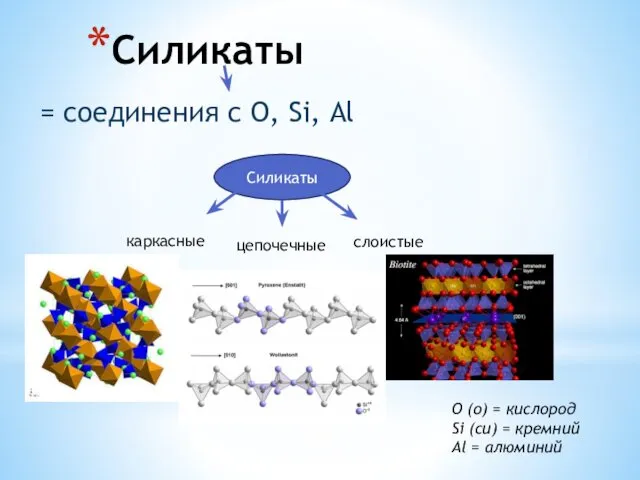 Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит
Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Вода на Земле. Строение молекулы воды
Вода на Земле. Строение молекулы воды