Содержание
- 3. Формы существования химического элемента
- 4. Из атомов мир создавала Природа. Два атома лёгких взяла водорода. Прибавила атом один кислорода. И получилась
- 5. Н2О Почему такой состав имеет молекула воды?
- 6. Задачи урока: 1. выяснить, от чего зависит состав сложных веществ; 2.что необходимо знать, чтобы составить формулы
- 7. Самостоятельная работа 1. Составьте: А) схемы строения атомов водорода и кислорода; Б) схему образования химической связи
- 8. 1.Как называется способность атомов образовывать связи с другими атомами? 2.Какие электроны называются валентными? 3. От чего
- 9. Выводы Число связей, в которых атом может принимать участие в молекуле называется валентностью. Валентные электроны расположены
- 10. Определите валентность элементов по структурной формуле. Внесите значение валентности элементов в таблицу. Валентность Степень окисления Н
- 11. Степень окисления Степень окисления (с.о.)- это условный заряд, который мог бы возникнуть на атоме при условии,
- 12. Сравнение понятий валентность и степень окисления Валентность Н I О II Са II Аl III С
- 13. Правила определения степеней окисления У свободных атомов и у простых веществ СТЕПЕНЬ ОКИСЛЕНИЯ равна 0 Металлы
- 14. Проверка задания 3 стр.55 1. Н20, Ва0, N20, S0, AI0, Cu0, F0 2. К2+1О, Ca+2CO3 ,
- 15. Определение степени окисления элементов в соединениях +3 х АlСl 3 (+3)*1 + х *3 = 0;
- 16. Задачи урока: 1. выяснить, от чего зависит состав сложных веществ; 2.что необходимо знать, чтобы составить формулы
- 17. Выводы: 1. Состав сложных веществ зависит от строения атомов, образующих вещества и возможности образовывать различные связи.
- 19. Скачать презентацию
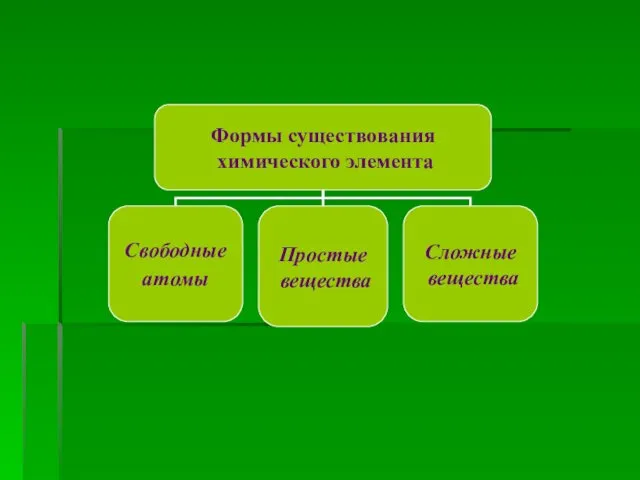
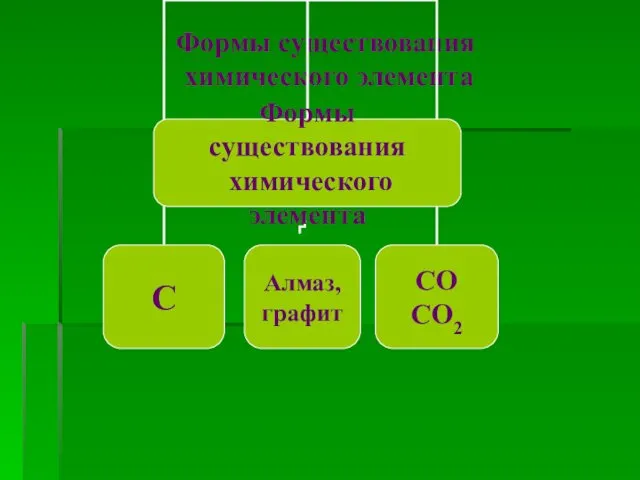














 Ковалентний зв’язок, його утворення
Ковалентний зв’язок, його утворення Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Неметаллы. Элементы V группы
Неметаллы. Элементы V группы Классификация химических реакций в неорганической химии
Классификация химических реакций в неорганической химии Как трудно быть особенной…
Как трудно быть особенной… Агрегатні стани речовини
Агрегатні стани речовини Масс-Спектроскопия
Масс-Спектроскопия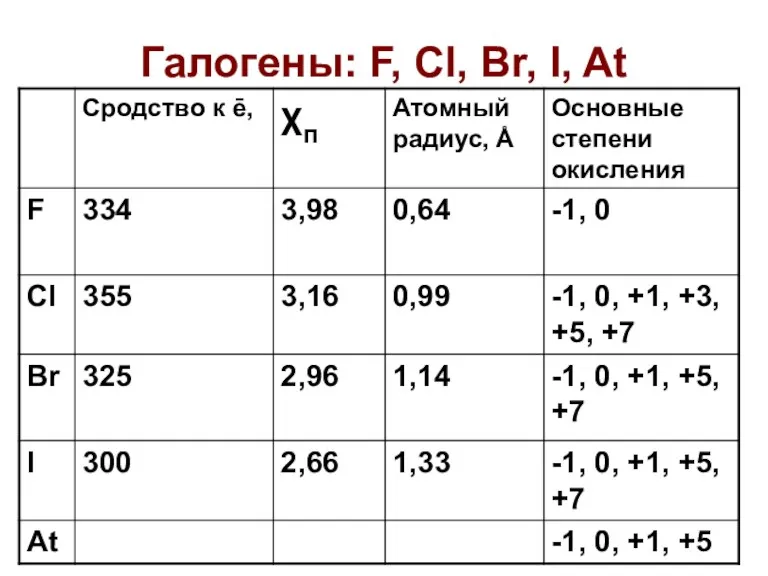 Галогены: F, Cl, Br, I, At
Галогены: F, Cl, Br, I, At Простые вещества – неметаллы. Аллотропия
Простые вещества – неметаллы. Аллотропия Кисень та хімічні властивості кисню. 7 клас
Кисень та хімічні властивості кисню. 7 клас Массовая доля химического элемента
Массовая доля химического элемента Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Дисперсные системы: общая характеристика и классификация
Дисперсные системы: общая характеристика и классификация Сернистый газ. Сернистая кислота и её соли
Сернистый газ. Сернистая кислота и её соли Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева Оксид фосфора(V). Ортофосфорная кислота и ее соли. Минеральные удобрения
Оксид фосфора(V). Ортофосфорная кислота и ее соли. Минеральные удобрения Багатоатомні насичені спирти. Фізичні та хімічні властивості
Багатоатомні насичені спирти. Фізичні та хімічні властивості Теория электролитической диссоциации
Теория электролитической диссоциации Алкены. Пропилен (пропен)
Алкены. Пропилен (пропен) Гидролиз солей
Гидролиз солей Ионоселективные электроды
Ионоселективные электроды Определение нефтепродуктов в воде с использованием Флюората-02-5М
Определение нефтепродуктов в воде с использованием Флюората-02-5М Тест по неорганической химии
Тест по неорганической химии Аммиак. 9 класс
Аммиак. 9 класс Железо и его свойства
Железо и его свойства Свойства природного газа
Свойства природного газа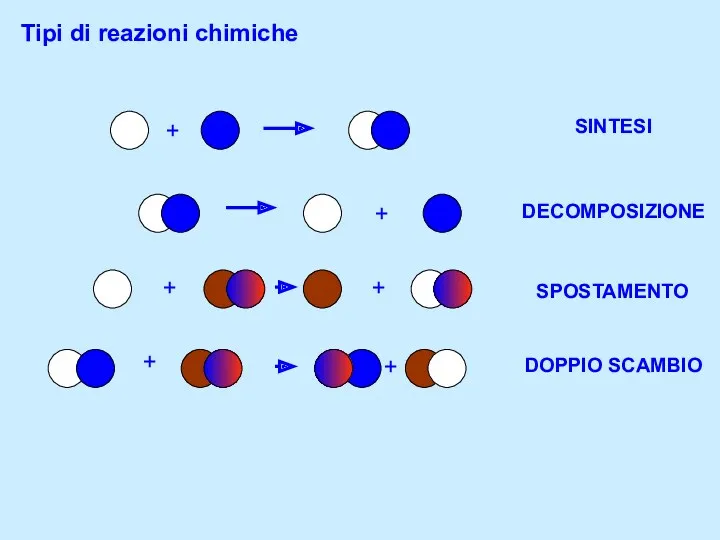 Tipi di reazioni chimiche
Tipi di reazioni chimiche Второй закон термодинамики. Биоэнергетика
Второй закон термодинамики. Биоэнергетика