Содержание
- 2. Оглавление: ВВЕДЕНИЕ КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ: По числу и составу реагирующих веществ и продуктов реакции По изменению
- 3. ВВЕДЕНИЕ Химические реакции – химические процессы, в результате которых из одних веществ образуются другие отличающиеся от
- 4. По числу и составу реагирующих веществ и продуктов реакции: Реакции, идущие без изменения состава веществ В
- 5. Аллотропия серы: S (ромбическая) S (пластическая) ОГЛАВЛЕНИЕ Классификация реакций
- 6. Аллотропия фосфора: Р (красный) Р (белый) ОГЛАВЛЕНИЕ
- 7. Реакции, идущие с изменением состава вещества Реакции соединения – это такие реакции, при которых из двух
- 8. Реакция соединения кислотного оксида фосфора(V) с водой: Р2 О5 + 3H2O = 2 H3PO4 ОГЛАВЛЕНИЕ Классификация
- 9. 2. Реакции разложения – это такие реакции, при которых из одного сложного вещества образуется несколько новых
- 10. Разложение перманганата калия при нагревании: Разгорание тлеющей лучины свидетельствует от том, что происходит выделение кислорода: 2KMnO4
- 11. 3. Реакции замещения – это такие реакции, в результате которых атомы простого вещества замещают атомы какого-нибудь
- 12. Взаимодействие щелочного металла натрия с водой: 2Na + 2H2O = 2NaOH + H2⭡ ОГЛАВЛЕНИЕ Классификация реакций
- 13. Взаимодействие щелочного металла кальция с водой: Са + 2Н2О = Са(ОН)2 + H2⭡ ОГЛАВЛЕНИЕ Классификация реакций
- 14. 4. Реакции обмена – это такие реакции, при которых два сложных вещества обмениваются своими составными частями
- 15. Взаимодействие сульфата хрома(III) с гидроксидом калия: Cr2(SO4)3 + 6KOH = 2Cr(OH)3 + 3K2SO4 ОГЛАВЛЕНИЕ Классификация реакций
- 16. 2. По изменению степеней окисления химических элементов, образующих вещества: Окислительно-восстановительные реакции: Окислительно-восстановительные реакции – реакции, идущие
- 17. Окислительно-восстановительная реакция: горение магния Сложные окислительно-восстановительные реакции составляются с помощью метода электронного баланса ОГЛАВЛЕНИЕ 0 0
- 18. Не окислительно-восстановительные реакции: К ним относятся все реакции ионного обмена, например: Na2CO3 + 2HCl = 2NaCl
- 19. 3. По участию катализатора: Катализаторы – это вещества, участвующие в химической реакции и изменяющие ее скорость
- 20. Каталитическая реакция взаимодействия алюминия с йодом: H2O 4Al + 3I2 ⭢ 2AlI3 ОГЛАВЛЕНИЕ Классификация реакций
- 21. 4. По агрегатному состоянию реагирующих веществ (фазовому составу): Гетерогенные реакции: Гетерогенные реакции – реакции, в которых
- 22. 5. По тепловому эффекту: Экзотермические реакции: Экзотермические реакции – реакции, протекающие с выделением энергии во внешнюю
- 23. Эндотермические реакции: Эндотермические реакции – реакции, протекающие с поглощением энергии во внешнюю среду. К ним относятся
- 24. 6. По направлению: Необратимые реакции: Необратимые реакции протекают в данных условиях только в одном направлении. К
- 26. Скачать презентацию






















 Кристаллические решетки
Кристаллические решетки Природные источники углеводородов
Природные источники углеводородов Щелочноземельные металлы
Щелочноземельные металлы NaHSO4. Гидросульфат натрия
NaHSO4. Гидросульфат натрия Получение пресной и чистой воды
Получение пресной и чистой воды Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Спирты
Спирты циклоалканы170
циклоалканы170 Напій кока-кола. Активні інгредієнти кока-коли
Напій кока-кола. Активні інгредієнти кока-коли Качественные реакции на органические вещества
Качественные реакции на органические вещества Властивості вуглеводів. Лабораторна робота 3
Властивості вуглеводів. Лабораторна робота 3 Амфотерные соединения
Амфотерные соединения Аспирин: польза или вред?
Аспирин: польза или вред? Опасности среды обитания человека
Опасности среды обитания человека Задачи и методы количественного анализа. Кислотно-основное титрование
Задачи и методы количественного анализа. Кислотно-основное титрование Күрделі эфирлер
Күрделі эфирлер Валентність хімічних елементів
Валентність хімічних елементів Сложные эфиры. Жиры
Сложные эфиры. Жиры Биоорганическая химия
Биоорганическая химия Основные классы неорганических соединений
Основные классы неорганических соединений Соляная кислота. Хлориды
Соляная кислота. Хлориды Конструкционные функциональные волокнистые композиты. Стеклопластики
Конструкционные функциональные волокнистые композиты. Стеклопластики Важнейшие оксиды в природе и жизни человека
Важнейшие оксиды в природе и жизни человека Химия нефти и газа. Переработка нефти
Химия нефти и газа. Переработка нефти Методы в химии
Методы в химии Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс
Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс Железо. Физические свойства
Железо. Физические свойства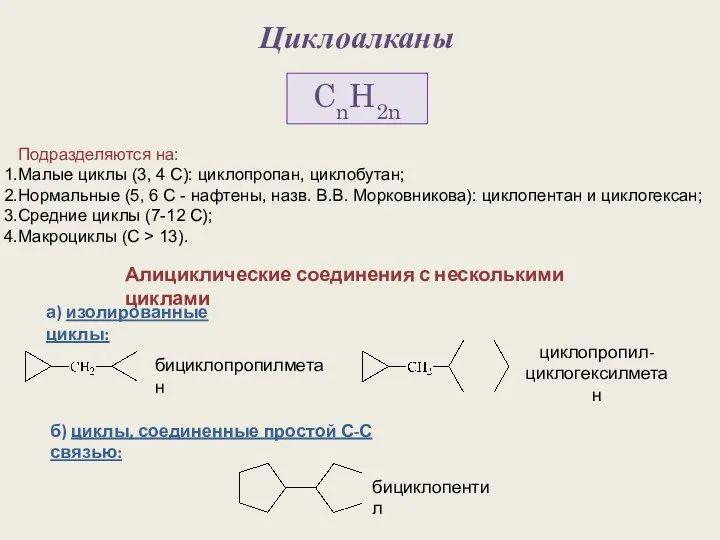 Циклоалканы. Строение алициклов
Циклоалканы. Строение алициклов