Слайд 2

Цели:
Обобщить и систематизировать знания о щелочноземельных металлах
Уметь характеризовать элементы по положению
в периодической таблице
Знать физические и химические свойства
применение соединений щелочноземельных металлов
Слайд 3

Положение в периодической таблице.
Строение атома
В периодической системе находятся в главной
подгруппе II группы.
Являются сильными восстановителями, отдают 2 ē, во всех
соединениях проявляют степень окисления +2.
Mg +12 2ē, 8ē, 2ē
Ca +20 2ē, 8ē, 8 ē, 2ē
Sr +38 2ē, 8ē, 18 ē, 8ē, 2ē
Ba +56 2ē, 8ē, 18 ē, 18 ē, 8ē, 2ē
Слайд 4

Физические свойства
цвет пламени þ t плавления
1,74г/см3 651 С0
1,54г/см3 851С0
2,63г/см3 770С0
3,76г/см3 710С0
Mg
Ca
Sr
Ba
Слайд 5
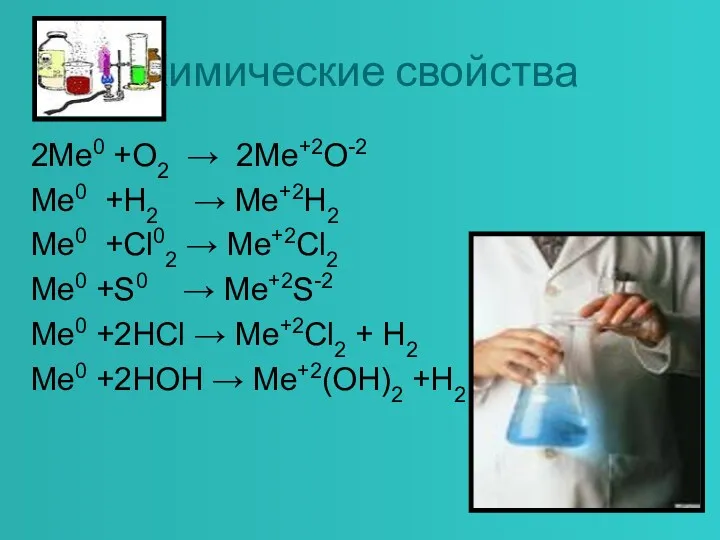
Химические свойства
2Me0 +O2 → 2Me+2O-2
Me0 +H2 → Me+2H2
Me0 +Cl02 → Me+2Cl2
Me0
+S0 → Me+2S-2
Me0 +2HCl → Me+2Cl2 + H2
Me0 +2HOH → Me+2(OH)2 +Н2
Слайд 6

Соединения щелочноземельных
металлов
Оксиды щелочноземельных металлов легко реагируют с оксидами неметаллов с
образованием соответствующих солей.
Слайд 7
BaSO4
Благодаря нерастворимости и способности задерживать рентгеновские лучи применяется в рентгенодиагностике
– баритовая каша.
Слайд 8

Ca3(PO4)2
Входит в состав фосфоритов и апатитов, а также в
состав костей и зубов. В организме взрослого человека содержится 1 кг Са в виде фосфата кальция.
Слайд 9

CaCO3
Карбонат кальция – одно из самых распространённых на Земле соединений.
Его содержат горные породы – мел, мрамор, известняк.
Слайд 10

CaSO4∙ 2H2O
Встречается в природе в виде минерала гипса, представляющего
собой кристаллогидрат. Используется в строительстве, в медицине для наложения гипсовых повязок, для получения слепков.
Слайд 11

MgCO3
Широко применяется в производстве стекла, цемента, кирпича, а также в
металлургии для перевода пустой породы в шлак.
Слайд 12

Са(ОН)2
Гидроксид кальция или гашёная известь с песком и водой называется
известковым раствором и широко используется в строительстве. При нагревании разлагается на оксид и воду.
Слайд 13

Проверка знаний
Сравните атомы элементов, поставив знаки <, > или =
вместо *:
а) заряд ядра: Mg * Ca, Na *Mg, Ca * К;
б) число электронных слоев: Mg * Ca, Na * Mg,
Ca * К;
в) число электронов на внешнем уровне: Mg * Ca, Na *Mg, Ca * К;
г) радиус атома: Mg * Ca, Na * Mg, Ca * K;
д) восстановительные свойства: Mg * Ca, Na * Mg,
Ca * K.
Слайд 14

Проверь себя
(самостоятельная работа )
Дополните схемы взаимодействия щелочноземельных
металлов с неметаллами общими формулами и названиями продуктов реакции.
Запишите конкретные уравнения реакции, расставив коэффициенты в них методом электронного баланса:
а) М+ S ____________ б) М+ N2 ____________________________
в) М+ Н 2 _____________ г) М+ С12 ___________________
Пример: ___________________ Пример: _________________________
Допишите уравнения реакций:
а) Са + H2O→ ……………………….
б) Mg + НСl→……………………….
в) Ва + О2→………………………..
Осуществить превращения по схеме:
Ме → МеО → Ме(ОН)2 → МеSО4
Слайд 15

Домашнее задание:
§ 12. упр. № 5, 8
Написать уравнения реакций с помощью
которых можно осуществить два любых превращения из составленных учащимися на уроке.














 Химические свойства металлов
Химические свойства металлов Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? d-элементы
d-элементы Подготовка к ВПР по химии. 11 класс
Подготовка к ВПР по химии. 11 класс Метаболизм кетоновых тел. Метаболизм холестерина
Метаболизм кетоновых тел. Метаболизм холестерина Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия Кислотные дожди
Кислотные дожди The Molecules of Life
The Molecules of Life Цинк и его соединения
Цинк и его соединения Фосфор и его соединения
Фосфор и его соединения Химия воды
Химия воды Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Классификация химических элементов
Классификация химических элементов Способы выражения состава раствора. Задача 7
Способы выражения состава раствора. Задача 7 НЮ 2.1.1. Металлы - общая характеристика
НЮ 2.1.1. Металлы - общая характеристика Гониометрическое исследование кристаллов
Гониометрическое исследование кристаллов Сплавы железа с углеродом: стали и чугуны
Сплавы железа с углеродом: стали и чугуны Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування
Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування Мінерали та гірські породи
Мінерали та гірські породи Серная кислота
Серная кислота Electrolysis
Electrolysis Вещества
Вещества Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Аминокислоты 2
Аминокислоты 2 Метаболизм углеводов
Метаболизм углеводов Спектральные методы: атомная спектроскопия
Спектральные методы: атомная спектроскопия Валентность и степень окисления. Химическая связь
Валентность и степень окисления. Химическая связь Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості
Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості