Реакційна здатність насичених вуглеводнів. Реакційна здатність ненасичених вуглеводнів (алкени, алкадієни, алкіни) презентация
Содержание
- 2. Вуглеводні: аліфатичні та аліциклічні Назва класу вуглеводню Загальна формула Тип гібридизації атома Карбону Основний тип реакції
- 3. Насичені вуглеводні
- 4. Алкани
- 5. Вуглеводні: номенклатура та ізомерія 3,5-диметил-3-етил-октан метилетилізопропілметан (2,3-диметилпентан)
- 6. Вуглеводні: номенклатура та ізомерія 2-етилпентен-1 пентадієн-1,3 2-метилбутадієн (ізопрен) етеніл (вініл) 2-пропеніл (аліл)
- 7. Вуглеводні: номенклатура та ізомерія 3-метилбутин-1 1-фенілпропін (метилфенілацетилен) етиніл пропаргіл
- 8. Вуглеводні: номенклатура та ізомерія Структурна ізомерія С5Н12 пентан Ткип= 36.2°С 2-метилбутан Ткип= 28°С 2,2-диметилпропан Ткип= 9.5°С
- 9. Алкани. Номенклатура 2,2,4-триметилпентан Первинний Вторинний Третинний Четвертинний
- 10. Вуглеводні: номенклатура та ізомерія Структурна ізомерія
- 11. Вуглеводні: номенклатура та ізомерія Просторова ізомерія цис-бутен-2 Ткип=4°С транс-бутен-2 Ткип=1°С
- 12. Вуглеводні: номенклатура та ізомерія (Е)-1-бром-1-нітро- 2-хлорпропен (Z)-1-бром-1-нітро- 2-хлорпропен
- 13. 3-метилбутин-1 пентин-1 пентин-2 Вуглеводні: номенклатура та ізомерія Структурна ізомерія
- 14. Вуглеводні: будова молекул Алкани Алкени
- 15. Вуглеводні: будова молекул Алкадієни
- 16. Вуглеводні: будова молекул Алкіни
- 17. Методи одержання алканів Лабораторні: 1. Лужне плавлення (синтез Дюма) RCOONa + NaOH R–H + Na2CO3 Наприклад,
- 18. 4. Реакція Кольбе (електроліз) RCOONa ⇔ RCOO– + Na+ RCOO– – 1е → R∙ + СО2
- 19. 3. Реакція В’юрца–Шоригіна: R–Hal + 2Na + Hal–R → 2NaHal + R–R Механізм: R–Hal + 2Na
- 20. 5. Гідрування алкенів та алкінів: СН3–С≡С–СН3 + Н2 СН3–СН=СН–СН3 + Н2 СН3–СН2–СН2–СН3 6. Крекінг алканів –
- 21. Алкани. Хімічні властивості Галогенування
- 22. Хімічні властивості: алкани Галогенування
- 23. Алкани. Хімічні властивості Галогенування (Механізм реакції) Ініціювання Ріст ланцюга
- 24. Алкани. Хімічні властивості Галогенування (Механізм реакції) Обрив ланцюга
- 25. Алкани. Хімічні властивості Галогенування (Механізм реакції) 1.Галогенування розпочинається тільки під дією ініціатора радикальних реакцій (УФ-світло, радикальні
- 26. Алкани. Хімічні властивості Галогенування (Механізм реакції) 4. Реакційна здатність Гідрогену у третинного атома Карбону вища, ніж
- 27. Алкани. Хімічні властивості Сульфохлорування С10H22 + SO2 + Cl2 → C10H21SO2Cl + HCl декан сульфохлорид декану
- 28. Хімічні властивості: алкани Нітрування Реакція М.І. Коновалова
- 29. Алкани. Хімічні властивості Термічний розклад (Крекінг) В.Г. Шухов (1891) Температура – 470—650°С; Тиск – 7 МПа
- 30. Алкани. Хімічні властивості Ізомеризація
- 31. Алкани. Хімічні властивості Окислення Сильні окисники (KMnO4, K2Cr2O7 і ін.)
- 32. Велику групу циклоалканів складають біциклічні сполуки, які бувають з роз’єднаними циклами, з безпосередньо сполученими одинарними С–С
- 33. Спіранові сполуки містять спільний (вузловий) атом Карбону для двох циклів. Їх назва починається з префікса спіро-,
- 34. Місткові сполуки містять два вузлових атоми Карбону. Їх назва починається з префікса біцикло-. Далі в квадратних
- 35. Структурна ізомерія залежить від величини циклу, природи зімсника, їх взаємного розташування і поділяється на такі види:
- 36. Енантіомерія аліциклічних сполук виникає при наявності хірального атома Карбону і відсутності елементів симетрії, в першу чергу
- 37. Конформаційна ізомерія циклоалканів пов’язана з особливостями їх будови. Передумовою сучасного трактування будови циклічних сполук була теорія
- 38. Конформаційна ізомерія циклоалканів Подальшим розвитком теоретичних уявлень будови циклоалканів була теорія конформаційного аналізу К. Пітцера (1947
- 39. При наявності об’ємних замісників найбільш вигдною є конформація, коли вони займають екваторіальне положення (прояв внутрішньомолекулярних вандерваальсівських
- 40. На відміну від усіх інших циклоалканів, циклопропан має плоский вуглецевий скелет. В циклопропані наявне значне кутове
- 41. Хімічні властивості циклоалканів: реакції приєднання
- 42. Хімічні властивості: реакції приєднання Хімічні властивості: реакції окиснення
- 43. Хімічні властивості: реакції заміщення
- 44. Ненасичені вуглеводні Алкенами называют алифатические углеводороды, содержащие двойную углерод -углеродную связь.
- 45. Хімічні властивості: алкени, алкадієни та алкіни Реакції електрофільного приєднання. Правило Марковникова
- 46. Хімічні властивості: алкени, алкадієни та алкіни Реакції електрофільного приєднання. Правило Марковникова
- 47. Хімічні властивості: алкени, алкадієни та алкіни Реакції електрофільного приєднання. Правило Марковникова
- 48. Химические свойства алкадиенов Гидрирование
- 49. Химические свойства алкадиенов Реакция Дильса-Альдера (диеновый синтез) Полимеризация
- 50. Хімічні властивості: алкени, алкадієни та алкіни Реакції електрофільного приєднання. Правило Марковникова
- 51. Механізм реакції електрофільного приєднання АЕ циклічний йон бромонію рz-орбіталь π-комплекс
- 52. Гидратация (реакция Кучерова) Хімічні властивості алкінів
- 53. Реакции замещения алкинов Образование ацетиленидов
- 54. Химические свойства алкинов Реакции окисления и восстановления Окисление алкинов Востановление алкинов
- 55. Химические свойства алкинов Димеризация, тримеризация и тетрамеризация
- 57. Скачать презентацию
 Введение в коллоидную химию. Основные понятия и закономерности
Введение в коллоидную химию. Основные понятия и закономерности Природный газ и нефть
Природный газ и нефть Хімічні властивості оксидів
Хімічні властивості оксидів Цеолиты. Свойства и область применения
Цеолиты. Свойства и область применения Получение и приминение этилена
Получение и приминение этилена Органическая химия
Органическая химия Непредельные углеводороды. Этилен и его гомологи
Непредельные углеводороды. Этилен и его гомологи Гидролиз. Применение гидролиза. (11 класс)
Гидролиз. Применение гидролиза. (11 класс) Вчення про розчини. Рівновага в розчинах електролітів
Вчення про розчини. Рівновага в розчинах електролітів Камень чароит
Камень чароит Основания, их классификация и свойства
Основания, их классификация и свойства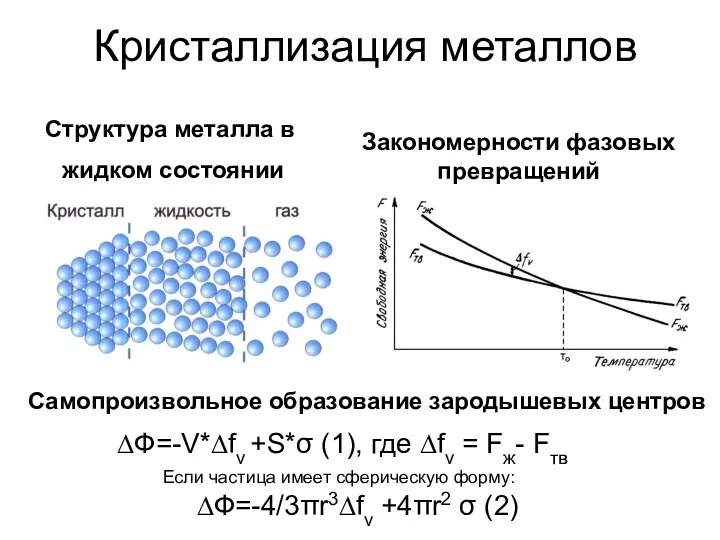 Закономерности фазовых превращений
Закономерности фазовых превращений Подготовка к ГИА. А9. Химические свойства простых веществ: металлов и неметаллов
Подготовка к ГИА. А9. Химические свойства простых веществ: металлов и неметаллов Азотжәне Фосфорэлементтерін салыстырыңдар,мәліметтерді кестеге толтырыңдар
Азотжәне Фосфорэлементтерін салыстырыңдар,мәліметтерді кестеге толтырыңдар Мыло
Мыло Создание косметических средств
Создание косметических средств Соли Mg SO4 – сульфат магния
Соли Mg SO4 – сульфат магния Отримання кисню. Властивості кисню
Отримання кисню. Властивості кисню Вода. 8 класс
Вода. 8 класс Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Цветные металлы
Цветные металлы Алюминий. Схема расположения электронов на энергетических подуровнях
Алюминий. Схема расположения электронов на энергетических подуровнях Контрольная работа по дисциплине: химия
Контрольная работа по дисциплине: химия Нитраты в овощах и фруктах
Нитраты в овощах и фруктах Химия как компонент системы естественнонаучного образования
Химия как компонент системы естественнонаучного образования Карбоновые кислоты
Карбоновые кислоты Хімічні явища в побуті
Хімічні явища в побуті Живая» и «мёртвая» вода
Живая» и «мёртвая» вода