Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций презентация
Содержание
- 2. Стоимость каждой из РЗ (РЗ-2 и РЗ-3) составляет 100б. В этой части курса (электрохимической) максимально можно
- 3. Литература 1. Дамаскин Б.Б., Петрий О.А., Цирлина Г.А.- Электрохимия: Учебник для вузов - 2-е изд.,испр. и
- 4. План Химическая и электрическая работа систем с химическими реакциями. Специальные устройства для проведения и изучения электрохимических
- 5. 7. Электрический ток в проводниках. Плотность тока. Уравнение неразрывности. Закон Ома для плотности тока. Удельная проводимость,
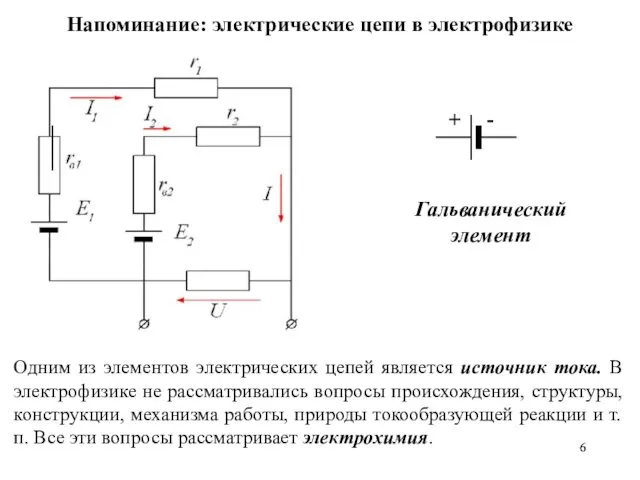
- 6. Напоминание: электрические цепи в электрофизике Одним из элементов электрических цепей является источник тока. В электрофизике не
- 7. Термин «электрохимия» объединяет два вида явлений: электрические и химические. Проявление этих различий рассмотрим на примере проведения
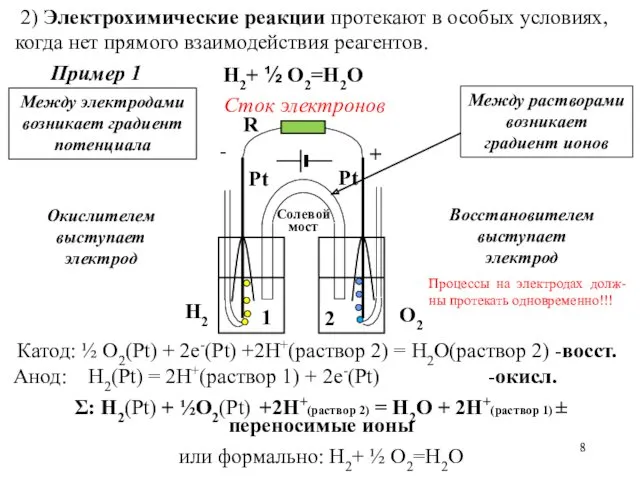
- 8. 2) Электрохимические реакции протекают в особых условиях, когда нет прямого взаимодействия реагентов. Между электродами возникает градиент
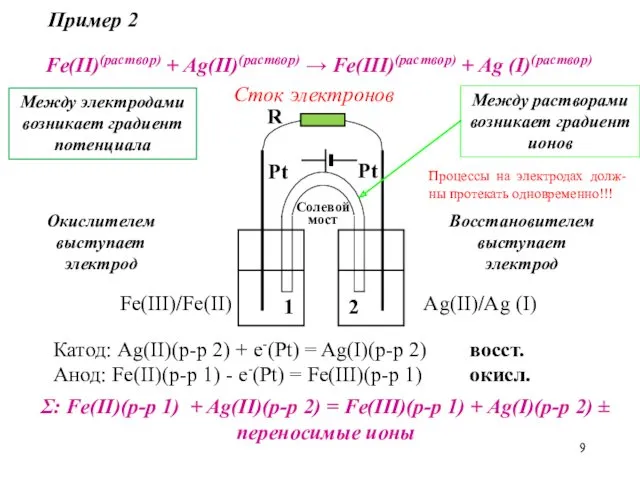
- 9. Fe(II)(раствор) + Ag(II)(раствор) → Fe(III)(раствор) + Ag (I)(раствор) Fe(III)/Fe(II) Ag(II)/Ag (I) Катод: Ag(II)(р-р 2) + e-(Pt)
- 10. Формальная запись гальванических элементов отображается в следующем виде: − Pt⎪(H2)⎪H+ (раствор 1)║H+ (раствор 2)⎪(O2)⎪Pt + 2)
- 11. Гальванический элемент – это устройство, в котором в определенном порядке сочетаются проводники первого и второго рода.
- 12. Удельные электропроводности некоторых веществ Металлы, æ, См·м-1 Серебро 6,7 ·107 Медь 6,45 ·107 Свинец 5,6·107 Растворители,
- 13. Первый гальванический элемент, изобретенный А. Вольта
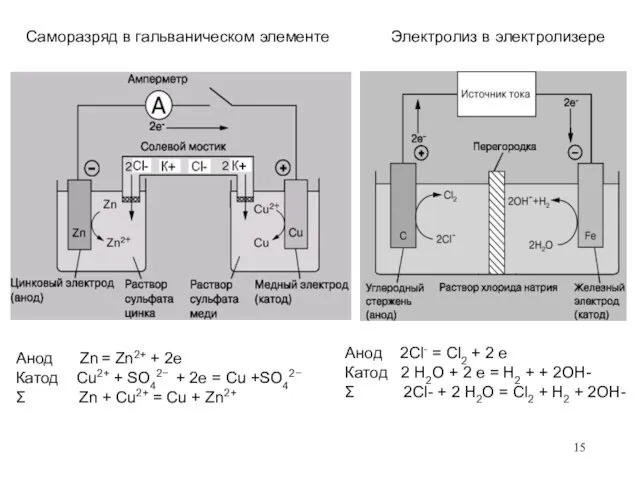
- 14. При наложении на электролитическую ячейку внешнего источника тока - электролиз: Примеры процесса в электролизере: + Pt⎪CuCl2
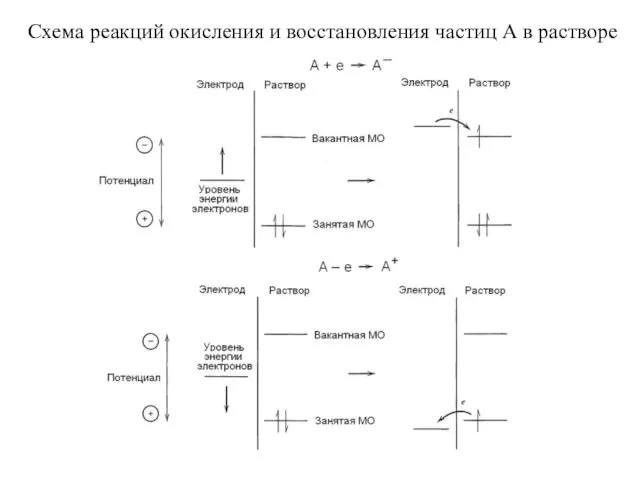
- 17. Схема реакций окисления и восстановления частиц А в растворе
- 18. Энергетическая проблема – главная современная проблема человечества. Химические источники тока (ХИТ) Первичные (после использования выбрасывают) -
- 19. - щелочные железо- или кадмий-никелевый Fe (или Cd) | KOH | NiOOH | Ni; Е =
- 20. 3) Электрохимические генераторы (топливные элементы) Преимущество – прямое получение электрической энергии без промежуточного образования тепловой энергии.
- 21. Равновесные и неравновесные системы Равновесные системы. Критерий равновесия в ГЦ - обратимость химического процесса. Измерения Е
- 22. Некоторые вопросы к функционированию гальванических элементов: Где и как возникает градиент потенциала в гальваническом элементе? Что
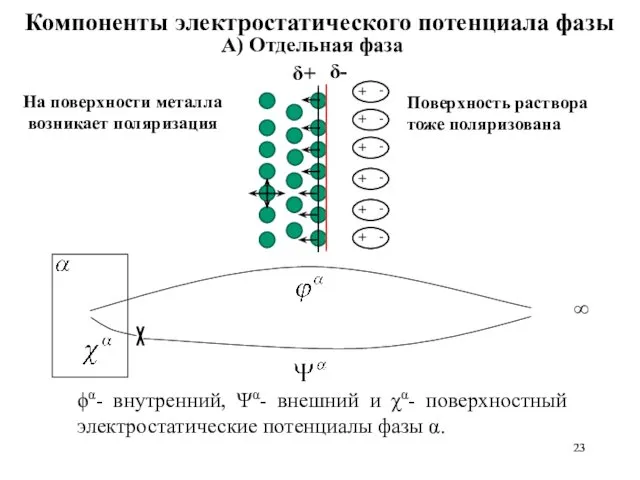
- 23. ϕα- внутренний, Ψα- внешний и χα- поверхностный электростатические потенциалы фазы α.
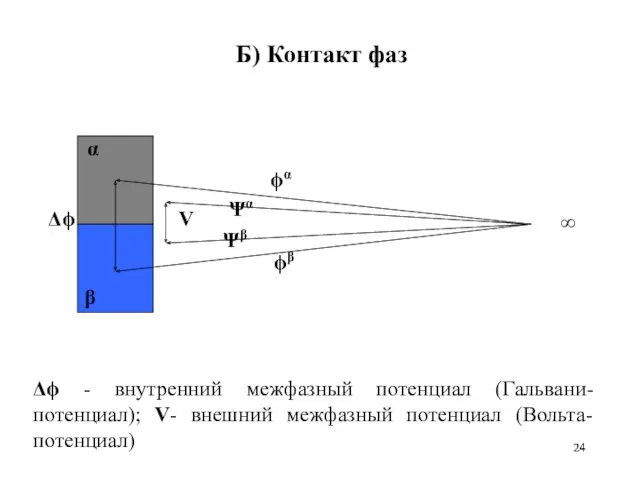
- 24. Б) Контакт фаз Δϕ - внутренний межфазный потенциал (Гальвани-потенциал); V- внешний межфазный потенциал (Вольта-потенциал)
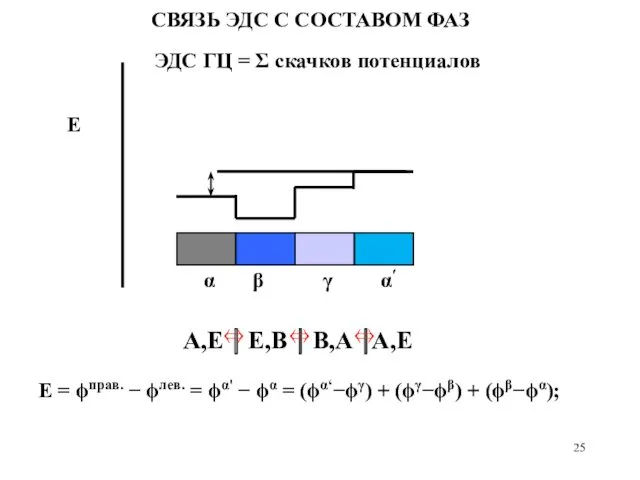
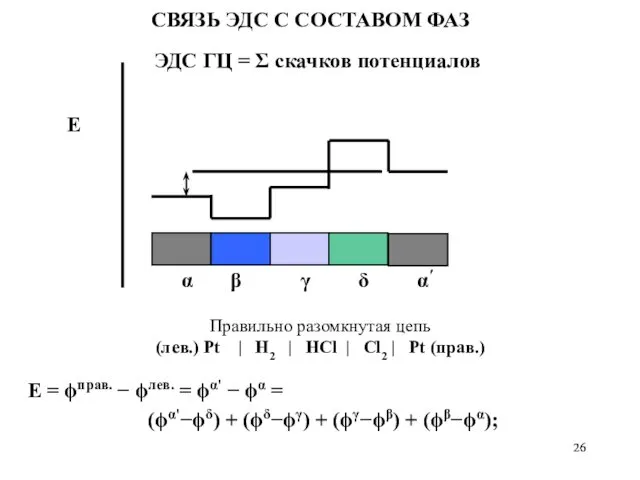
- 25. СВЯЗЬ ЭДС С СОСТАВОМ ФАЗ ЭДС ГЦ = Σ скачков потенциалов E Е = ϕправ. −
- 26. Правильно разомкнутая цепь (лев.) Pt | H2 | HCl | Cl2 | Pt (прав.) СВЯЗЬ ЭДС
- 27. Электрохимический потенциал компонента фазы: заряженный незаряженный
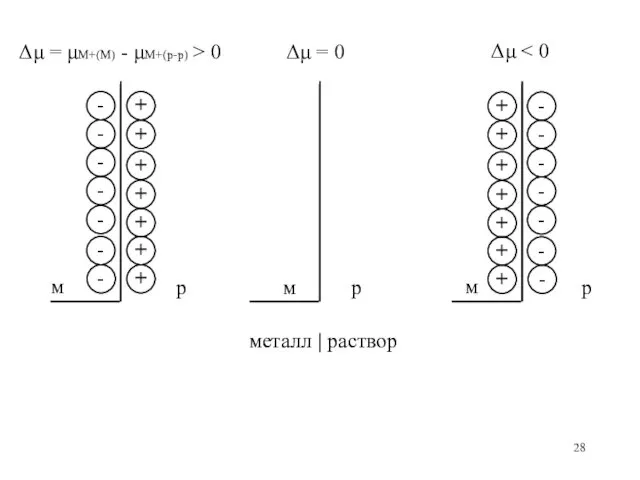
- 28. Δμ = μM+(M) - μM+(p-p) > 0 Δμ = 0 Δμ металл | раствор м м
- 30. Скачать презентацию

















 Алкадиены
Алкадиены Химиялық қауіптілер. Нитраттар
Химиялық қауіптілер. Нитраттар Неорганические полимеры
Неорганические полимеры Камни и Телец
Камни и Телец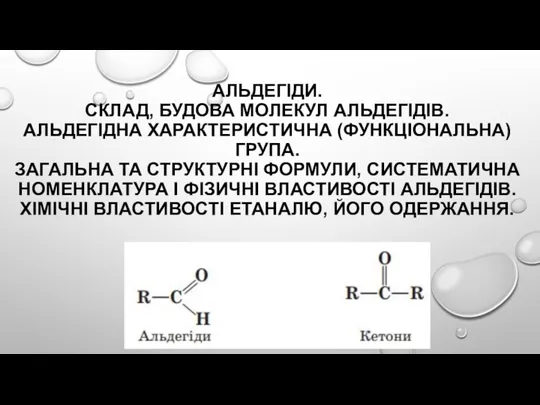 Альдегіди. Склад, будова молекул альдегідів. Альдегідна характеристична (функціональна) група
Альдегіди. Склад, будова молекул альдегідів. Альдегідна характеристична (функціональна) група Металдар коррозиясы және онымен күресу шаралары
Металдар коррозиясы және онымен күресу шаралары Введение в токсикологическую химию. Объекты химико-токсикологического исследования
Введение в токсикологическую химию. Объекты химико-токсикологического исследования Скорость химической реакции
Скорость химической реакции Азотные удобрения
Азотные удобрения Кислоты. Состав кислот
Кислоты. Состав кислот Значення хімічних процесів у природі
Значення хімічних процесів у природі Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Чистые вещества и смеси. 8 класс
Чистые вещества и смеси. 8 класс Теплові прояви механічної, електричної та хімічної енергії
Теплові прояви механічної, електричної та хімічної енергії Железо и его соединения
Железо и его соединения Гигиена труда при работе с пестицидами и минеральными удобрениями
Гигиена труда при работе с пестицидами и минеральными удобрениями Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Історія хімії
Історія хімії Магний. Нахождение в природе
Магний. Нахождение в природе Железо. Строение атома, физические и химические свойства простого вещества
Железо. Строение атома, физические и химические свойства простого вещества Основы коррозии и защиты металлов. Опасность локальных видов коррозии
Основы коррозии и защиты металлов. Опасность локальных видов коррозии Обзор уникальных свойств и областей применения магнитных жидкостей. Получение ферромагнитной жидкости
Обзор уникальных свойств и областей применения магнитных жидкостей. Получение ферромагнитной жидкости Анализ лекарственных средств паминофенола, ароматических кислот: бензойная кислота, натрия бензоат, салициловая кислота
Анализ лекарственных средств паминофенола, ароматических кислот: бензойная кислота, натрия бензоат, салициловая кислота Минерал чароит. Месторождения
Минерал чароит. Месторождения Основные физико-химические свойства нефтей и нефтепродуктов
Основные физико-химические свойства нефтей и нефтепродуктов Элементы химической термодинамики
Элементы химической термодинамики Свойства растворов и гетерогенных систем
Свойства растворов и гетерогенных систем Алюминий AL- химический элемент
Алюминий AL- химический элемент