Содержание
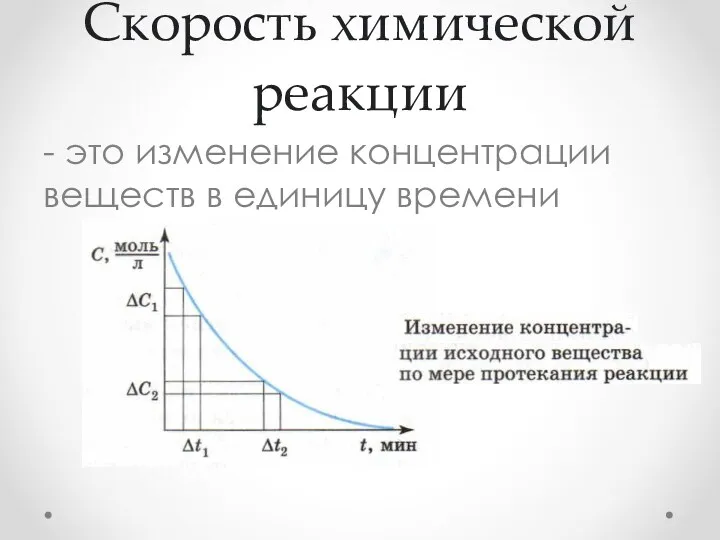
- 2. Скорость химической реакции - это изменение концентрации веществ в единицу времени
- 3. Если химические реакции происходят в однородной среде, например в растворе или в газовой фазе, то взаимодействие
- 4. Если реакция идет между веществами, находящимися в разных агрегатных состояниях (например, между твердым веществом и газом
- 5. 1. Влияние природы реагирующих веществ Zn + 2HCl = ZnCl2+H2(г) Zn + 2 CH3COOH = (CH3COO)2Zn
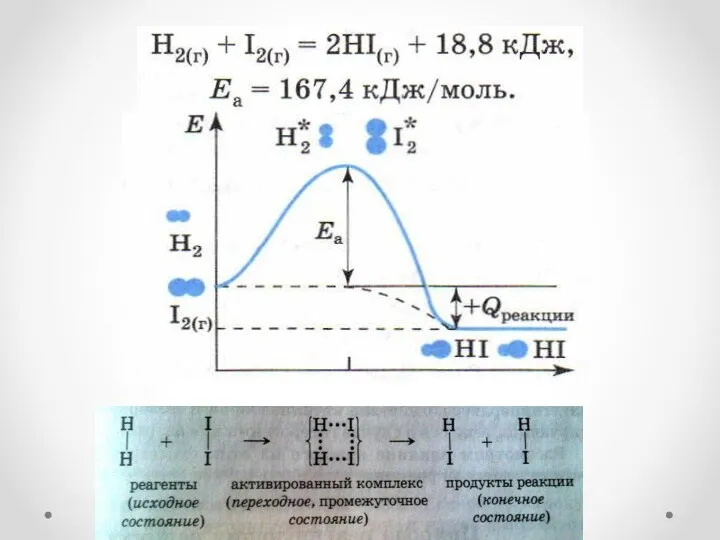
- 6. Энергия активации. Еа Минимальный избыток энергии, который должна иметь частица(или пара частиц), что бы произошло эффективное
- 8. 2. Влияние концентрации N2(г) + 3H2(г) = 2NH3(г) v = k ∙ [N2] ∙[H2]3 Основной закон
- 9. 3. Влияние температуры Правило Я. Х. Вант-Гоффа: Повышение температуры на каждые 10 ˚С приводит к увеличению
- 10. Задача Во сколько раз изменится скорость химической реакции 2А + 2В = С, если температуру смеси
- 11. Задача 2 Атмосферные загрязнения постепенно уничтожают защитный озоновый слой Земли. Озоновому слою угрожают поступающие в атмосферу
- 12. Решение Запишем уравнение реакции и условие задачи в формульном виде: . Cl + O3 = .
- 13. Задача 3 Диоксид серы - самый распространенный загрязнитель воздуха. Он опасен для здоровья людей, особенно тех,
- 14. Решение: Запишем уравнение реакции и условие задачи в формульном виде: . O + SO2 = SO3
- 15. Задача 4 Важнейшие источники восполнения запаса кислорода в атмосфере - это диоксид углерода и вода. Часть
- 16. Решение: Запишем уравнение реакции и условие задачи в формульном виде: 2 ( . OH) = 2
- 18. Скачать презентацию













 Хром
Хром Металлы. Лекция № 9
Металлы. Лекция № 9 Решение упражнений по теме: Углеводы
Решение упражнений по теме: Углеводы Контрольная работа. Разбор. 9 класс
Контрольная работа. Разбор. 9 класс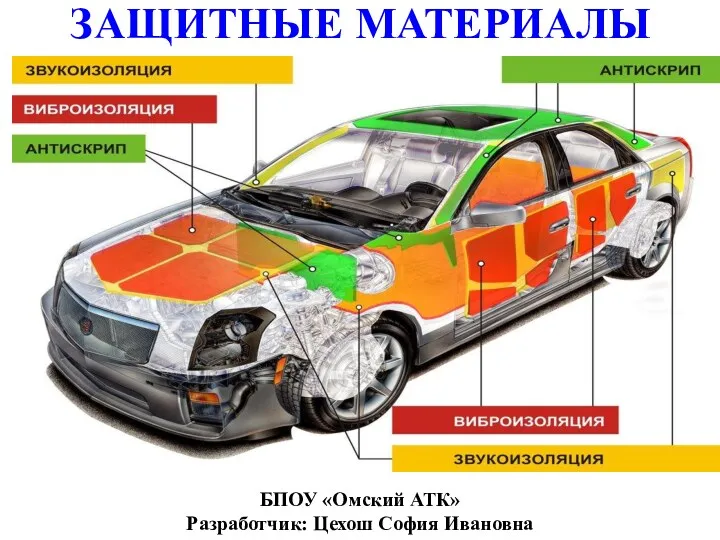 Защитные материалы
Защитные материалы Магнитные наночастицы: проблемы и достижения
Магнитные наночастицы: проблемы и достижения Кислотно-основные равновесия в водном растворе. Буферные растворы. (Лекция 3)
Кислотно-основные равновесия в водном растворе. Буферные растворы. (Лекция 3) Палладий. История открытия химических веществ
Палладий. История открытия химических веществ Общая характеристика неметаллов
Общая характеристика неметаллов Аммиак. Строение, свойства, получение, применение
Аммиак. Строение, свойства, получение, применение Оксиды. Понятия об оксидах
Оксиды. Понятия об оксидах Путешествие на остров Соединений химических элементов. Урок-игра
Путешествие на остров Соединений химических элементов. Урок-игра Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул
Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул Алюминий и его соединения
Алюминий и его соединения Растворы. (Лекция 7)
Растворы. (Лекция 7) Химические методы определения U, Pu, Th
Химические методы определения U, Pu, Th Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Химическое равновесие
Химическое равновесие d997-13229e5e
d997-13229e5e Типы химических реакций
Типы химических реакций Методы выделения и очистки продуктов биотехнологических производств
Методы выделения и очистки продуктов биотехнологических производств Соли аммония
Соли аммония Минералогический состав почв
Минералогический состав почв Physical chemistry of nanostructured systems
Physical chemistry of nanostructured systems Азотсодержащие органические соединения
Азотсодержащие органические соединения История развитии химии
История развитии химии Objectives and background. Apply for an unknown mixture
Objectives and background. Apply for an unknown mixture Аллотропные модификации кремния
Аллотропные модификации кремния