Слайд 2

О железе
Железо – не только основа всего мира, самый главный
элемент
окружающей нас природы. Оно основа культуры и промышленности.
Оно орудие войны и мирного труда, и во всей таблице Менделеева
невозможно найти другой такой элемент , который был бы так связан с
прошлыми, настоящими и будущими судьбами человечества.
академик Ферсман А.Е.
Слайд 3

Немного истории
В середине II тысячелетия до н.э. в Египте была основана
металлургия железа – получение его из железных руд. Это положило начало железному веку в истории человечества.
Слайд 4

Слайд 5
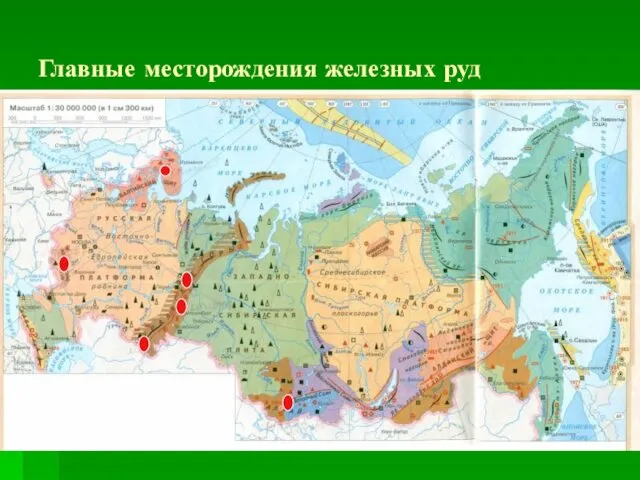
Главные месторождения железных руд
Слайд 6

Слайд 7

Железо – d-элемент.
Порядковый номер
26
Относительная атомная масса
55,847
Валентность переменная
II-III
Слайд 8

Физические свойства железа
Плотность=7,87 г/см3
Тпл = 1539ْ С
Ткип = 3200ْ С
Намагничивается
Легко обрабатывается: режется, прокатывается,
куётся
Слайд 9

Химические свойства железа
Металл средней активности
в концентрированных серной и азотной кислотах пассивируется
Слайд 10

Железо реагирует :
С простыми веществами:
Fe + S = FeS
2Fe + 3Cl2
= 2FeCl3
3Fe + 2O2 = Fe3O4 (FeO*Fe2O3)
Со сложными веществами:
3Fe + 4H2O = Fe3O4 +4H2
Fe + 2HCl = FeCl2 + H2
Fe + CuSO4 = FeSO4 + Cu
Слайд 11

Коррозия металла
Железо разрушается под действием окружающей среды – оно ржавеет
4Fe +
3O2 + 2n·H2O = 2Fe2O3·nH2 O
Состав ржавчины очень сложный
Слайд 12

Защита железа от коррозии
Лако-красочные покрытия
Эмаль – силикатное стекло с добавлением оксидов
металлов
Металлические покрытия: лужение, оцинковывание, хромирование и т.д.
Выплавление нержавеющих сталей
Ингибирование
Слайд 13

Соединения железа
FeO →Fe(OH)2 – основные соединения
FeO + H2SO4 = FeSO4
+H2O
Fe2O3 → Fe(OH)3 – амфотерные соединения
Fe(OH)3 + NaOH =t Na[Fe(OH)4]
Слайд 14

Качественные реакции
На ион Fe2+ - взаимодействие с красной кровяной солью гексацианоферратом
(III)калия
Fe+2SO4+K3[Fe(CN)6]=KFe+3[Fe+2(CN)6]↓+K2SO4
синего цвета
На ион Fe3+–взаимодействие с роданидом аммония
Fe+3CI3+3NH4SCN↔Fe(SCN)3↓+3NH4CI
кроваво-красного
цвета













 Теория химического строения органических соединений
Теория химического строения органических соединений Plastic is one of the challenges of the 21st century
Plastic is one of the challenges of the 21st century Непредельные углеводороды ряда этилена. Олефины
Непредельные углеводороды ряда этилена. Олефины Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Фазовые равновесия в растворах
Фазовые равновесия в растворах Сера. Аллотропные модификации
Сера. Аллотропные модификации Carbohydrates and their metabolism. Digestion of carbohydrates
Carbohydrates and their metabolism. Digestion of carbohydrates Правила работы в лаборатории и приёмы обращения с лабораторным оборудованием (8 класс)
Правила работы в лаборатории и приёмы обращения с лабораторным оборудованием (8 класс) Химическая связь
Химическая связь Термическая и химико-термическая обработка
Термическая и химико-термическая обработка Обчислення за хімічними рівняннями відносного виходу продукту реакції. Урок №19. 11 клас
Обчислення за хімічними рівняннями відносного виходу продукту реакції. Урок №19. 11 клас Методические подходы к решению химических задач. Задание 34
Методические подходы к решению химических задач. Задание 34 Методика обучения решению задач на соотношение атомов в школьном курсе химии
Методика обучения решению задач на соотношение атомов в школьном курсе химии Химические уравнения
Химические уравнения Аммиак
Аммиак Техника безопасности в кабинете химии
Техника безопасности в кабинете химии Виды камней
Виды камней Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение Соли. 11 класс
Соли. 11 класс CaSO4 кристаллының ас жазықтығына проекциясының құрылымдық моделі
CaSO4 кристаллының ас жазықтығына проекциясының құрылымдық моделі Обмен жиров в организме
Обмен жиров в организме Введение в органическую химию
Введение в органическую химию Фосфор и его соединения. Урок по химии для 9 класса
Фосфор и его соединения. Урок по химии для 9 класса Электролиттік диссоциациялану теориясы тұрғысынан қышқыл, негіз, тұздардың химиялық қасиеттері
Электролиттік диссоциациялану теориясы тұрғысынан қышқыл, негіз, тұздардың химиялық қасиеттері Элементы группы галогенов
Элементы группы галогенов Кислород, его характеристика, получение и свойства
Кислород, его характеристика, получение и свойства Спирти. 3агальна характеристика спиртів
Спирти. 3агальна характеристика спиртів Щелочи
Щелочи