Содержание
- 2. Понятие об алкенах Алкены – углеводороды, содержащие в молекуле одну двойную связь между атомами углерода, а
- 3. Характеристика двойной связи (С ═ С) Вид гибридизации – Валентный угол – Длина связи С =
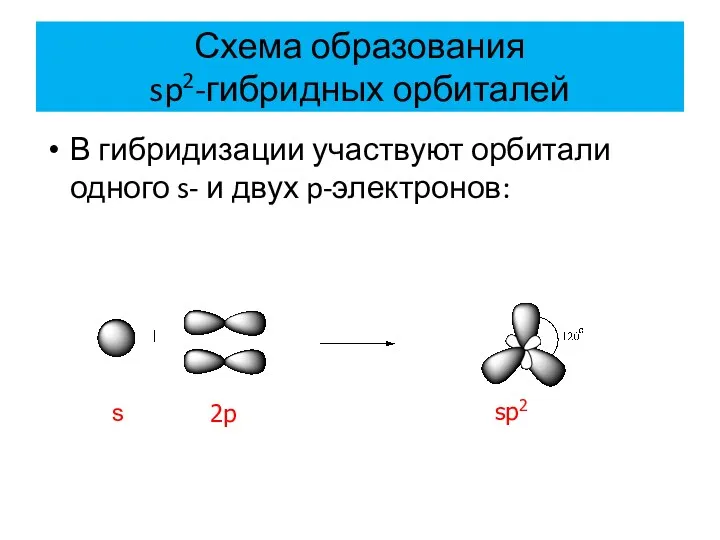
- 4. Схема образования sp2-гибридных орбиталей В гибридизации участвуют орбитали одного s- и двух p-электронов: s 2p sp2
- 5. Гомологический ряд алкенов Этен Пропен Бутен Пентен Гексен Гептен C2H4 C3H6 C4H8 C5H10 C6H12 C7H14 Общая
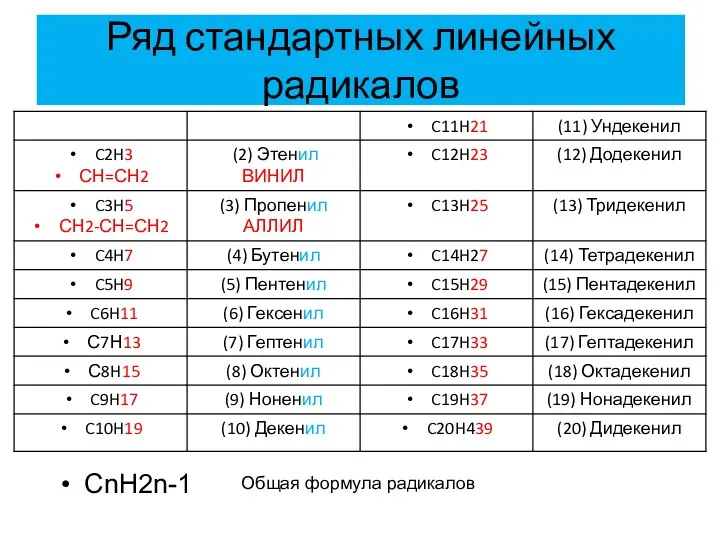
- 6. Ряд стандартных линейных радикалов СnH2n-1 Общая формула радикалов
- 7. Номенклатура Название алкенов по систематической номенклатуре образуют из названий алканов, заменяя суффикс –ан на –ен. Цифрой
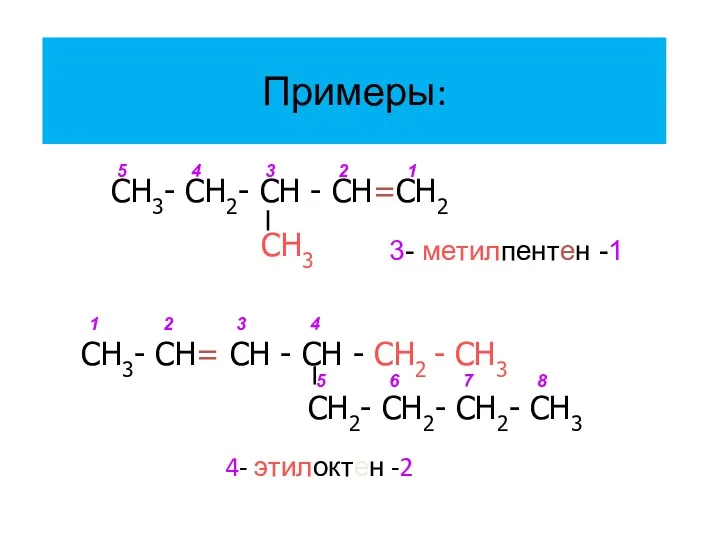
- 8. Примеры: 4- этилоктен -2 СН3- СН2- СН - СН=СН2 СН3 СН3- СН= СН - СН -
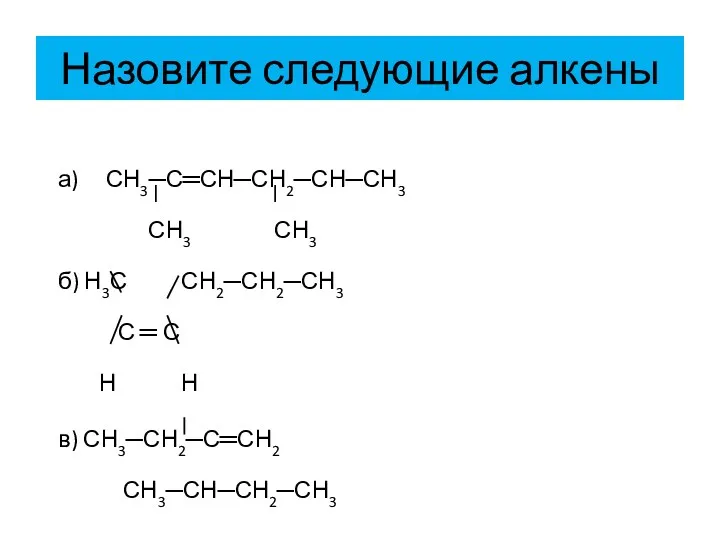
- 9. Назовите следующие алкены а) СН3─С═СН─СН2─СН─СН3 СН3 СН3 б) Н3С СН2─СН2─СН3 С ═ С Н Н в)
- 10. Определите структурную формулу по названию 1,2,3-трихлорпропен-1 2-бром-3,4-диметилгептен-3 3-метил-5-этилоктен-2 2-метилоктен-2
- 11. Изомерия алкенов Для алкенов возможны два типа изомерии: 1-ый тип – структурная изомерия: углеродного скелета положения
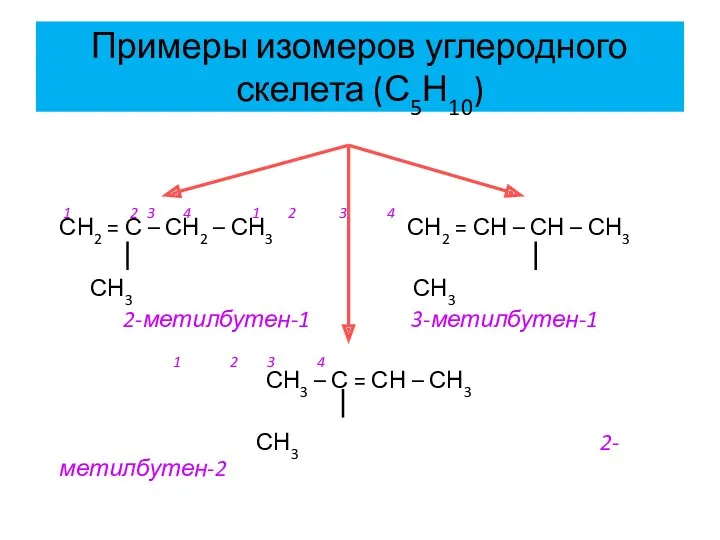
- 12. Примеры изомеров углеродного скелета (С5Н10) 1 2 3 4 1 2 3 4 СН2 = С
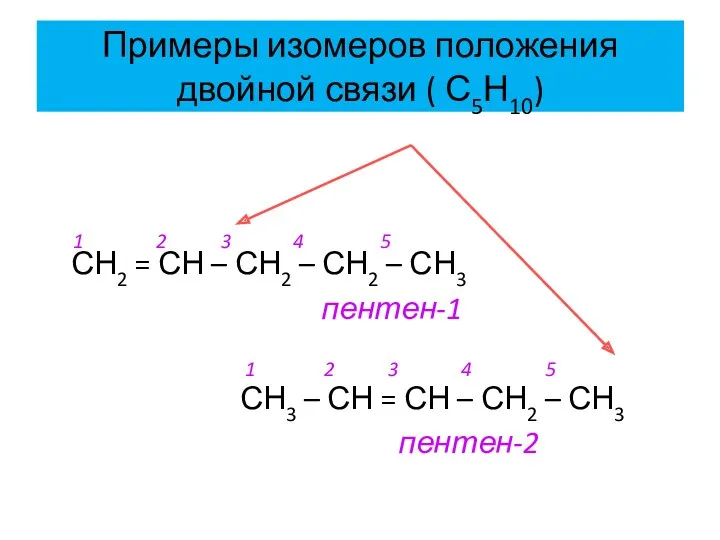
- 13. Примеры изомеров положения двойной связи ( С5Н10) 1 2 3 4 5 СН2 = СН –
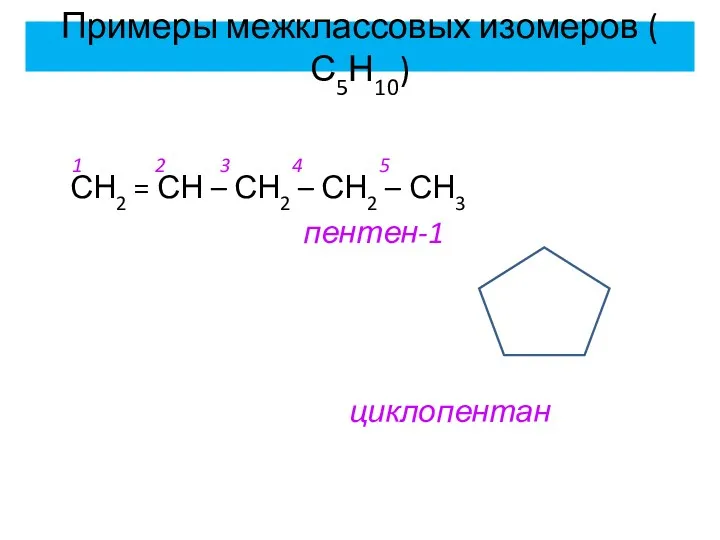
- 14. Примеры межклассовых изомеров ( С5Н10) 1 2 3 4 5 СН2 = СН – СН2 –
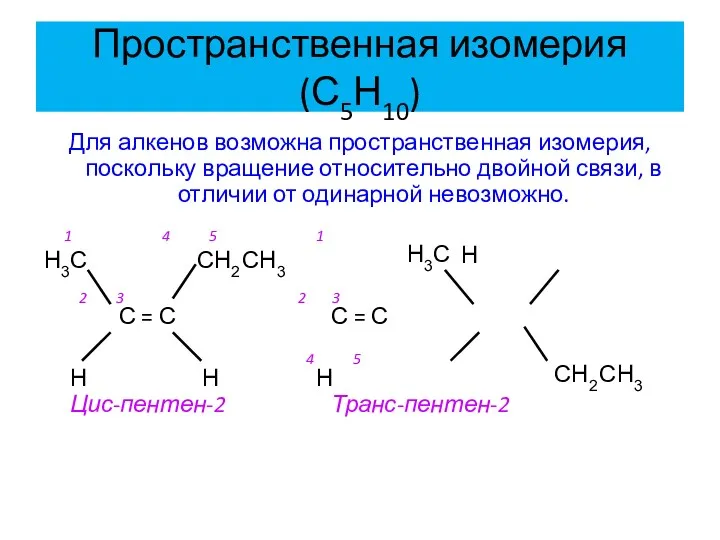
- 15. Пространственная изомерия (С5Н10) Для алкенов возможна пространственная изомерия, поскольку вращение относительно двойной связи, в отличии от
- 16. Напишите 3 вида структурных и пространственный изомеры н-бутена-1
- 17. Физические свойства алкенов Алкены плохо растворимы в воде, но хорошо растворяются в органических растворителях. С2– С4
- 18. Химические свойства алкенов По химическим свойствам алкены резко отличаются от алканов. Алкены более химически активные вещества,
- 19. Типы химических реакций, которые характерны для алкенов Реакции присоединения. Реакции полимеризации. Реакции окисления.
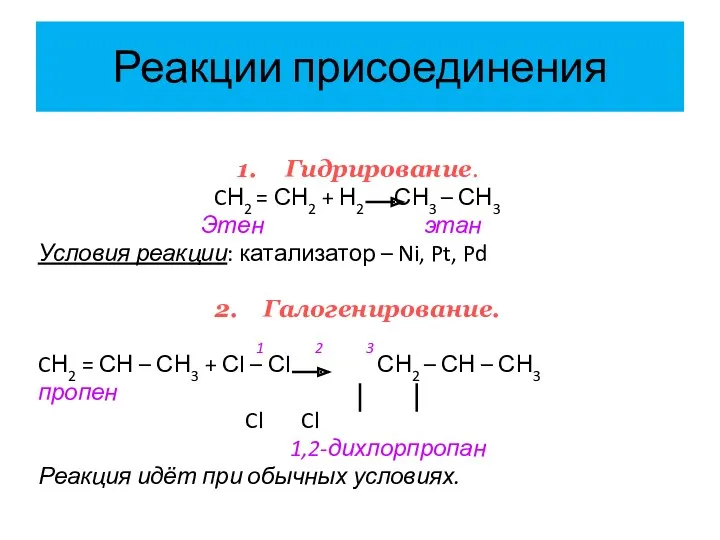
- 20. Реакции присоединения 1. Гидрирование. CН2 = СН2 + Н2 СН3 – СН3 Этен этан Условия реакции:
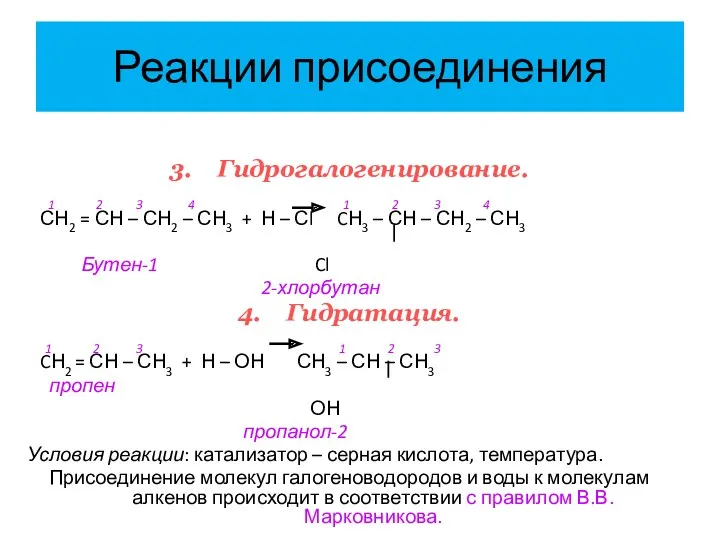
- 21. Реакции присоединения 3. Гидрогалогенирование. 1 2 3 4 1 2 3 4 СН2 = СН –
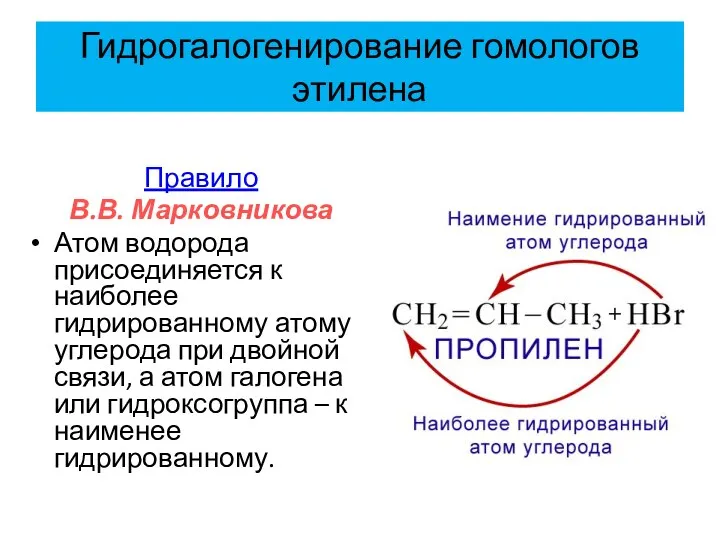
- 22. Гидрогалогенирование гомологов этилена Правило В.В. Марковникова Атом водорода присоединяется к наиболее гидрированному атому углерода при двойной
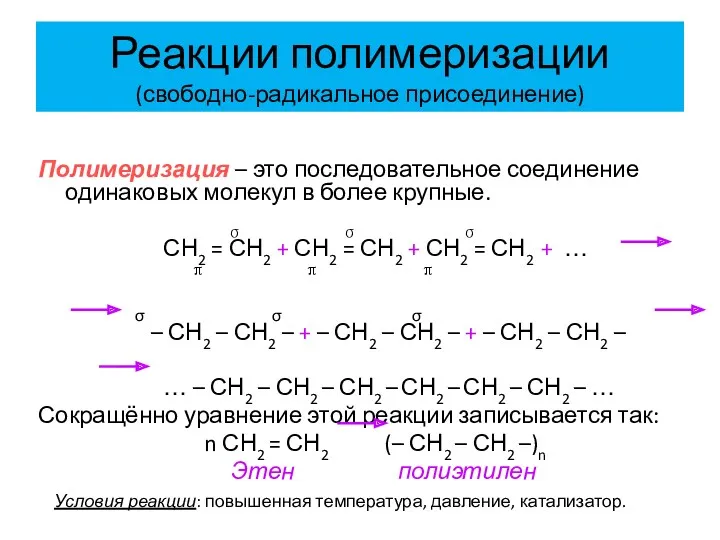
- 23. Реакции полимеризации (свободно-радикальное присоединение) Полимеризация – это последовательное соединение одинаковых молекул в более крупные. σ σ
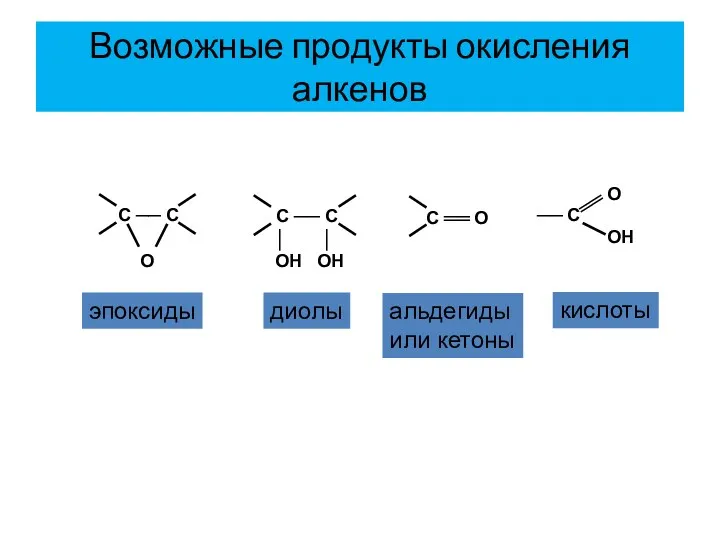
- 24. Возможные продукты окисления алкенов эпоксиды диолы альдегиды или кетоны кислоты
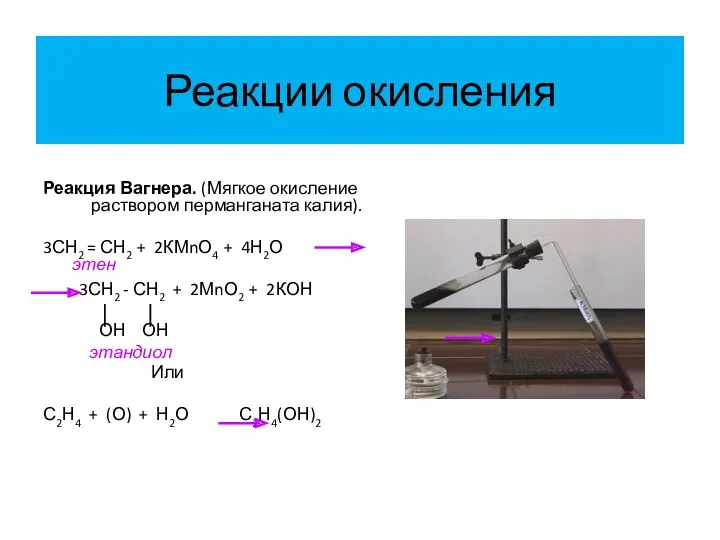
- 25. Реакции окисления Реакция Вагнера. (Мягкое окисление раствором перманганата калия). 3СН2 = СН2 + 2КМnО4 + 4Н2О
- 26. Реакции окисления Жесткое окисление раствором перманганата калия в кислой среде (K2Cr2O7, KMnO4). Происходит полный разрыв двойной
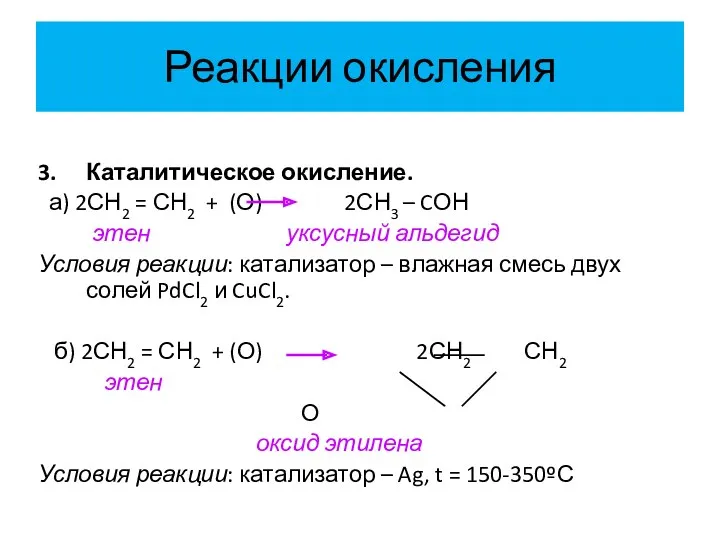
- 27. Реакции окисления 3. Каталитическое окисление. а) 2СН2 = СН2 + (О) 2СН3 – CОН этен уксусный
- 28. Горение алкенов Алкены горят красноватым светящимся пламенем, в то время как пламя предельных углеводородов голубое. Массовая
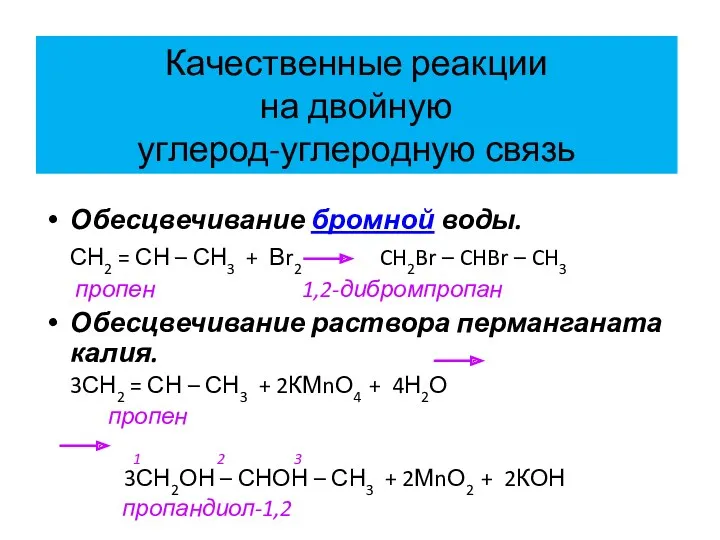
- 29. Качественные реакции на двойную углерод-углеродную связь Обесцвечивание бромной воды. СН2 = СН – СН3 + Вr2
- 30. Применение Алкены широко используются в промышленности в качестве исходных веществ для получения растворителей (спирты, дихлорэтан, эфиры
- 31. Это интересно Всем известный полиэтилен был получен был получен в 1933 году Э. Фосеттом и Р.
- 32. а) СН3-СН=СН2 + НСl → ? б) СН2=СН-СН2-СН3 + НBr → ? В) СН3-СН2-СН=СН2 + НОН
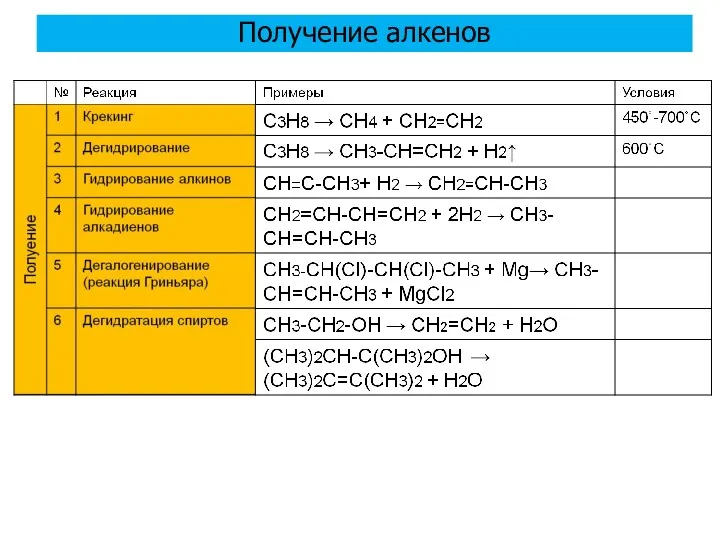
- 33. Получение алкенов
- 35. Скачать презентацию















 Простые вещества металлы
Простые вещества металлы Биотыңайтқыштар
Биотыңайтқыштар Цинк
Цинк Тканые армирующие наполнители
Тканые армирующие наполнители Углеводы. Урок по химии для 9 класса
Углеводы. Урок по химии для 9 класса Оксиди нітрогену
Оксиди нітрогену Классы неорганических веществ (лекция № 4/5)
Классы неорганических веществ (лекция № 4/5) Роль хімії у розв`язанні екологічної проблеми
Роль хімії у розв`язанні екологічної проблеми Молекулярна маса речовини
Молекулярна маса речовини Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Запалювання нагрітим тілом та електричним розрядом
Запалювання нагрітим тілом та електричним розрядом Интересные факты о химических веществах
Интересные факты о химических веществах Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи General, specific properties are common to all matters
General, specific properties are common to all matters Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Фосфор и его соединения. Урок по химии для 9 класса
Фосфор и его соединения. Урок по химии для 9 класса Химические реакторы
Химические реакторы Физические методы стабилизации масел
Физические методы стабилизации масел Экспериментальным исследованием установить тип данной химической реакции
Экспериментальным исследованием установить тип данной химической реакции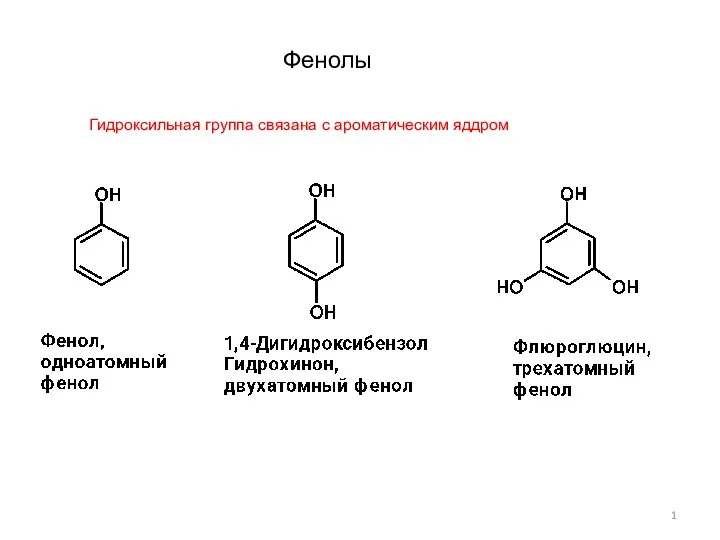 Фенолы-1
Фенолы-1 Химический факультет
Химический факультет Непредельные углеводороды. Алкины
Непредельные углеводороды. Алкины Катиониты. Классификация катионитов
Катиониты. Классификация катионитов Азотная кислота
Азотная кислота Классификация химических реакций
Классификация химических реакций Озон. Применение
Озон. Применение Дисперсные системы
Дисперсные системы