Слайд 2

Карбоновыми кислотами называются производные углеводородов, в молекуле которых содержится одна или
несколько карбоксильных групп –COOH.
Общая формула карбоновых кислот:
В зависимости от природы радикала, связанного с карбоксильной группой, кислоты подразделяются на предельные, непредельные и ароматические.
Число карбоксильных групп определяет основность кислот.
Общая формула предельных одноосновных кислот: СnH2n+1COOH (или СnH2nO2).
Слайд 3
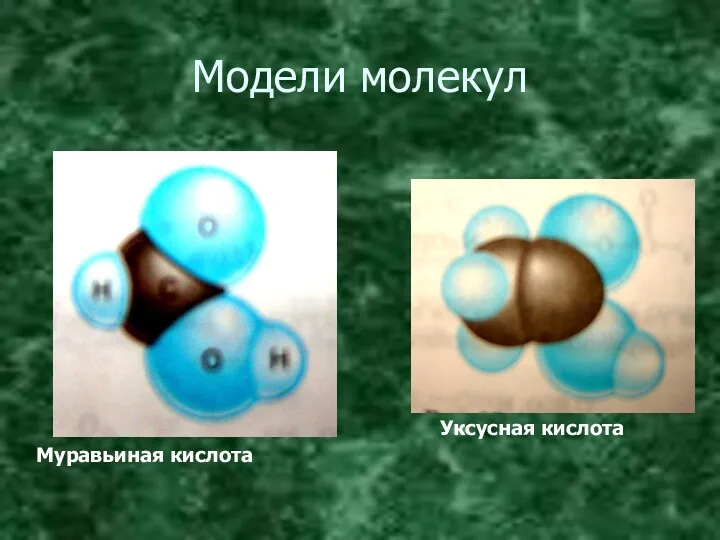
Модели молекул
Уксусная кислота
Муравьиная кислота
Слайд 4

Номенклатура
Распространены тривиальные названия. По правилам IUPAC к названию углеводорода добавляют
"- овая кислота".
HCOOH – муравьиная кислота
CH3COOH – уксусная кислота
CH3CH2COOH – пропионовая кислота
CH3(CH2)2COOH – масляная кислота
CH3(CH2)3COOH – валериановая кислота
CH3(CH2)4COOH – капроновая кислота
C6H5COOH – бензойная кислота
CH3(CH2)14COOH – пальмитиновая кислота
CH3(CH2)16COOH – стеариновая кислота
Слайд 5

Изомерия.
Для алифатических кислот - изомеризация углеводородного радикала.
Для ароматических -
изомерия положения заместителя при бензольном кольце.
Межклассовая изомерия со сложными эфирами (например, CH3-COOH и HCOO-CH3).
Слайд 6

Физические свойства
С1- С3 жидкости с характерным резким запахом
С4- С9 вязкие
маслянистые жидкости с неприятным запахом
С С10 твердые нерастворимые вещества
Карбоновые кислоты имеют аномально высокие температуры кипения из-за наличия межмолекулярных водородных связей и существуют в основном в виде димеров .
С ростом относительной молекулярной массы температура кипения предельных одноосновных кислот увеличивается
Слайд 7

Получение
Окисление первичных спиртов и альдегидов (кислородом на катализаторе; KMnO4; K2Cr2O7):
R-CH2OH
→ RCOH → RCOOH
каталитическое окисление метана:
2CH4 + 3O2 → 2H–COOH + 2H2O
каталитическое окисление бутана:
2CH3–CH2–CH2–CH3 + 5O2 → 4CH3COOH + 2H2O
Ароматические кислоты синтезируют окислением гомологов бензола: в качестве окислителя можно использовать растворы KMnO4 или K2Cr2O7 в кислой среде:
5C6H5CH3 + 6KMnO4 + 9H2SO4 → 5C6H5COOH + 3K2SO4 + 6MnSO4 + 14H2O
Слайд 8

Химические свойства
Карбоновые кислоты- слабые электролиты, в водном растворе диссоциируют:
R–COOH
R–COO- + H+
Карбоновые кислоты обладают свойствами, характерными для минеральных кислот. Они реагируют с активными металлами, основными оксидами, основаниями, солями слабых кислот.
Взаимодействие с металлами:
2СH3COOH + Mg → (CH3COO)2Mg + H2
Взаимодействие с основными оксидами:
2СH3COOH + СaO → (CH3COO)2Ca + H2O
Взаимодействие с основаниями:
H–COOH + NaOH → H–COONa + H2O
Слайд 9

Взаимодействие с солями более слабых и летучих кислот:
2СH3CH2COOH + Na2CO3
→ 2CH3CH2COONa + H2O + CO2
Взаимодействие со спиртами:
CH3COOH+ C2H5OH CH3COOC2H5 + H2O
Взаимодействие с галогенами:
CH3COOH + Cl2 → ClCH2COOH + HCl
Раствор муравьиной кислоты, в отличие от других карбоновых кислот дает реакцию «серебряного зеркала»
HCOOH + Ag2O → CO2+ H2O
Слайд 10

Применение
Муравьиная кислота – в медицине, в пчеловодстве, в органическом синтезе, при
получении растворителей и консервантов; в качестве сильного восстановителя.
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров).
Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов.
Щавелевая кислота – в металлургической промышленности (удаление окалины).
Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке.
Слайд 11

Какие вещества образуются, если в реакцию вступят вещества, модели молекул которых
изображены на рисунке?
составьте уравнение химической реакции.










 Химический элемент радий
Химический элемент радий Основания. Классификация оснований
Основания. Классификация оснований Реакции электрофильного замещения в ароматическом ряду Se
Реакции электрофильного замещения в ароматическом ряду Se Главная подгруппа IV группы
Главная подгруппа IV группы Алкадиены (диеновые углеводороды)
Алкадиены (диеновые углеводороды) Свойства моторных топлив
Свойства моторных топлив Соли. Классификация. Физические и химические свойства. Получение и применение солей
Соли. Классификация. Физические и химические свойства. Получение и применение солей Химия и обмен углеводов. Функции углеводов
Химия и обмен углеводов. Функции углеводов Азотовмисні та елементоорганічні сполуки
Азотовмисні та елементоорганічні сполуки Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Азотная кислота. К уроку химии для 9 класса
Азотная кислота. К уроку химии для 9 класса Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Колоїдний захист
Колоїдний захист Алюминий и его соединения
Алюминий и его соединения Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння
Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння Содержание кислорода и углекислого газа в помещениях школы
Содержание кислорода и углекислого газа в помещениях школы Конструкционные функциональные волокнистые композиты. Углеродные волокна
Конструкционные функциональные волокнистые композиты. Углеродные волокна Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Основные химические понятия
Основные химические понятия Интоксикации сельскохозяйственными ядохимикатами (пестицидами)
Интоксикации сельскохозяйственными ядохимикатами (пестицидами) Химическая кинетика
Химическая кинетика Классификация органических реакций
Классификация органических реакций Строение электронных оболочек атомов
Строение электронных оболочек атомов Алкены
Алкены Основные понятия и законы химии. Тема1
Основные понятия и законы химии. Тема1 Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9
Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9 Осадительное титрование. Меркуриметрия
Осадительное титрование. Меркуриметрия Общая характеристика неметаллов
Общая характеристика неметаллов