Содержание
- 2. — (CH2— CH2—) Поливинилы — (CH2— CH2—)n Олигомеры Полимеры Элементарное звено Функциональная группа Z Концевые группы
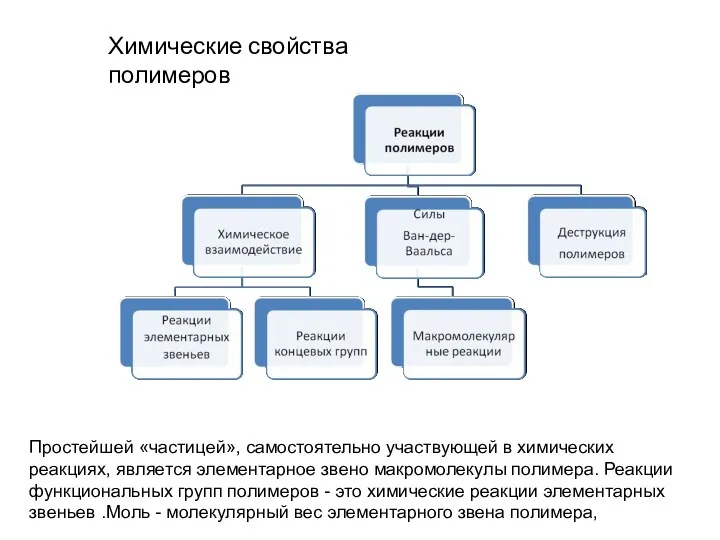
- 3. Простейшей «частицей», самостоятельно участвующей в химических реакциях, является элементарное звено макромолекулы полимера. Реакции функциональных групп полимеров
- 4. Физические свойства полимеров Анизотропия свойств кристаллических, жидкокристаллических, и ориентированных аморфных полимеров Способность к волокно- и пленкообразованию
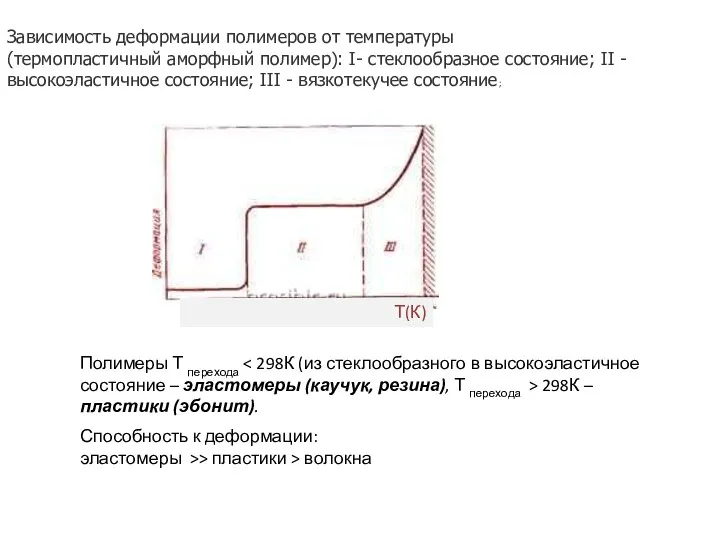
- 5. Зависимость деформации полимеров от температуры (термопластичный аморфный полимер): I- стеклообразное состояние; II - высокоэластичное состояние; III
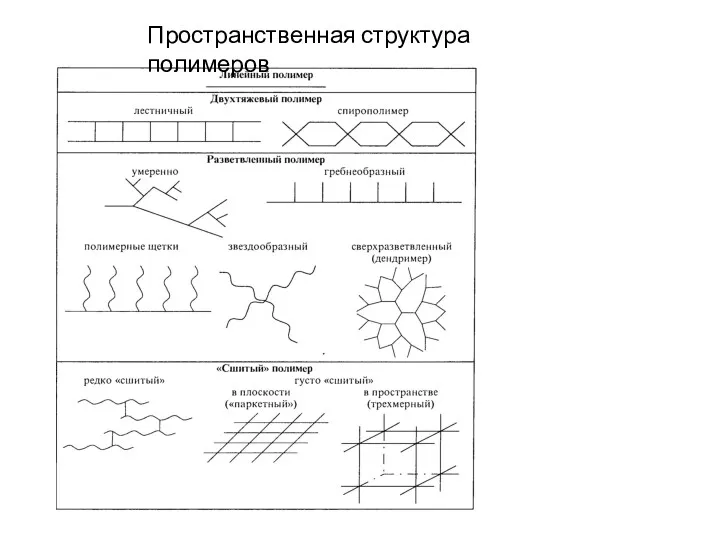
- 6. Пространственная структура полимеров
- 7. Полярность связи Дипольный момент μ = δ ⋅ l [Кл⋅м], Дебай (D) 1 D = 3,33⋅10-30
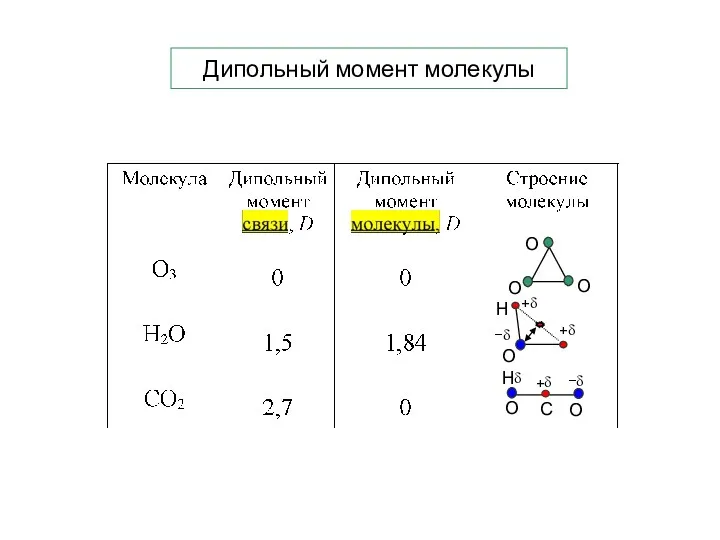
- 8. Дипольный момент молекулы
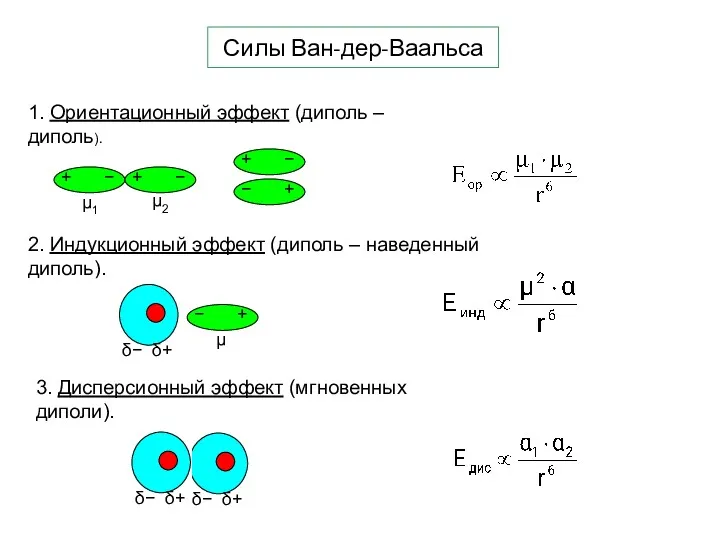
- 9. Силы Ван-дер-Ваальса 1. Ориентационный эффект (диполь – диполь). 2. Индукционный эффект (диполь – наведенный диполь). 3.
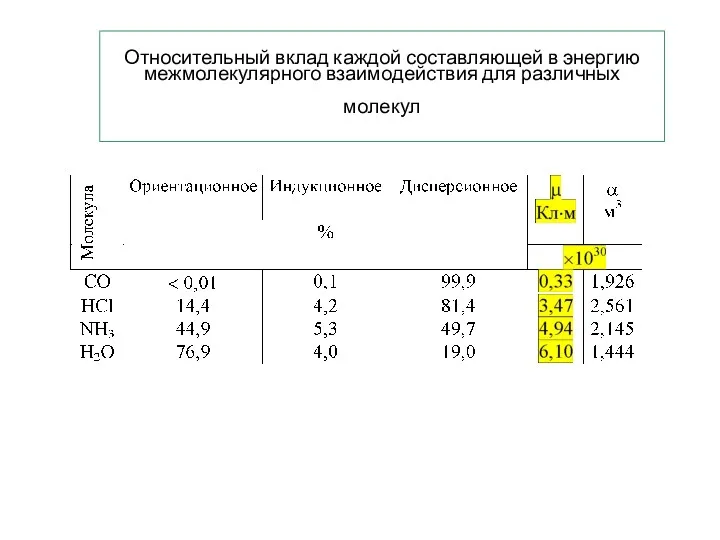
- 10. Относительный вклад каждой составляющей в энергию межмолекулярного взаимодействия для различных молекул
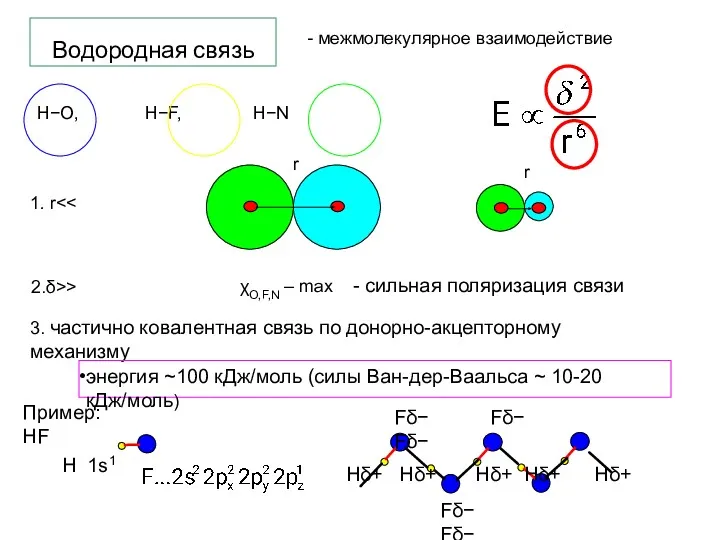
- 11. Водородная связь - межмолекулярное взаимодействие 1. r 2.δ>> χO,F,N – max - сильная поляризация связи 3.
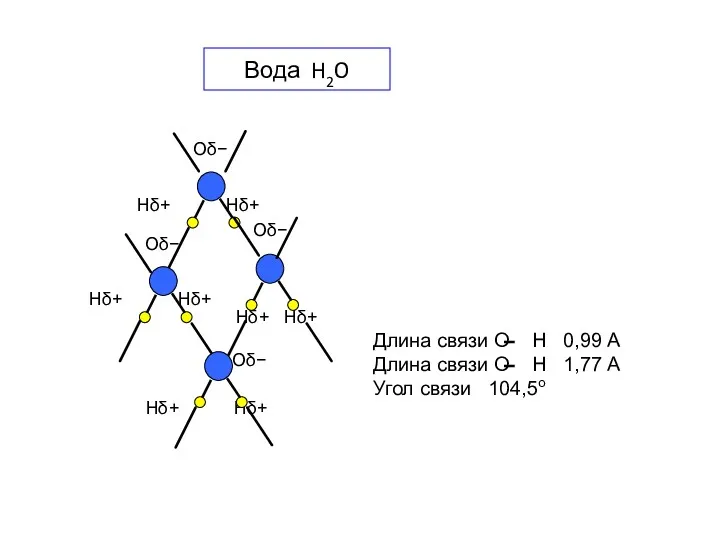
- 12. Вода H2O
- 13. Конформация клубок-глобула
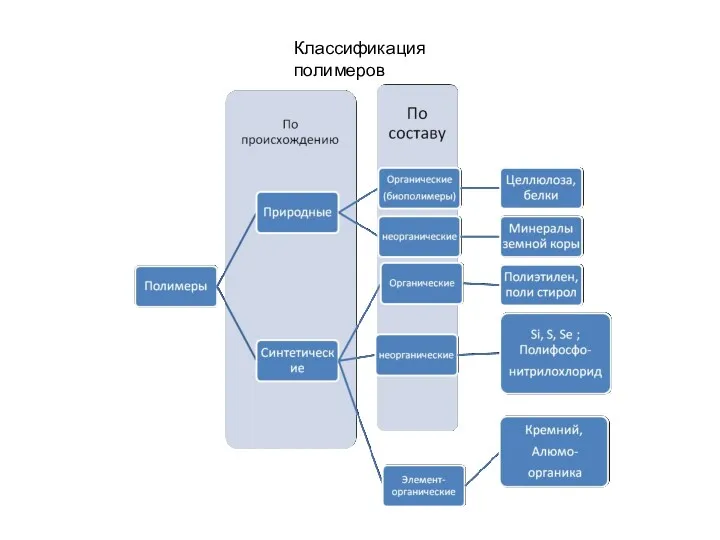
- 14. Классификация полимеров
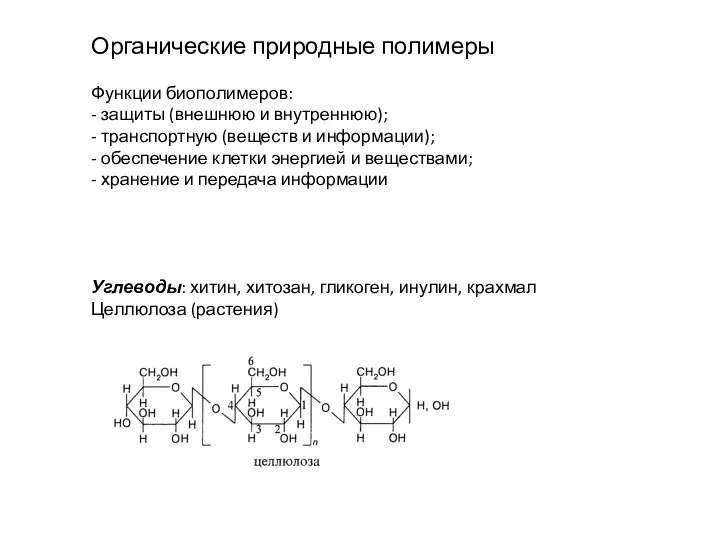
- 15. Органические природные полимеры Функции биополимеров: - защиты (внешнюю и внутреннюю); - транспортную (веществ и информации); -
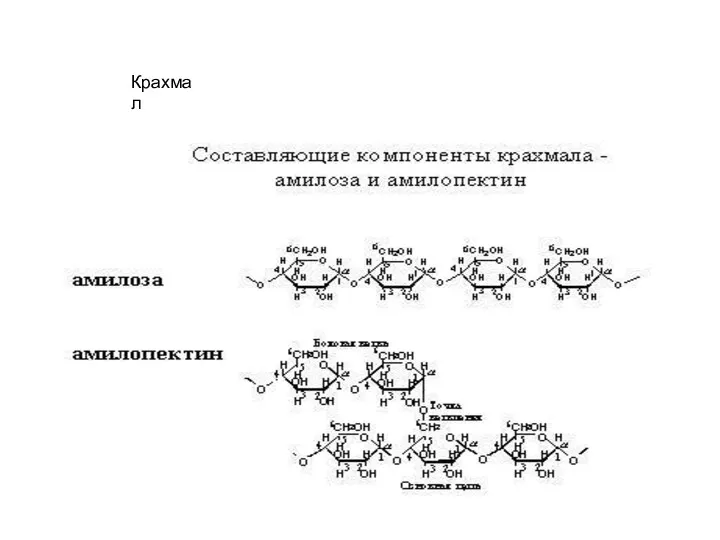
- 16. Крахмал
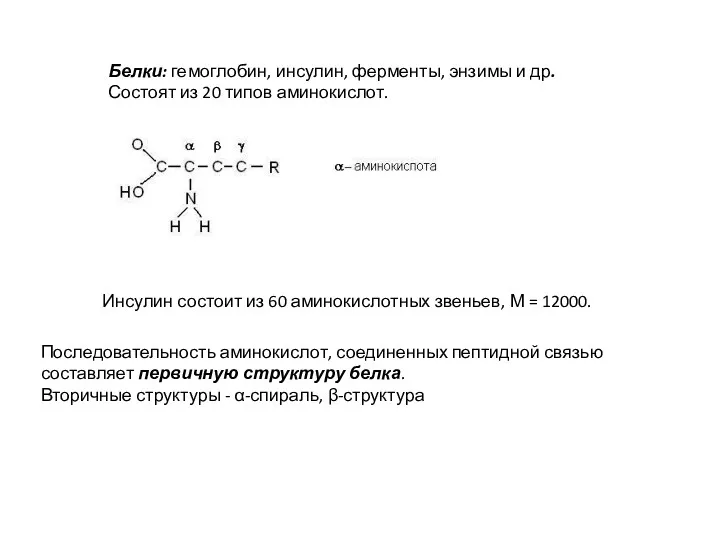
- 17. Белки: гемоглобин, инсулин, ферменты, энзимы и др. Состоят из 20 типов аминокислот. Инсулин состоит из 60
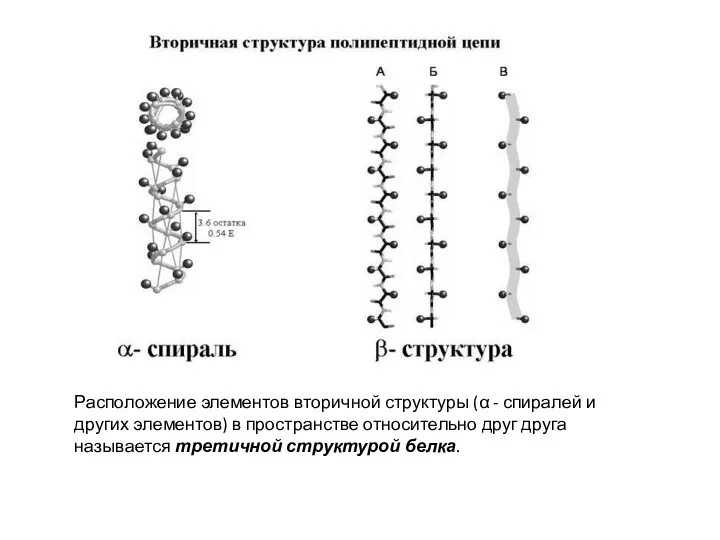
- 18. Расположение элементов вторичной структуры (α - спиралей и других элементов) в пространстве относительно друг друга называется
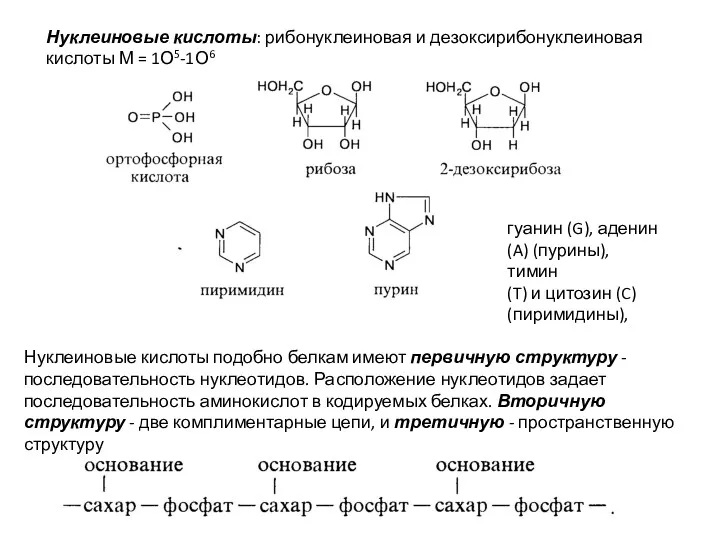
- 19. Нуклеиновые кислоты: рибонуклеиновая и дезоксирибонуклеиновая кислоты М = 1О5-1О6 Нуклеиновые кислоты подобно белкам имеют первичную структуру
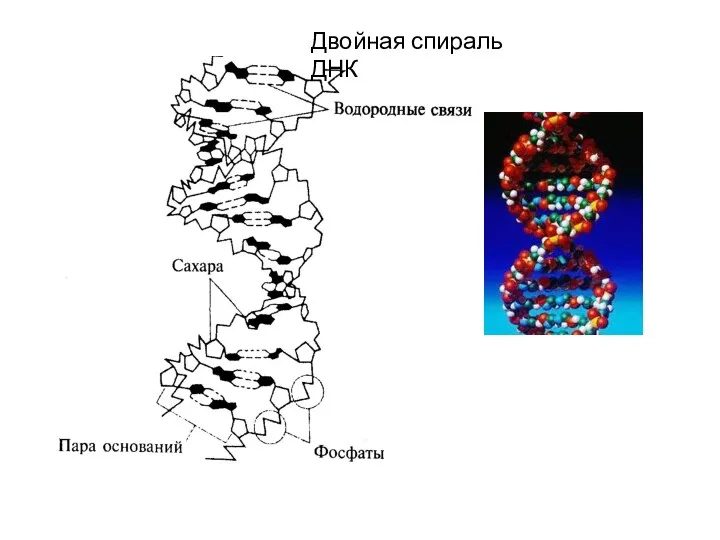
- 20. Двойная спираль ДНК
- 21. Функции ДНК ДНК является носителем генетической информации. Функция обеспечивается фактом существования генетического кода. Воспроизведение и передача
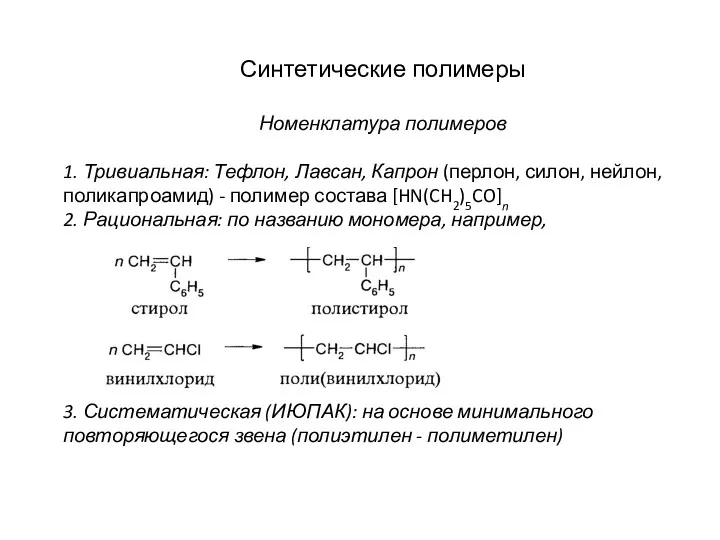
- 22. Синтетические полимеры Номенклатура полимеров 1. Тривиальная: Тефлон, Лавсан, Капрон (перлон, силон, нейлон, поликапроамид) - полимер состава
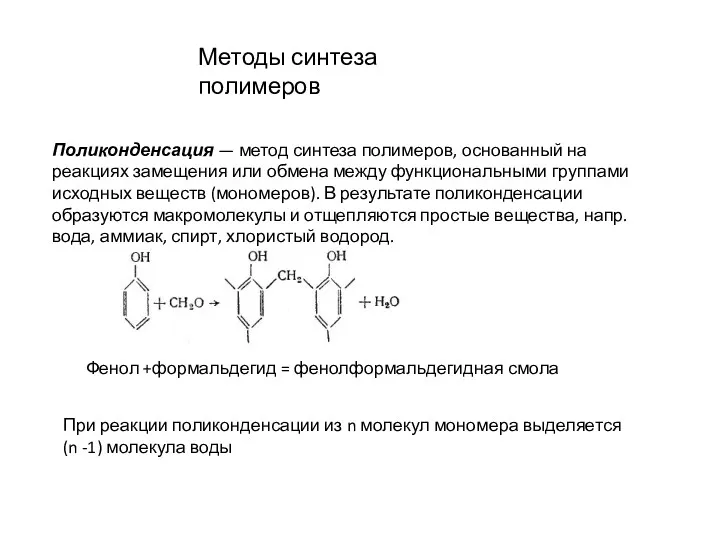
- 23. Поликонденсация — метод синтеза полимеров, основанный на реакциях замещения или обмена между функциональными группами исходных веществ
- 24. Полимеризация — химическая реакция соединения одинаковых молекул в сложные молекулы большой молекулярной массы. Продукт полимеризации имеет
- 25. Деструкция полимеров Крекинг— способ переработки нефти и нефтепродуктов, основанный на расщеплении больших молекул углеводородов нефти и
- 27. Скачать презентацию


![Полярность связи Дипольный момент μ = δ ⋅ l [Кл⋅м],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/233271/slide-6.jpg)




 Минералды тыңайтқыштар
Минералды тыңайтқыштар Тотығу-тотықсыздану титрлеу әдісі
Тотығу-тотықсыздану титрлеу әдісі Пены. Пенообразование
Пены. Пенообразование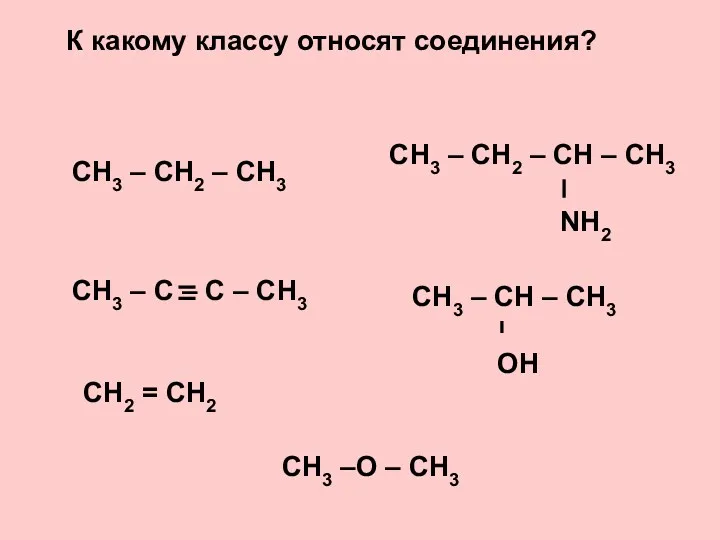 16_OP_05_Alkany
16_OP_05_Alkany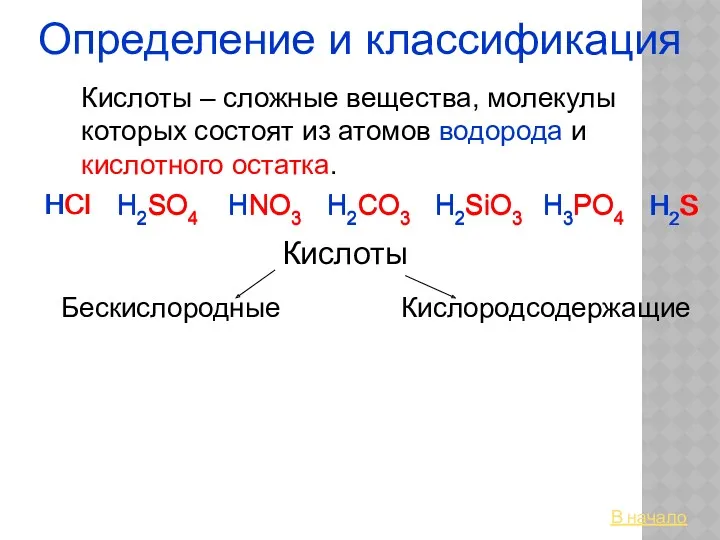 Кислоты. Определение и классификация
Кислоты. Определение и классификация Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы
Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы Квантово-механический подход к описанию строения атомов
Квантово-механический подход к описанию строения атомов d-элементы
d-элементы Химия и живопись
Химия и живопись Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Химическое равновесие
Химическое равновесие Тест: полимеры
Тест: полимеры Платина. Физические и химические свойства
Платина. Физические и химические свойства Минералогия с основами кристаллографии
Минералогия с основами кристаллографии Химические реакции
Химические реакции Бордың адам ағзасына әсері
Бордың адам ағзасына әсері Гідроліз солей
Гідроліз солей Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2)
Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2) Соединения железа. Охарактеризуйте Fe
Соединения железа. Охарактеризуйте Fe Cross-section sample preparation using focused ion beam system (FIB) for transmission electron microscopy (TEM)
Cross-section sample preparation using focused ion beam system (FIB) for transmission electron microscopy (TEM) Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Structural, substructural properties and chemical composition
Structural, substructural properties and chemical composition Водород
Водород Композиционные материалы
Композиционные материалы Реакции ионного обмена
Реакции ионного обмена Галогенопроизводные углеводородов 1
Галогенопроизводные углеводородов 1