Тепловий ефект хімічних реакцій. Екзотермічні ї ендотермічні реакції термохімічні рівняння презентация
Содержание
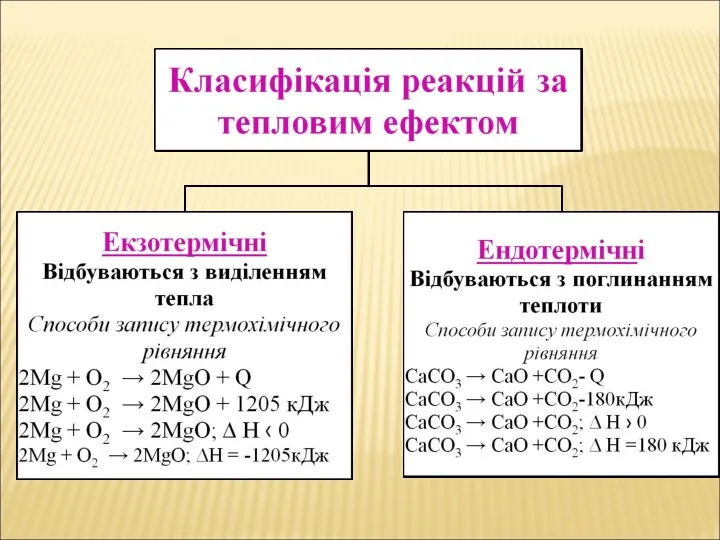
- 2. ТЕРМОХІМІЯ – ЦЕ РОЗДІЛ ХІМІЇ, ЯКИЙ ВИВЧАЄ ХІМІЧНІ ПРОЦЕСИ З ТОЧКИ ЗОРУ ПОГЛИНАННЯ АБО ВИДІЛЕННЯ ТЕПЛОТИ.
- 4. ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ – КІЛЬКІСТЬ ТЕПЛОТИ, ЩО ВИДІЛЯЄТЬСЯ ЧИ ПОГЛИНАЄТЬСЯ ПІД ЧАС ХІМІЧНИХ РЕАКЦІЇ. Тепловий ефект
- 5. ЗАКОН ГЕССА Тепловий ефект реакції залежить лише від початкового та кінцевого стану реагуючих речовин, але не
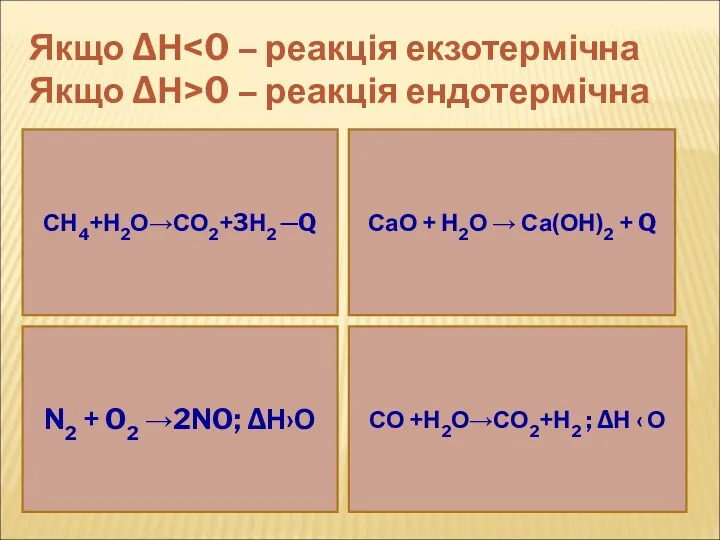
- 6. Якщо ∆Н Якщо ∆Н>0 – реакція ендотермічна СН4+Н2О→СО2+3Н2 ─Q СаО + Н2О → Са(ОН)2 + Q
- 7. Рівняння реакцій, в яких указано чисельне значення теплового ефекту реакції, а також агрегатний стан речовин, називають
- 8. Закріпи свої знання
- 9. Завдання 1. У процесі згоряння 12 г вуглецю виділяється 393 кДж тепла. Запишіть термохімічне рівняння. C
- 10. Завдання 2. При утворенні 1 моль хлороводню з простих речовин виділяється 92,2 кДж. Обчислити кількість теплоти
- 11. Завдання 3. Обчисліть кількість теплоти, що виділиться при спалюванні: а) 4 моль; б) 4г; в) 4л
- 13. Скачать презентацию








 Фенол қосылыстары
Фенол қосылыстары Антибиотики как ЛС
Антибиотики как ЛС Металлы и неметаллы
Металлы и неметаллы Основи. Гідроксиди Натрію і Кальцію
Основи. Гідроксиди Натрію і Кальцію Нобелевская премия по химии
Нобелевская премия по химии Высокоэффективная жидкостная хроматография
Высокоэффективная жидкостная хроматография Органические вещества
Органические вещества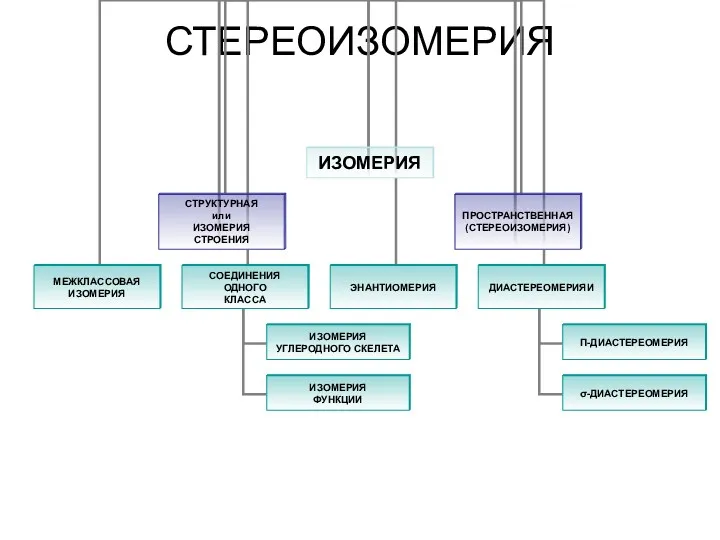 Стереоизомерия. Изомерия. Пространственная (стереоизомерия) углеродного скелета
Стереоизомерия. Изомерия. Пространственная (стереоизомерия) углеродного скелета Реакции ионного обмена в растворах электролитов. рH раствора как показатель кислотности среды
Реакции ионного обмена в растворах электролитов. рH раствора как показатель кислотности среды Вещества и их системы. Растворы. Массовая доля растворенного вещества. 11 класс
Вещества и их системы. Растворы. Массовая доля растворенного вещества. 11 класс Құймалар. Механикалық қоспа
Құймалар. Механикалық қоспа История развития и предмет исследования супрамолекулярной химии. Классификация супрамолекулярных соединений
История развития и предмет исследования супрамолекулярной химии. Классификация супрамолекулярных соединений Кремний и его соединения. Нахождение в природе
Кремний и его соединения. Нахождение в природе Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Оксид серы(4). Сернистая кислота и её соли
Оксид серы(4). Сернистая кислота и её соли Кафедра химической технологии лекарственных веществ (ХТЛВ)
Кафедра химической технологии лекарственных веществ (ХТЛВ) Електролітична дисоціація
Електролітична дисоціація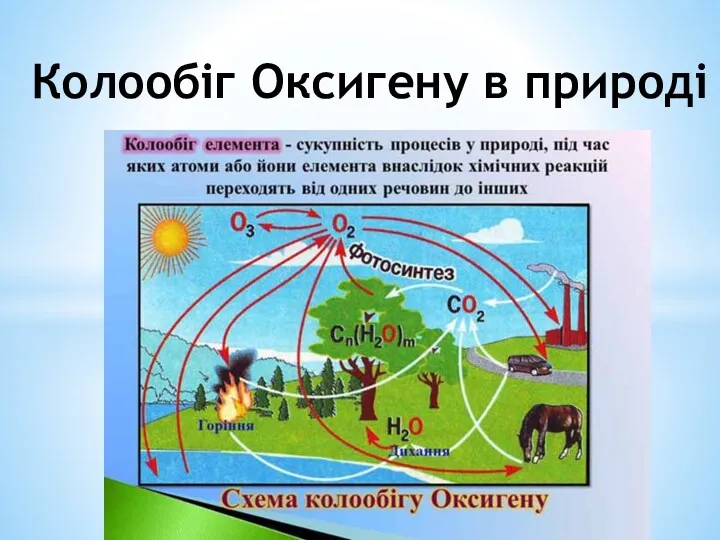 Колообіг оксигену в природі
Колообіг оксигену в природі Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Хімія металургійних процесів. Теорія сплавів
Хімія металургійних процесів. Теорія сплавів Классификация химических реакций по механизму реакции
Классификация химических реакций по механизму реакции Көмірсутектер.Олардың жіктелуі, құрылысы,изомериясы және номенклатурасы
Көмірсутектер.Олардың жіктелуі, құрылысы,изомериясы және номенклатурасы Органическая химия. Этапы развития органической химии
Органическая химия. Этапы развития органической химии Элемент свинец Рb
Элемент свинец Рb Щелочи
Щелочи Спирты. Действие этанола на организм человека (10 класс)
Спирты. Действие этанола на организм человека (10 класс) Вирощування кристалів солей
Вирощування кристалів солей Термопластичные полимеры
Термопластичные полимеры