Содержание
- 2. «Смесь» - это то, что принято за целое. Смесь может быть любого вида – твердая (сплав,
- 3. «Чистое вещество» - это то, что по условию задачи составляет интересующую нас часть целого (соль в
- 4. «Примеси»- это то, что по условию задачи составляет остальную часть целого (например: вода в солевом растворе;
- 5. «Доля» (α) чистого вещества – это отношение количества чистого вещества (m) в смеси к общему количеству
- 6. «Процентная концентрация» (с) чистого вещества в смеси – это доля, выраженная процентным отношением, т.е. с =
- 7. Законы сохранения масс M1 + M2 = M3 m1 + m2 = m3 Процентные концентрации и
- 8. Пример: солевой раствор В стакан воды массой mвод насыпали соли массой mcол. В итоге образовался раствор
- 9. В соответствии с ключевыми зависимостями имеем: 1. Доля соли (чистого вещества) в растворе равна α =
- 10. 1.Разбавление водой (или примесями) Масса чистого вещества останется без изменения Масса воды(примесей)увеличится Масса смеси увеличится на
- 11. 2.Добавление чистого вещества Масса чистого вещества увеличится, Масса примесей останется без изменения Масса смеси увеличится на
- 12. 3. Выпаривание воды (или удаление примесей) Масса чистого вещества останется без изменения Масса воды (примесей) уменьшится
- 13. 4. Смешивание двух растворов (соединение двух сплавов) Массы чистого вещества, массы примесей и массы смесей соответственно
- 15. Скачать презентацию












 Металдарға қандай физикалық қасиеттер тән?
Металдарға қандай физикалық қасиеттер тән? Растворы. Концентрация растворов
Растворы. Концентрация растворов Виды химической связи
Виды химической связи Паровые зоны в гидротермальных системах
Паровые зоны в гидротермальных системах Мир кристаллов. Изучение теоретического материала по теме Кристалл
Мир кристаллов. Изучение теоретического материала по теме Кристалл Поверхностные явления. Адсорбция
Поверхностные явления. Адсорбция Реакции ионного обмена
Реакции ионного обмена ОВР – окислительно-восстановительные реакции. Тема 4
ОВР – окислительно-восстановительные реакции. Тема 4 Электронные конфигурации атомов химических элементов. Графическое изображение электронных конфигураций атомов
Электронные конфигурации атомов химических элементов. Графическое изображение электронных конфигураций атомов Кто хочет стать химиком
Кто хочет стать химиком Сравнение нормативов некоторых веществ
Сравнение нормативов некоторых веществ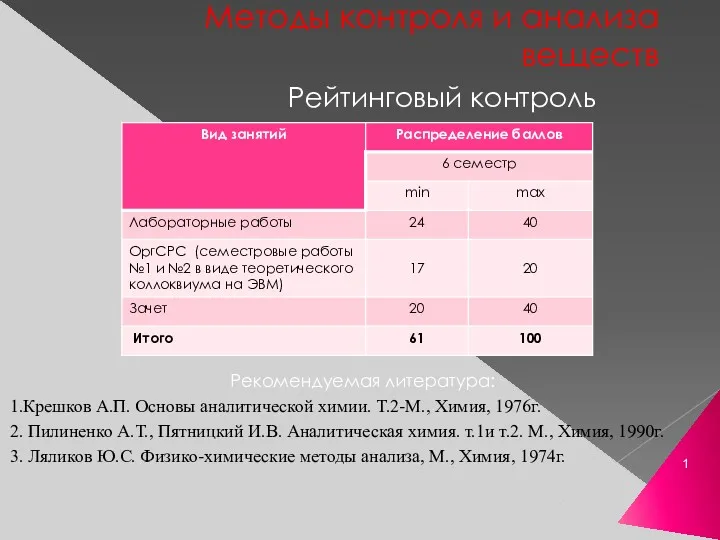 Методы контроля и анализа веществ
Методы контроля и анализа веществ Способы выражения состава раствора. Задача 7
Способы выражения состава раствора. Задача 7 Органический полимер полиэфирэфиркетон (PEEK). Использование PEEK в 3D-печати
Органический полимер полиэфирэфиркетон (PEEK). Использование PEEK в 3D-печати Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.) Електролітична дисоціація. Гідроліз солей
Електролітична дисоціація. Гідроліз солей Циклоалканы
Циклоалканы Непредельные углеводороды
Непредельные углеводороды Обобщающий урок по теме Металлы
Обобщающий урок по теме Металлы Предмет органической химии
Предмет органической химии Окислительно-восстановительные реакции. Генетический ряд кальция
Окислительно-восстановительные реакции. Генетический ряд кальция Типы химических реакций в органической химии
Типы химических реакций в органической химии Воздух и его свойства
Воздух и его свойства Непредельные углеводороды
Непредельные углеводороды Строение атома. Лекция 2
Строение атома. Лекция 2 Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Полипропилен. Области применения полипропилена
Полипропилен. Области применения полипропилена Органика вокруг нас
Органика вокруг нас