Слайд 2

«Вода… Ты не имеешь ни вкуса,
ни цвета, ни запаха,
тебя невозможно
описать – тобой наслаждаешься,
не ведая, что ты такое.
Ты не просто необходима для жизни,
ты и есть сама жизнь.
Ты божество, ты совершенство,
ты самое большое богатство на свете »
Антуан де Сент – Экзюпери.
Слайд 3

Слайд 4

Слайд 5
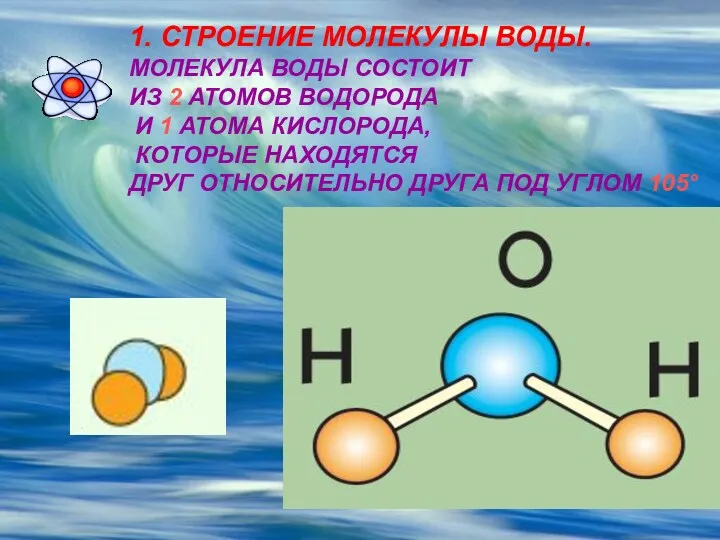
1. СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ.
МОЛЕКУЛА ВОДЫ СОСТОИТ
ИЗ 2 АТОМОВ ВОДОРОДА
И
1 АТОМА КИСЛОРОДА,
КОТОРЫЕ НАХОДЯТСЯ
ДРУГ ОТНОСИТЕЛЬНО ДРУГА ПОД УГЛОМ 105°
Слайд 6

Пользуясь таблицей растворимости,
распределите вещества
по группам:
растворимые,
нерастворимые и малорастворимые.
Назовите
данные вещества.
Ba(OH)2, KCl, BaSO4, CaSO4,
NaNO3, CuSO4, HNO3, AgCl, FeS, Ca(OH)2.
Слайд 7

2.ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ.
ЧИСТАЯ (ДИСТИЛЛИРОВАННАЯ) ВОДА – БЕСЦВЕТНАЯ ЖИДКОСТЬ, БЕЗ ЗАПАХА
И ВКУСА
ЕДИНСТВЕННОЕ ВЕЩЕСТВО, КОТОРОЕ НА ЗЕМЛЕ СУЩЕСТВУЕТ В ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ
ТЕМПЕРАТУРА КИПЕНИЯ 100°С
ТЕМПЕРАТУРА КРИСТАЛЛИЗАЦИИ (ПЛАВЛЕНИЯ) 0°С
Слайд 8

-В XVIII ВЕКЕ ВОДА ПОСЛУЖИЛА ЭТАЛОНОМ ДЛЯ ВЫБОРА ЕДИНИЦЫ МАССЫ:
МАССЕ 1 куб. см. БЫЛО ПРИПИСАНО ЗНАЧЕНИЕ 1г
- МАКСИМАЛЬНАЯ ПЛОТНОСТЬ ПРИ 4°С ПРИНЯТА ЗА 1г/мл, ВСЕ ОСТАЛЬНЫЕ ВЕЩЕСТВА СРАВНИВАЮТСЯ ПО ПЛОТНОСТИ И МАССЕ С ВОДОЙ
-ПЛОТНОСТЬ ЛЬДА МЕНЬШЕ, ЧЕМ У ЖИДКОЙ ВОДЫ, ЧТО ЯВЛЯЕТСЯ АНОМАЛЬНЫМ СВОЙСТВОМ ВОДЫ
-ВОДА ОБЛАДАЕТ САМОЙ БОЛЬШОЙ ТЕПЛОЕМКОСТЬЮ
-ОНА НЕ ПРОВОДИТ
ЭЛЕКТРИЧЕСКИЙ ТОК
Слайд 9
Слайд 10

3. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ.
1. С МЕТАЛЛАМИ.
а) очень активные металлы при взаимодействии
с водой образуют гидроксид и водород
2Na + 2H2O = 2NaOH + H2
гидроксид натрия
2K + 2H2O = 2KOH + H2
гидроксид калия
Ca + 2H2O = Ca(OH)2 + H2
гидроксид кальция
Слайд 11

б) средние по активности металлы при взаимодействии с водой при нагревании
образуют оксид металла и водород
Zn + H2O = ZnO + H2
оксид цинка
в) малоактивные металлы с водой
не реагируют
Слайд 12

2. С ОКСИДАМИ.
а) оксиды металлов при взаимодействии с водой образуют гидроксиды
CaO
+ H2O = Ca(OH)2
гидроксид кальция
б) оксиды неметаллов при взаимодействии с водой образуют кислоты
SO3 + H2O = H2SO4
серная кислота
Слайд 13

Термин "кислотный дождь" существует
уже более 100 лет; впервые его
использовал
британский исследователь
Роберт Ангус Смит в 1882 году,
когда опубликовал книгу
"Воздух и дождь: начало химической
климатологии ".
Кислотные дожди (или более правильно,
кислотные осадки, так как выпадение
вредных веществ может происходить
как в виде дождя, так и в виде снега, града)
наносят значительный экологический,
экономический и эстетический ущерб.
Слайд 14

Причины образования кислотных дождей
вулканы
Естественные причины
гроза
Слайд 15

Причины образования кислотных дождей
Искусственные источники
минеральные удобрения
сжигание топлива
топливо самолетов
нефтепереработка
автотранспорт
Слайд 16
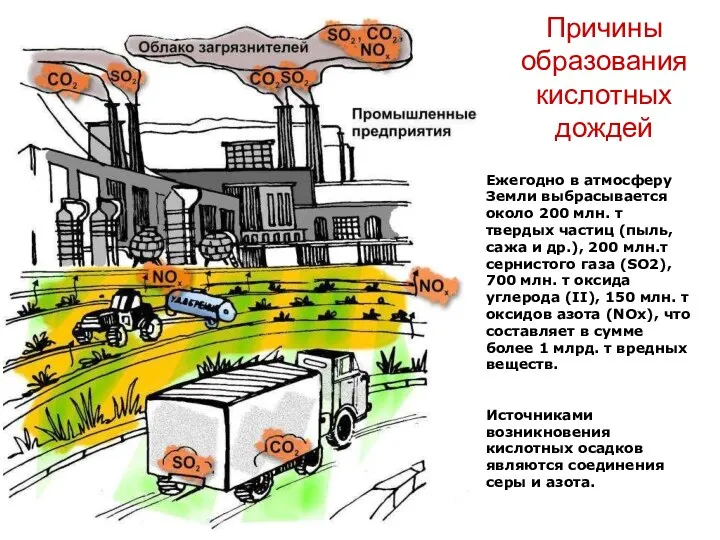
Причины образования кислотных дождей
Ежегодно в атмосферу Земли выбрасывается около 200 млн.
т твердых частиц (пыль, сажа и др.), 200 млн.т сернистого газа (SO2), 700 млн. т оксида углерода (II), 150 млн. т оксидов азота (NOx), что составляет в сумме более 1 млрд. т вредных веществ.
Источниками возникновения кислотных осадков являются соединения серы и азота.
Слайд 17

Сера
содержится в таких полезных ископаемых как уголь, нефть, железные, медные и
др. руды; одни из них используют как топливо, другие направляют на предприятия химической и металлургической промышленности.
При переработке (в частности, при обжиге руд) сера переходит в химические соединения, например, в сернистый газ (оксид серы (IV)). Образовавшиеся соединения частично улавливаются очистными сооружениями, остальное их количество выбрасывается в атмосферу. Соединяясь с парами воды, предварительно окисленный оксид серы (IV) образует серную кислоту.
Слайд 18

Сера
В большинстве антропогенных выбросов преобладают оксид серы (IV) и сульфаты. Сульфаты
выделяются при сжигании топлива и в ходе таких промышленных процессов, как нефтепереработка, производство цемента и гипса, серной кислоты. Из природных источников серосодержащих соединений важную роль играют биогенные выбросы из почвы и продукты жизнедеятельности растений. В настоящее время в науке недостаточно данных о механизме процессов, в результате которых выделяются соединения серы.
Слайд 19

Сера
При извержениях вулканов преобладает оксид серы (IV), в меньшем количестве в
атмосферу поступает сероводород, а также сульфаты в виде аэрозолей и твердых частиц. Ежегодно во всем мире в результате вулканической деятельности выделяется 4-16 млн. т соединений серы (в пересчете на SO2) .
Слайд 20

Азот
содержится в топливе многих видов ископаемых, например, в угле и нефти.
Из антропогенных источников выделяется около 93 % оксидов азота (II), который в результате химических реакций в атмосфере превращается в оксид азота (IV), который и образует с водой азотную кислоту.
Слайд 21

Природные источники оксидов азота - это грозовые разряды и молнии, а
также биогенные вещества. Летучие органические соединения, в отличие от оксидов серы и азота, поступают в атмосферу главным образом из природных источников (65% от общего количества). Основной источник этих веществ - растения, в результате жизнедеятельности которых образуются сложные органические вещества.
Слайд 22

Последствия кислотных
дождей в природе
В результате выпадения кислотных осадков нарушается равновесие в
экосистемах, ухудшается продуктивность сельскохозяйственных растений и питательные свойства почв.
Слайд 23

Последствия кислотных дождей
в технике
В результате коррозии разрушаются металлические конструкции.
Слайд 24

Последствия кислотных
дождей в архитектуре
Кислотные осадки разрушают сооружения из мрамора и известняка.
Исторические памятники Греции и Рима, простояв тысячелетия, за последние годы разрушаются прямо на глазах.
Слайд 25

Последствия
кислотных дождей
в архитектуре
Такая же судьба грозит
и Тадж-Махалу –
шедевру индийской
архитектуры
периода Великих моголов,
в Лондоне - Тауэру и
Вестминстерскому
аббатству…
Слайд 26

Последствия
кислотных дождей
архитектура
Слайд 27

Последствия
кислотных дождей
… в Санкт-Петербурге –
Казанскому собору,
Александро-Невской Лавре и др.
Слайд 28

Последствия кислотных дождей
в архитектуре
На соборе Св. Павла слой портлендского известняка
изъеден на 2.5 см.
В Голландии статуи на соборе Св. Иоанна "тают, как леденцы".
Черными отложениями, этим "раком камня", изъеден королевский дворец на площади Дам в Амстердаме.
Слайд 29

Задание
Закончите уравнения реакций,
назовите их тип.
N 2O5 + H2O =
Mg +
H2O =
Li+ H2O =
СaO + H2O =
Слайд 30

В природе путешествует Н2О.
Она не исчезает никогда.
То в снег превратится, то
в лед,
Растает и снова в поход.
По горным вершинам, широким долинам,
Вдруг в небо взорвется, дождями вернется,
Вокруг оглянись, в природу вглядись -
Вас окружает везде и всегда,
Это волшебное чудо – вода!
Слайд 31
Слайд 32

1.Одним словом
(именем существительным) выразите
тему сегодняшнего урока
2.Подберите к этому
слову 2
прилагательных
3. Подберите к этому слову 3 глагола
4. Составьте фразу, в которой будет
отражена значимость этого слова
5. Подберите синоним к этому слову.































 Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Влияние этилового спирта на организм детей
Влияние этилового спирта на организм детей Экоэстафета. ученики 9 Б класса гимназии №6 г. Гродно
Экоэстафета. ученики 9 Б класса гимназии №6 г. Гродно Основные понятия и законы химии. Тема1
Основные понятия и законы химии. Тема1 Пластмасса, пластикалық материалдар
Пластмасса, пластикалық материалдар Жесткость воды и способы её устранения
Жесткость воды и способы её устранения Фазовое равновесие
Фазовое равновесие Сильные и слабые электролиты. Кислотность среды. 9 класс
Сильные и слабые электролиты. Кислотность среды. 9 класс Соли аммония
Соли аммония Будова електронних оболонок атомів
Будова електронних оболонок атомів Свойства растворов высокомолекулярных соединений
Свойства растворов высокомолекулярных соединений Комплексные (или координационные) соединения
Комплексные (или координационные) соединения Транспортное обеспечение внесения удобрений
Транспортное обеспечение внесения удобрений Порівняльний аналіз методів відновлення свинцево-кислотних акумуляторів
Порівняльний аналіз методів відновлення свинцево-кислотних акумуляторів Теоретические основы биоорганической химии
Теоретические основы биоорганической химии Водород
Водород Экспресс-методы решения задач по химии
Экспресс-методы решения задач по химии Окисно-відновні реакції. 9 клас
Окисно-відновні реакції. 9 клас Химия 20 века
Химия 20 века Химическая связь. (Лекция 4, 5)
Химическая связь. (Лекция 4, 5) Окислительно - восстановительные реакции (ОВР) (часть 1)
Окислительно - восстановительные реакции (ОВР) (часть 1) Кристаллическое строение и кристаллизация металлов
Кристаллическое строение и кристаллизация металлов Полимеры и их использование
Полимеры и их использование Основные понятия и законы химии
Основные понятия и законы химии Тема Сплавы. Чугун
Тема Сплавы. Чугун ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ
ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ Мектепте химия пәнінен олипиядалық есептерді шешуде иондар қасиеттерінің маңызы
Мектепте химия пәнінен олипиядалық есептерді шешуде иондар қасиеттерінің маңызы