Содержание
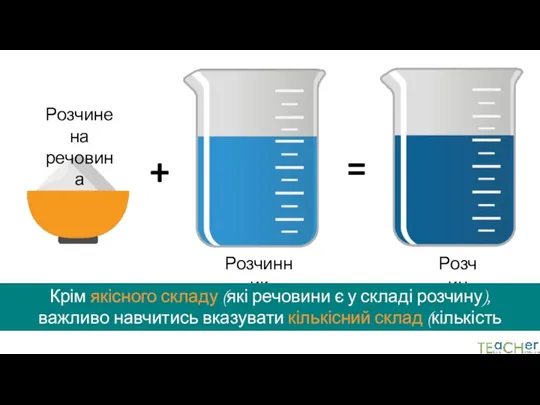
- 2. + = Розчинена речовина Розчинник Розчин Крім якісного складу (які речовини є у складі розчину), важливо
- 3. Масова частка розчиненої речовини Масова частка розчиненої речовини – це відношення маси речовини до маси всього
- 4. Масова частка показує, скільки г розчиненої речовини міститься у 100 г розчину У 100 г 9%-го
- 5. Задача 1. Натрій хлорид масою 6 г розчинили у воді масою 194 г. Яка масова частка
- 6. Задача 2. Скільки грамів натрій гідроксиду NaOH треба взяти для приготування 500 г розчину з масовою
- 8. Скачать презентацию




 Химиялық өнеркәсіп шикізаты . Шикізат көздері Химиялық өндірістегі энергия және энергия көздері
Химиялық өнеркәсіп шикізаты . Шикізат көздері Химиялық өндірістегі энергия және энергия көздері Кислоты. Определение рН кислоты, щелочи, воды
Кислоты. Определение рН кислоты, щелочи, воды Способы выражения концентрации в титриметрическом анализе
Способы выражения концентрации в титриметрическом анализе Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Получение и собирание газов. Практическая работа
Получение и собирание газов. Практическая работа Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Фенол, його властивості
Фенол, його властивості Геохимия урана и тория в магматическом процессе
Геохимия урана и тория в магматическом процессе Периодическая система элементов Д. И. Менделеева. IA группа
Периодическая система элементов Д. И. Менделеева. IA группа Свойства органических соединений
Свойства органических соединений Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент
Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины
Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины Описание проведения опыта. Зажгите свечу
Описание проведения опыта. Зажгите свечу Азотсодержащие органические соединения. Амины. Анилинароматический амин
Азотсодержащие органические соединения. Амины. Анилинароматический амин Классы неорганических соединений
Классы неорганических соединений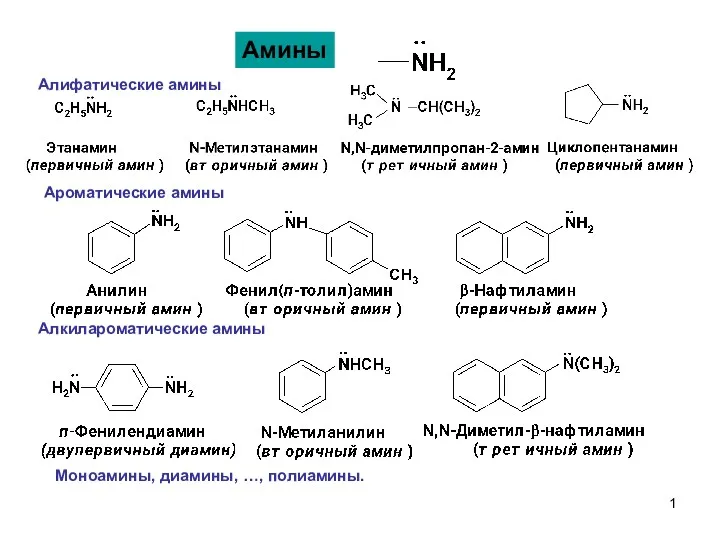 Амины-1
Амины-1 Хімічні формули речовин
Хімічні формули речовин Торий. Алынуы
Торий. Алынуы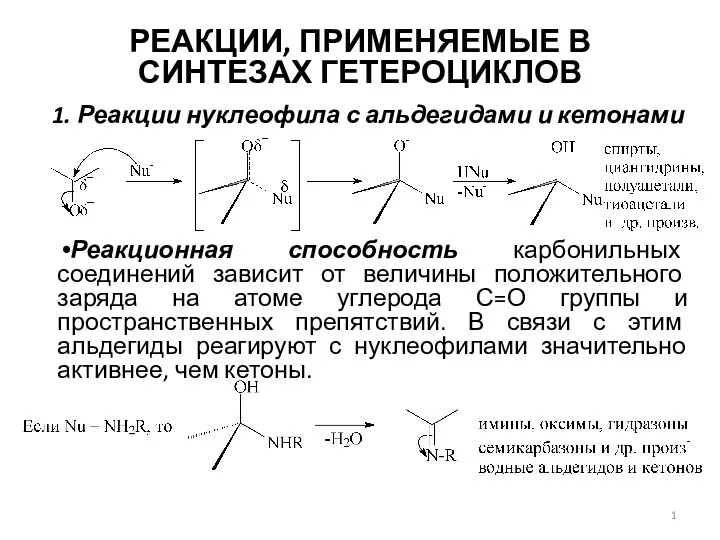 Реакции, применяемые в синтезах гетероциклов
Реакции, применяемые в синтезах гетероциклов Электролиттік диссоциациялану теориясы тұрғысынан қышқыл, негіз, тұздардың химиялық қасиеттері
Электролиттік диссоциациялану теориясы тұрғысынан қышқыл, негіз, тұздардың химиялық қасиеттері Спекание. Основные типы спекания
Спекание. Основные типы спекания Рафинирование от растворимых окислов
Рафинирование от растворимых окислов Хром
Хром Молибден. Нахождение в природе
Молибден. Нахождение в природе Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями
Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями Бытовая химия в нашем доме и альтернативные способы уборки
Бытовая химия в нашем доме и альтернативные способы уборки Жиры. История открытия, строение, классификация, свойства
Жиры. История открытия, строение, классификация, свойства Практическая работа № 3. Получение, собирание и распознавание газов
Практическая работа № 3. Получение, собирание и распознавание газов