Содержание
- 2. Цели и задачи работы: Научиться выделять информационную часть задания и экспериментальную учебную проблему. Уметь анализировать возможные
- 3. Оборудование и вещества Лабораторное оборудование: - штатив для пробирок, пробирки, шпатель, стеклянная палочка, лучинка, лабораторный штатив,
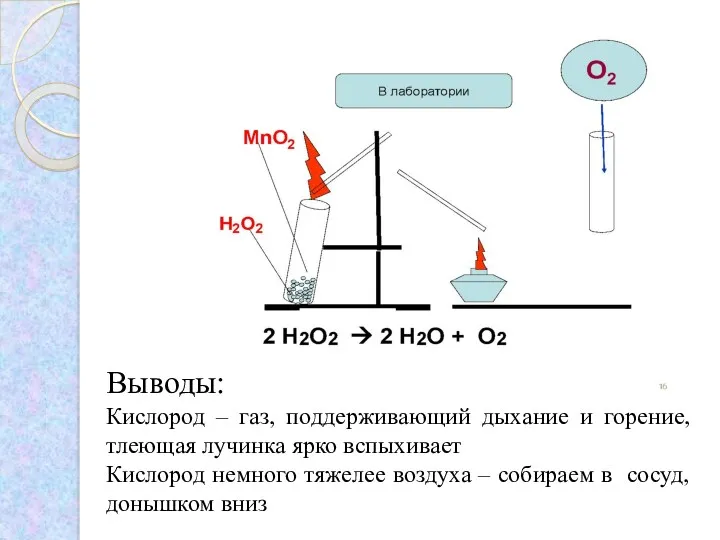
- 4. Опыт: Получение и собирание кислорода. Доказательство наличия кислорода в сосуде Возьмите 1 чистую сухую пробирку. Аккуратно
- 5. Выводы: Кислород – газ, поддерживающий дыхание и горение, тлеющая лучинка ярко вспыхивает Кислород немного тяжелее воздуха
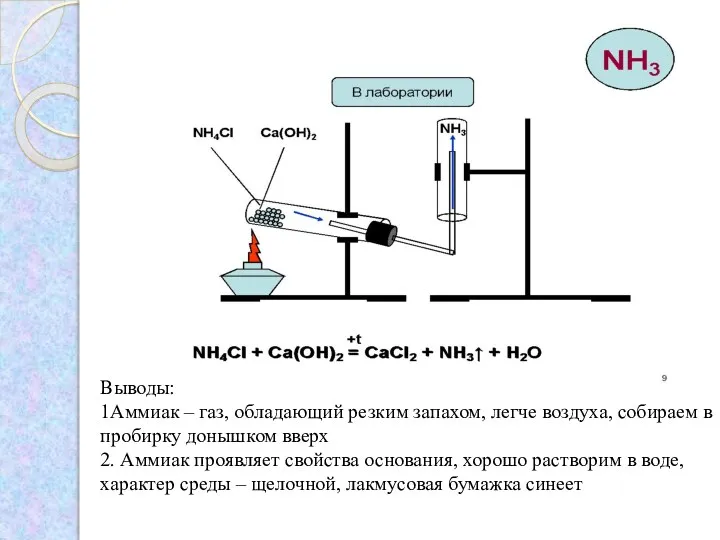
- 6. Опыт: Получение и собирание аммиака. Доказательство наличия аммиака в сосуде Возьмите 1 чистую сухую пробирку. Аккуратно
- 7. Выводы: 1Аммиак – газ, обладающий резким запахом, легче воздуха, собираем в пробирку донышком вверх 2. Аммиак
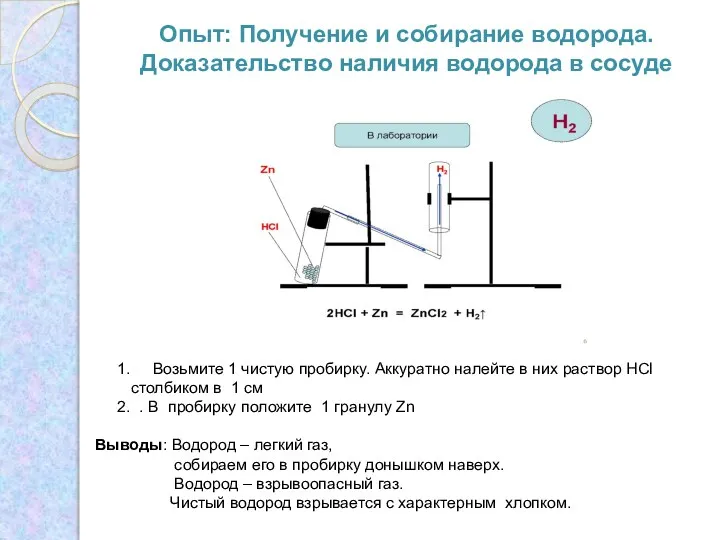
- 8. Опыт: Получение и собирание водорода. Доказательство наличия водорода в сосуде Возьмите 1 чистую пробирку. Аккуратно налейте
- 9. Опыт: Получение и собирание углекислого газа. Доказательство наличия углекислого газа в сосуде Возьмите 1 чистую сухую
- 11. Скачать презентацию





 20230814_obobshchenie_po_teme_nemetally
20230814_obobshchenie_po_teme_nemetally Биохимия и молекулярная биология. Биосинтез мембранных липидов. Лекция 9
Биохимия и молекулярная биология. Биосинтез мембранных липидов. Лекция 9 Задачі на визначення ступеню електролітичної дисоціації
Задачі на визначення ступеню електролітичної дисоціації Элемент № 24 периодической таблицы. Хром
Элемент № 24 периодической таблицы. Хром Белки – высокомолекулярные природные соединения (биополимеры)
Белки – высокомолекулярные природные соединения (биополимеры) Материаловедение. Строение вещества. Металлы и сплавы
Материаловедение. Строение вещества. Металлы и сплавы Химическая промышленность
Химическая промышленность Окислительно – восстановительные реакции
Окислительно – восстановительные реакции Амины. Анилин
Амины. Анилин Чистые вещества и смеси
Чистые вещества и смеси Углеводы. Моносахариды. Дисахариды. Полисахариды
Углеводы. Моносахариды. Дисахариды. Полисахариды Облагораживание тяжелых нефтей и природных битумов
Облагораживание тяжелых нефтей и природных битумов Предмет химии. Вещества
Предмет химии. Вещества Задачи
Задачи Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Менделеевские уроки. День науки
Менделеевские уроки. День науки Химический элемент алюминий
Химический элемент алюминий Иодометрия. Комплексиметрия (начало)
Иодометрия. Комплексиметрия (начало) Высокомолекулярные вещества и их растворы
Высокомолекулярные вещества и их растворы Азот. Физические и химические свойства. Распространенность азота в природе. Способы получения
Азот. Физические и химические свойства. Распространенность азота в природе. Способы получения Природный и попутный нефтяной газы
Природный и попутный нефтяной газы Простые вещества. Металлы и неметаллы
Простые вещества. Металлы и неметаллы Электрохимические процессы. Лекция 7
Электрохимические процессы. Лекция 7 Вещества и их превращения Роль химии в нашей жизни
Вещества и их превращения Роль химии в нашей жизни Общая характеристика неметаллов
Общая характеристика неметаллов Физико-химические свойства органических веществ. Номенклатура, изомерия, задачи
Физико-химические свойства органических веществ. Номенклатура, изомерия, задачи Химические основы жизни
Химические основы жизни Обобщающий урок по теме Металлы
Обобщающий урок по теме Металлы