Содержание
- 2. Мета Розглянути поняття феноли, як похідні бензену Ознайомити з будовою фенолів, фізичними та хімічними властивостями Добування
- 3. Очікувані результати Знати: *молекулярну, структурну та електронну формули фенолу Вміти: *розрізняти фенол *записувати рівняння хімічних реакцій
- 4. «Мікрофон» Дайте визначення спиртів. Назвіть функціональну групу спиртів та поясніть як вона сполучена в молекулі спирту.
- 5. Феноли – це ароматичні сполуки, до складу яких входять гідроксильні групи, зв’язані з бензеновим ядром.
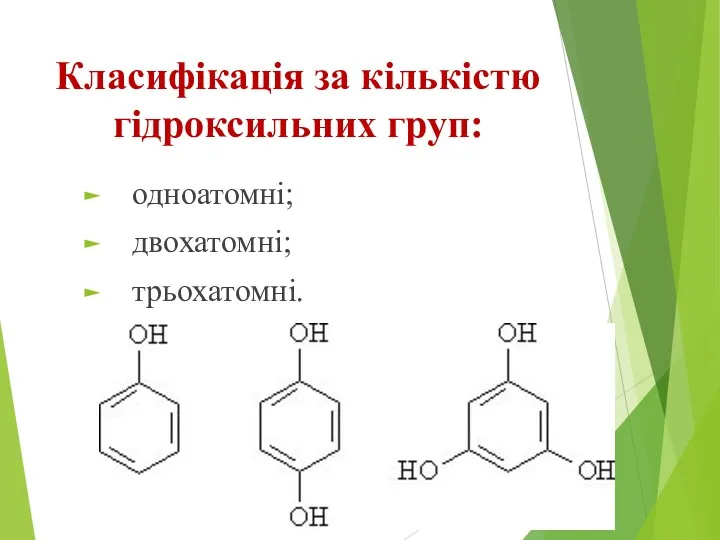
- 6. Класифікація за кількістю гідроксильних груп: одноатомні; двохатомні; трьохатомні.
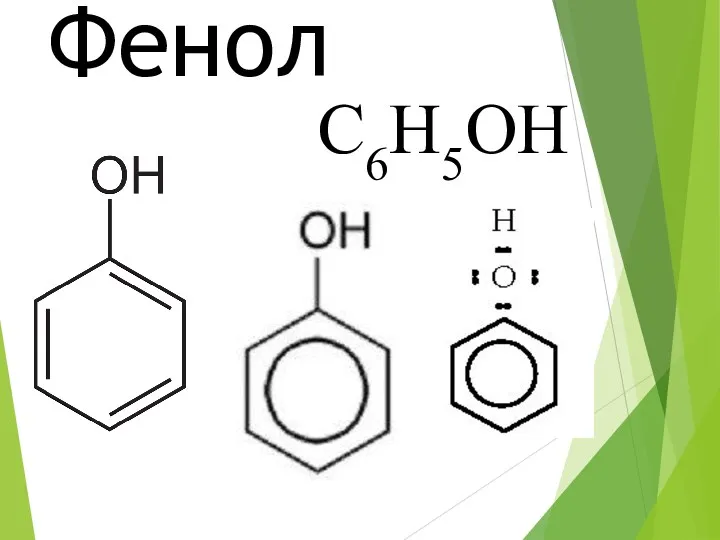
- 7. Фенол C6H5OH
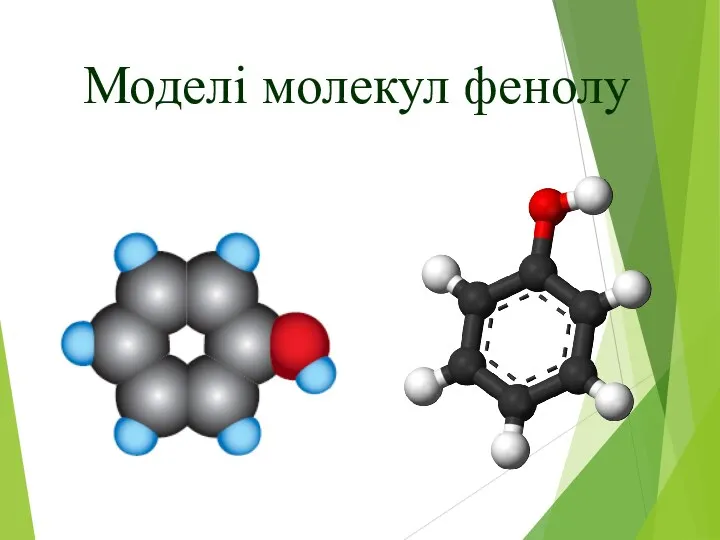
- 8. Моделі молекул фенолу
- 9. Політична карикатура на події 1888—1889 років у Румунії: за допомогою фенолу, потужного дезінфектанту, новий уряд на
- 10. Фізичні властивості кристалічна безбарвна речовина з характерним запахом нерозчинна у холодній воді при t= 60°C розчинність
- 11. розчин фенолу у воді називається карболовою кислотою (карболка), яка проявляє слабкі кислотні властивості. ОН група не
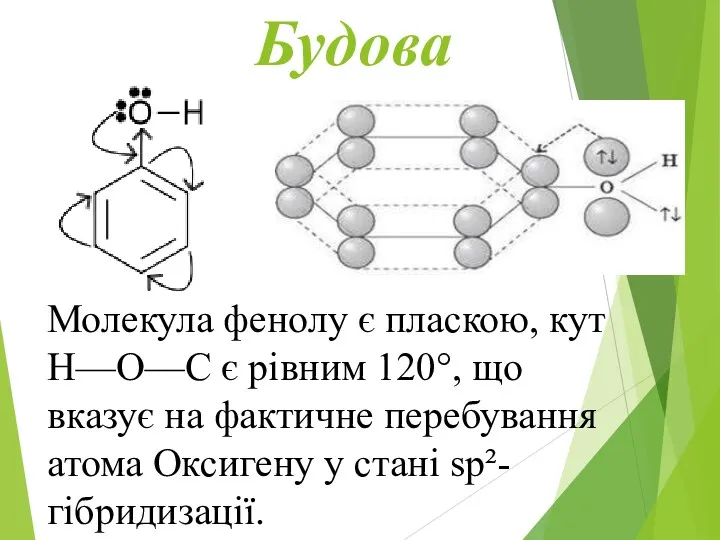
- 12. Будова Молекула фенолу є пласкою, кут H—O—C є рівним 120°, що вказує на фактичне перебування атома
- 13. Хімічні властивості Реакції за участі ОН-групи: - взаємодіє з металічним Na: 2C6H5OH + 2Na = 2C6H5ONa
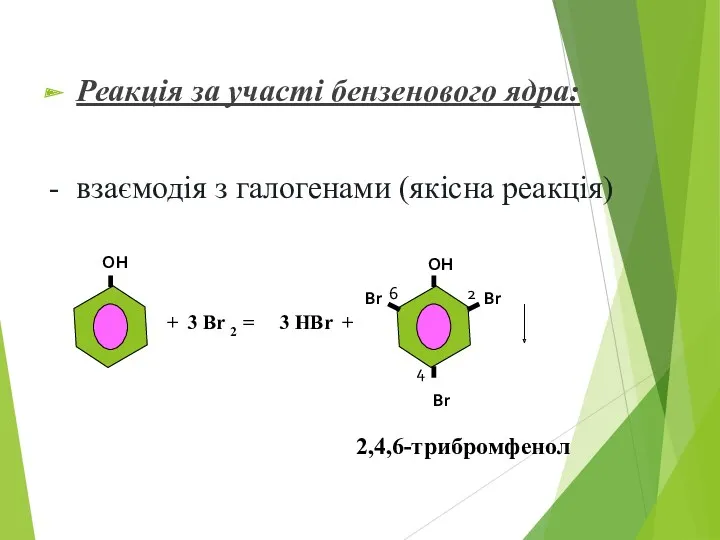
- 14. Реакція за участі бензенового ядра: - взаємодія з галогенами (якісна реакція) + 3 Br 2 =
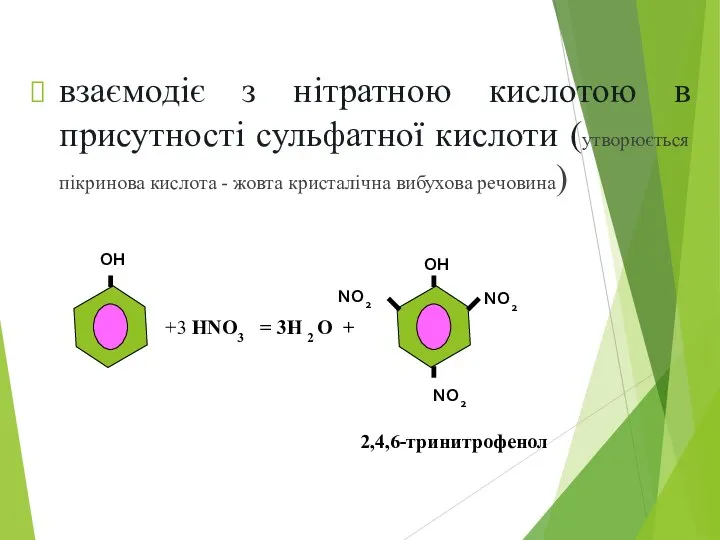
- 15. взаємодіє з нітратною кислотою в присутності сульфатної кислоти (утворюється пікринова кислота - жовта кристалічна вибухова речовина)
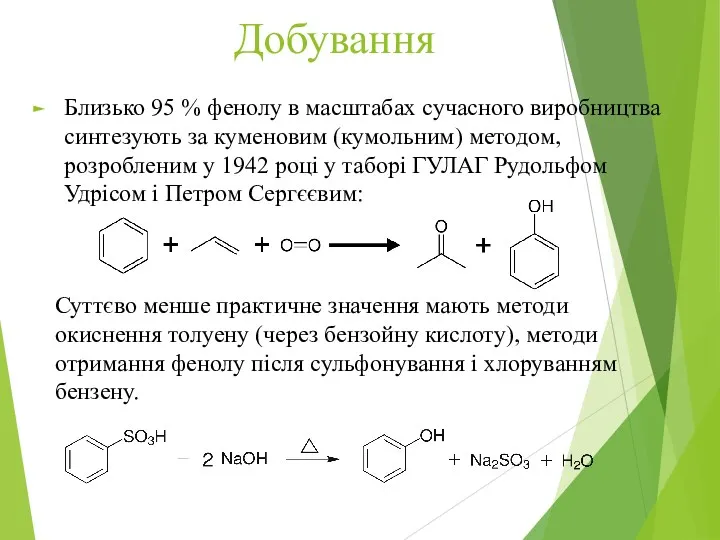
- 16. Добування Близько 95 % фенолу в масштабах сучасного виробництва синтезують за куменовим (кумольним) методом, розробленим у
- 17. Застосування в медицині як антисептик (карболка) для виробництва фенолформальдегідних пластмас. виробництво барвників, лікарських препаратів і вибухових
- 18. Методи нейтралізації фенолу та його похідних каталітичне окиснення газів, що містять фенол. виділення фенолу розчинниками. знезараження
- 22. Скачать презентацию











 Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Соединения железа
Соединения железа Галогены - химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева
Галогены - химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева Алканы. Строение, номенклатура, изомерия, химические и физические свойства
Алканы. Строение, номенклатура, изомерия, химические и физические свойства Общая характеристика неметаллов
Общая характеристика неметаллов Титан. Хром
Титан. Хром Современные проблемы молекулярной биологии
Современные проблемы молекулярной биологии Хімічні властивості кислот
Хімічні властивості кислот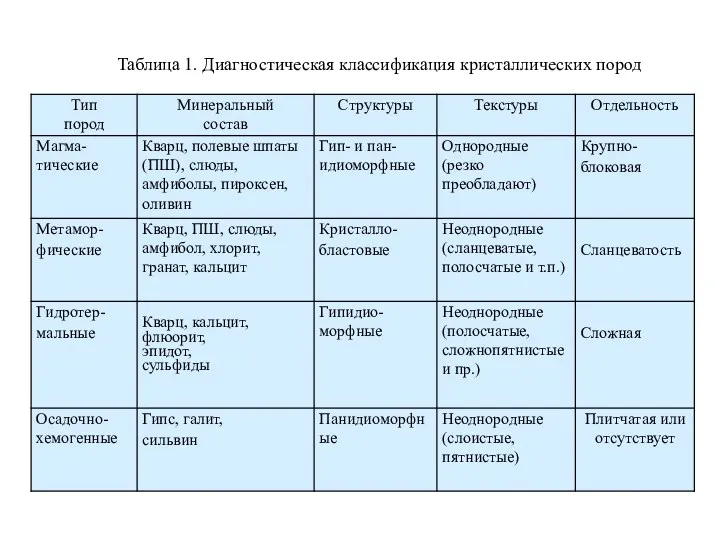 Диагностика метаморфических и гидротермальных горных пород
Диагностика метаморфических и гидротермальных горных пород Нуклеиновые кислоты
Нуклеиновые кислоты Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар
Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар Аммиак. Строение атома азота
Аммиак. Строение атома азота Азотсодержащие соединения. Амины. Аминокислоты
Азотсодержащие соединения. Амины. Аминокислоты Organic molecules
Organic molecules Щелочные металлы
Щелочные металлы Чисті речовини і суміші
Чисті речовини і суміші Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Полимерные материалы, пластмассы и изделия из них
Полимерные материалы, пластмассы и изделия из них Поливинилхлорид
Поливинилхлорид Неметаллы. Занятие 20
Неметаллы. Занятие 20 Омыватель лобового стекла
Омыватель лобового стекла Неон (Ne)
Неон (Ne) Основные разделы химии
Основные разделы химии Строение атома
Строение атома Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент
Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент Химия нефти и газа
Химия нефти и газа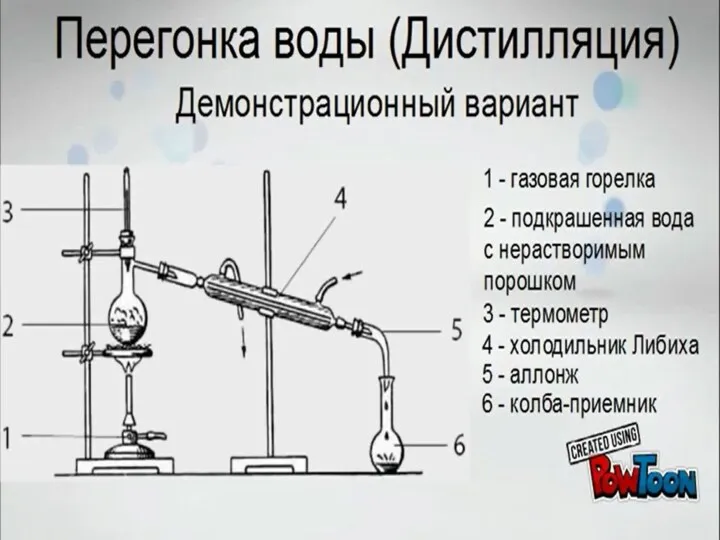 Перегонка воды (дистилляция). Демонстрационный вариант
Перегонка воды (дистилляция). Демонстрационный вариант Водород. Строение, свойства, получение, применение
Водород. Строение, свойства, получение, применение