Содержание
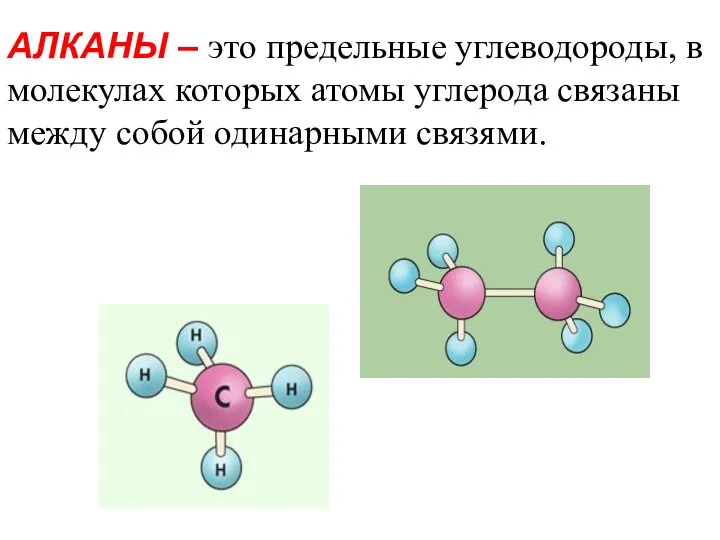
- 2. АЛКАНЫ – это предельные углеводороды, в молекулах которых атомы углерода связаны между собой одинарными связями.
- 3. Общая формула СnH2n+2 , где n=1,2,3…
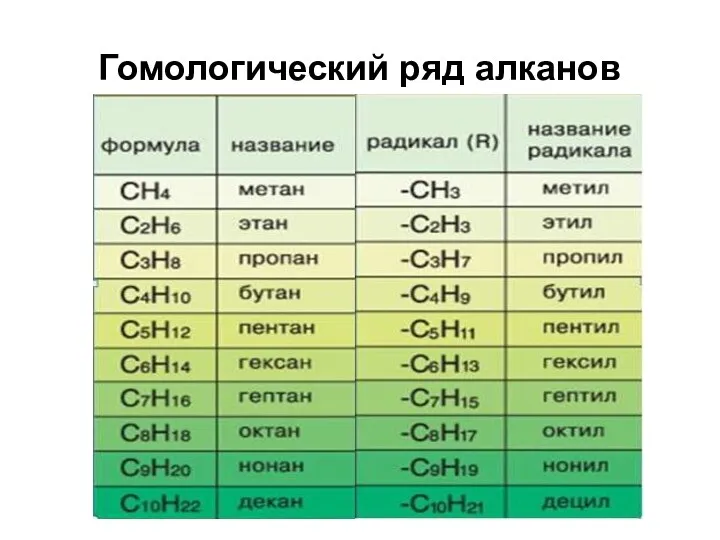
- 4. Гомологический ряд алканов
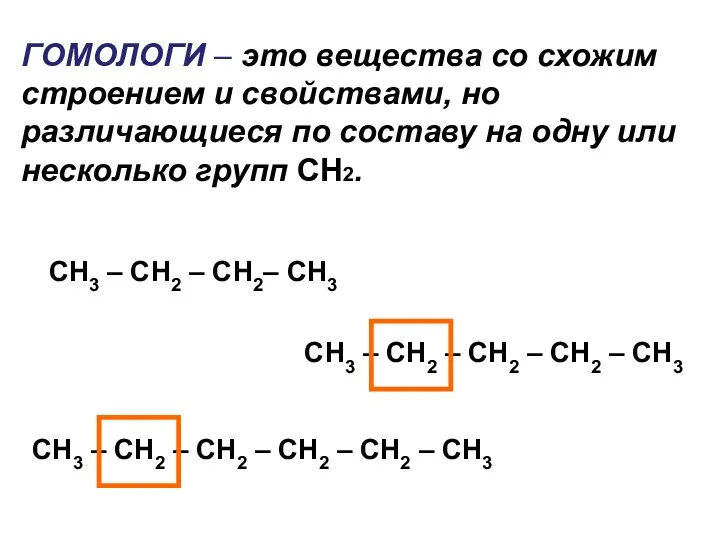
- 5. ГОМОЛОГИ – это вещества со схожим строением и свойствами, но различающиеся по составу на одну или
- 6. ИЗОМЕРЫ – вещества, имеющие одинаковый состав молекул, но различное химическое строение и обладающие поэтому разными свойствами.
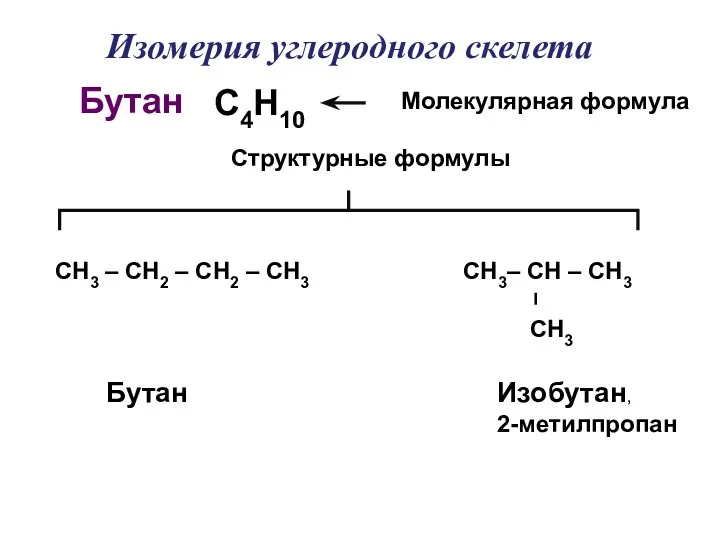
- 7. С4Н10 СН3 – СН2 – СН2 – СН3 Молекулярная формула Структурные формулы Бутан Бутан Изобутан, 2-метилпропан
- 8. НОМЕНКЛАТУРА АЛКАНОВ Алгоритм: Выбор главной, самой длинной цепи: CH3 – CH - CH2 - CH3 │
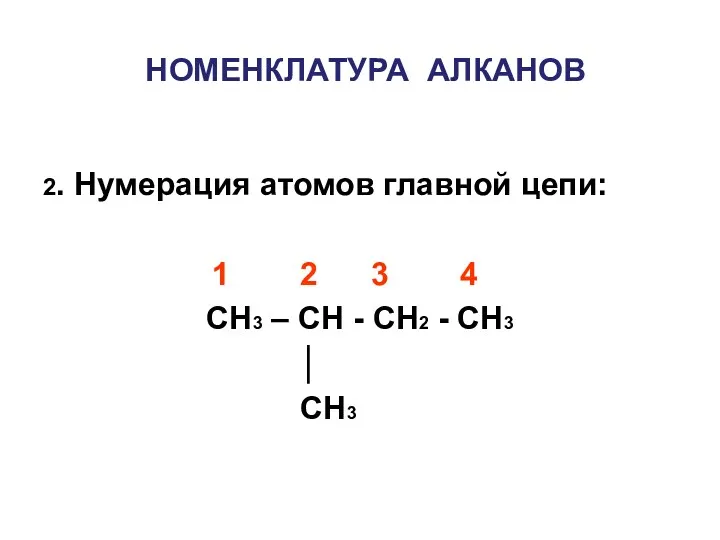
- 9. НОМЕНКЛАТУРА АЛКАНОВ 2. Нумерация атомов главной цепи: 1 2 3 4 CH3 – CH - CH2
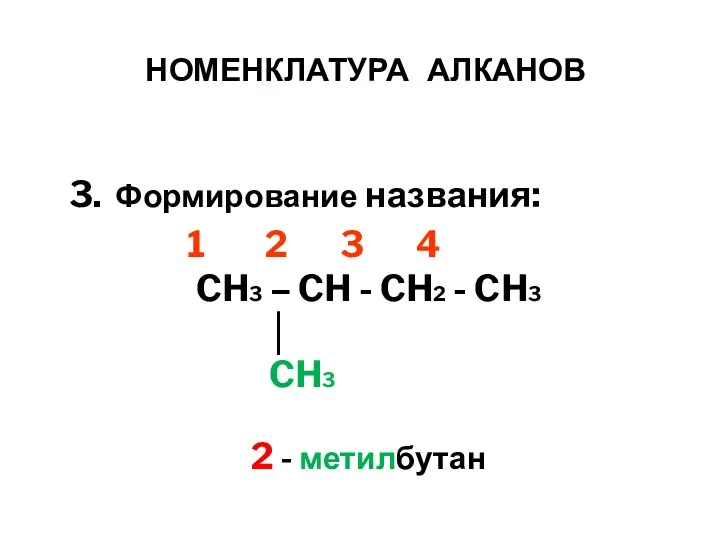
- 10. НОМЕНКЛАТУРА АЛКАНОВ 3. Формирование названия: 1 2 3 4 CH3 – CH - CH2 - CH3
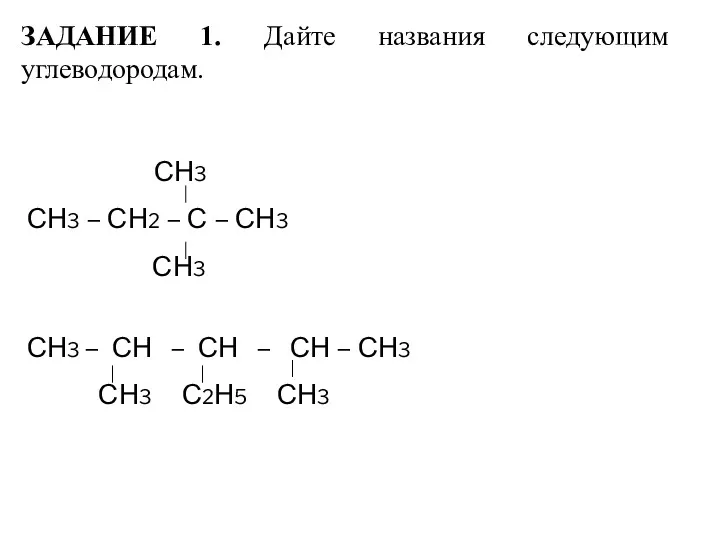
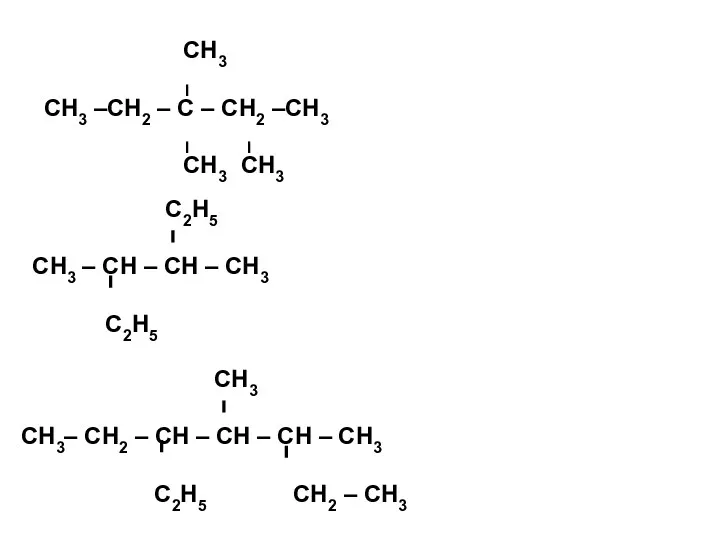
- 11. ЗАДАНИЕ 1. Дайте названия следующим углеводородам. СН3 СН3 – СН2 – С – СН3 СН3 СН3
- 12. СН3 І СН3 –СН2 – С – СН2 –СН3 І І СН3 СН3
- 13. ЗАДАНИЕ 2. Составьте структурные формулы следующих веществ: 1. 2,3 – диметилпентан; 2. 3,3,4 – триметилгексан; 3.
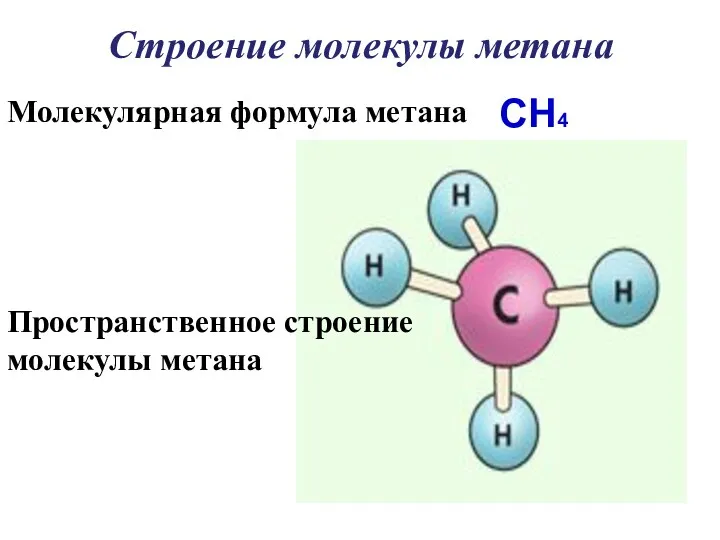
- 14. Строение молекулы метана Молекулярная формула метана CH4 Пространственное строение молекулы метана
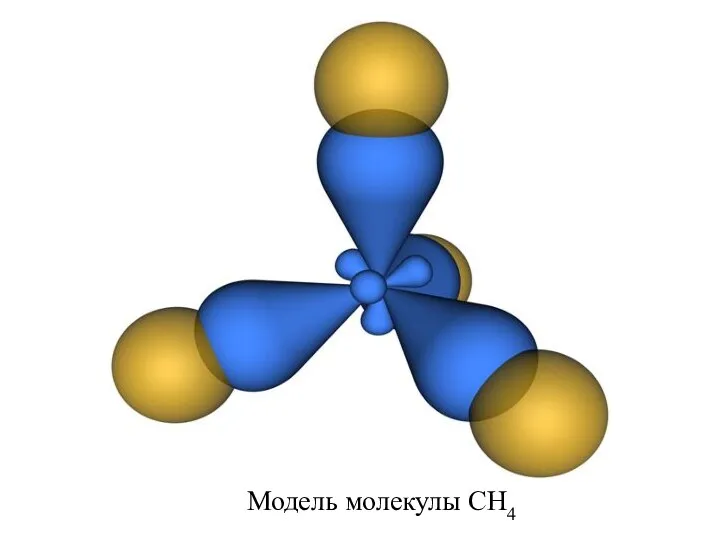
- 15. Модель молекулы CH4
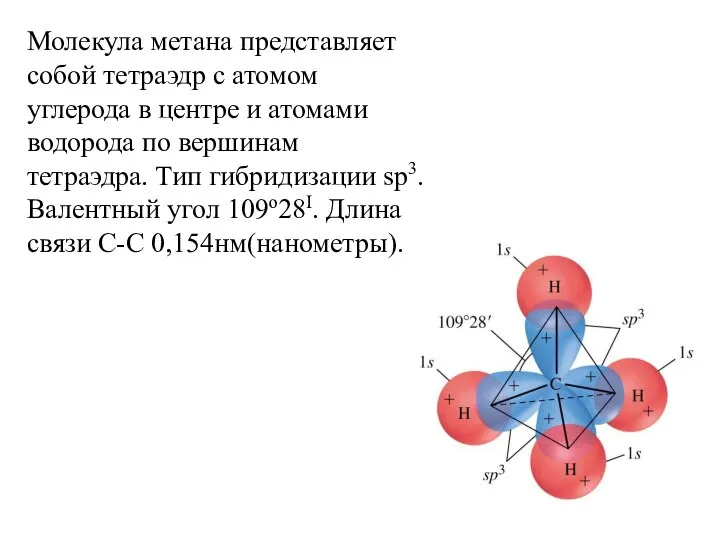
- 16. Молекула метана представляет собой тетраэдр с атомом углерода в центре и атомами водорода по вершинам тетраэдра.
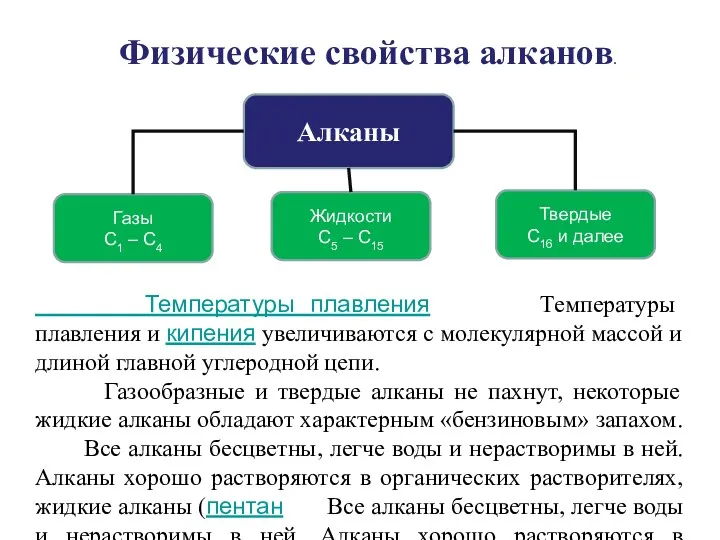
- 17. Алканы Жидкости С5 – С15 Газы С1 – С4 Твердые С16 и далее Физические свойства алканов.
- 18. 1. Реакции замещения Протекают по механизму радикального замещения. а) с галогенами (с Cl2 – на свету,
- 19. 2. Реакции окисления CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O CH4 + 2O2 → CO2 +
- 20. 3. Термические превращения алканов а) дегидрирование(отщепление водорода) в присутствии катализатора при высоких температурах : CH3 –
- 21. в) крекинг - это реакция разложения алкана с длинной углеродной цепью на алканы и алкены с
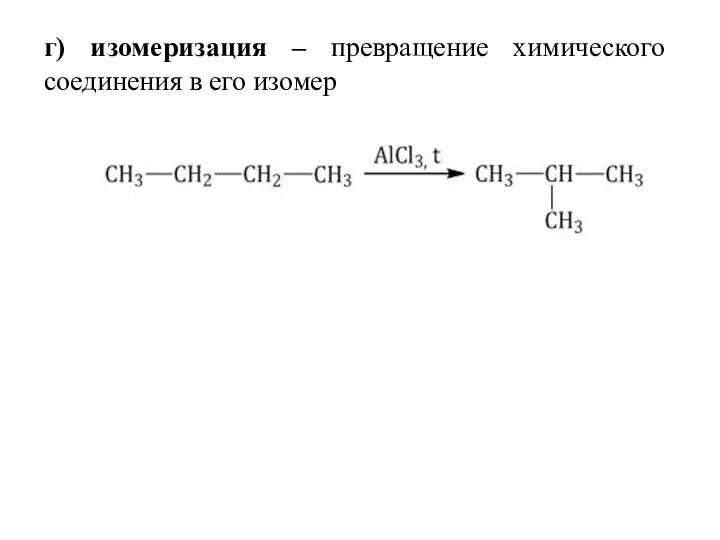
- 22. г) изомеризация – превращение химического соединения в его изомер
- 23. Способы получения
- 24. Задания для самостоятельной работы: Задание 1. Назовите вещества
- 26. Скачать презентацию










 Гидролиз. Применение гидролиза. (11 класс)
Гидролиз. Применение гидролиза. (11 класс) Сероводород. Сульфиды
Сероводород. Сульфиды Растворы. Реакции ионного обмена. Гидролиз солей
Растворы. Реакции ионного обмена. Гидролиз солей Предельные одноатомные спирты
Предельные одноатомные спирты Пластмассы
Пластмассы Вирощення кристталів
Вирощення кристталів Химическая связь
Химическая связь Свойства минералов
Свойства минералов Метал конструкциялық материалдар
Метал конструкциялық материалдар Классы неорганических веществ
Классы неорганических веществ Теория строения органических соединений
Теория строения органических соединений Історичні відомості про способи класифікації хімічних елементів. Поняття про лужні метали, галогени, інертні гази
Історичні відомості про способи класифікації хімічних елементів. Поняття про лужні метали, галогени, інертні гази Тағамдық қоспалар. Тағамдық бояулар. Антиоксиданттар. Эмульгаторлар
Тағамдық қоспалар. Тағамдық бояулар. Антиоксиданттар. Эмульгаторлар Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях Фенолы
Фенолы Стирка по научному
Стирка по научному Кислоты. Определение и классификация
Кислоты. Определение и классификация Магматические горные породы
Магматические горные породы Соединения железа
Соединения железа Титриметрический анализ. Кривые титрования
Титриметрический анализ. Кривые титрования Химические свойства основных классов неорганических веществ
Химические свойства основных классов неорганических веществ Эфирные масла
Эфирные масла Көмірсутектерді пиролиздеу арқылы қарапайым олефиндерді алу
Көмірсутектерді пиролиздеу арқылы қарапайым олефиндерді алу Классы неорганических соединений
Классы неорганических соединений Предельные углеводороды и их производные
Предельные углеводороды и их производные Кислоты. Классификация кислот, их химические свойства
Кислоты. Классификация кислот, их химические свойства Технологическое проектирование процессов переработки пэн
Технологическое проектирование процессов переработки пэн Электролитическая диссоциация
Электролитическая диссоциация