Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах презентация
Содержание
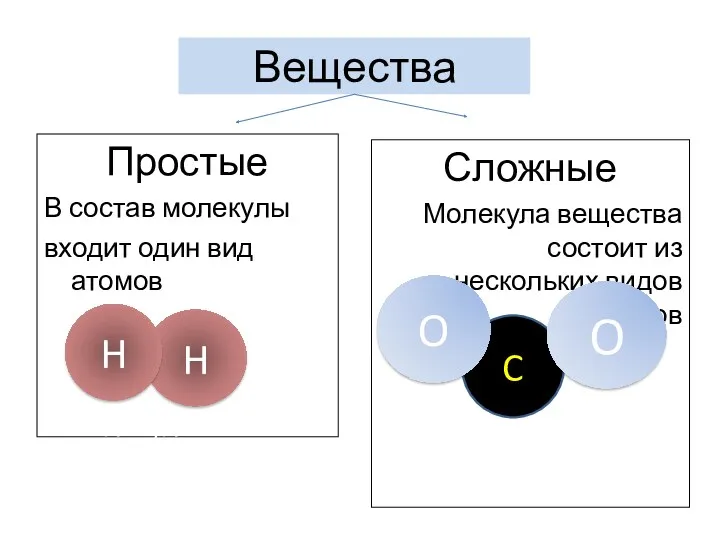
- 2. Вещества Простые В состав молекулы входит один вид атомов в состав молекулы веществв состав молекулы вD
- 4. Формулы веществ Химическая формула – это условная запись состава вещества, посредствам химических знаков и символов.
- 5. Для записи формул веществ: 1.знаки химических элементов 2. индекс 3. коэффициент
- 6. Задание: 1. 3H 2. 5H2 3. Fe 4. HNO3 5. 4H2СO3
- 7. Напишите формулы: 1. 5атомов меди 2. атом серы 3. молекула кислорода, состоящая из двух атомов 4.
- 8. 5H2СO3 Коэффициент - показывает число молекул или атомов Индекс – показывает число атомов в молекуле. Знаки
- 9. Задание: Переведите текстовую информацию в символическую: 1).Две молекулы озона. В состав каждой молекулы входят 3 атома
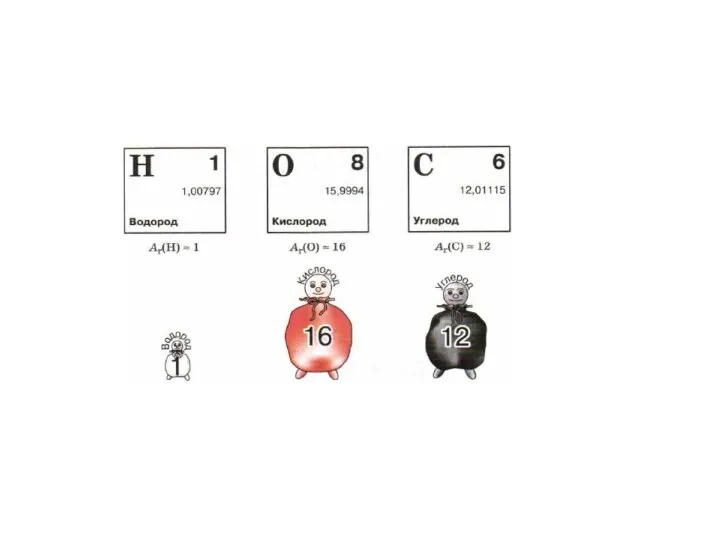
- 10. Относительная атомная масса Ar Относительная молекулярная масса Mr
- 11. Относительная масса атома mат (Н) = 0,000 000 000 000 000 000 000 001674 г =
- 12. mат (Н) = 0,000 000 000 000 000 000 000 001674 г = 0,1674∙10-23 г mат
- 14. II. Нахождение Ar с помощью периодической системы. Правила округления: - если после запятой стоит цифра меньше
- 15. ОТНОСИТЕЛЬНАЯ МОЛЕКУЛЯРНАЯ МАССА Мr(Н2О) = 2∙Ar(H) + A r(O) = 2∙1 + 16 = 18 Мr(Н2SО4)
- 17. Вычисление массовых долей элементов в сложных веществах Задача №1 . Вычислить массовые доли элементов в серной
- 18. Задача №2 Для получения железа (выплавки) используют железные руды: магнитный железняк Fe3O4 , красный железняк Fe2O3
- 20. Скачать презентацию
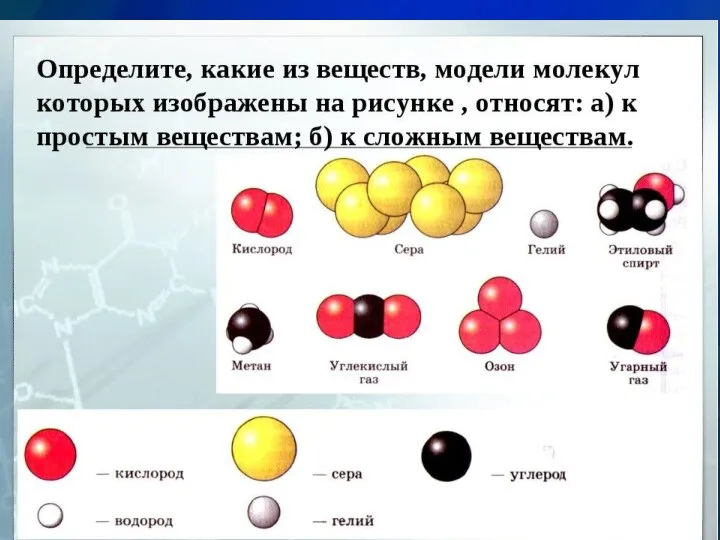














 Запись атомов и молекул с помощью химических символов
Запись атомов и молекул с помощью химических символов Химия элементов
Химия элементов Природні гази
Природні гази Синтетичні високомолекулярні речовини. Полімери. Реакції полімеризації і поліконденсації
Синтетичні високомолекулярні речовини. Полімери. Реакції полімеризації і поліконденсації Чистые вещества, смеси
Чистые вещества, смеси Горение топлива
Горение топлива Типы расчетных задач, способы их решения. Задания 39-40
Типы расчетных задач, способы их решения. Задания 39-40 a27156dfd11d4f939d9a0cf3023d54c5
a27156dfd11d4f939d9a0cf3023d54c5 Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота Периодическая система Д.И. Менделеева и строение атома
Периодическая система Д.И. Менделеева и строение атома Термодинамика химических процессов
Термодинамика химических процессов Ароматические углеводороды. Арены
Ароматические углеводороды. Арены Биополимеры. Классификация полисахаридов (гликаны)
Биополимеры. Классификация полисахаридов (гликаны) Тефлон. Что такое тефлон?
Тефлон. Что такое тефлон? Характеристика металу Ферум
Характеристика металу Ферум Металлы и неметаллы
Металлы и неметаллы Нанотехнологии в школьном образовании. Семинар учителей химии
Нанотехнологии в школьном образовании. Семинар учителей химии Переработка нефти. Крекинг
Переработка нефти. Крекинг Коррозия металлов
Коррозия металлов α-Аминокислоты и белки
α-Аминокислоты и белки Сульфидтер. Аз еруші сульфидтер
Сульфидтер. Аз еруші сульфидтер Классификация минералов по химическому принципу. Занятие 14
Классификация минералов по химическому принципу. Занятие 14 Соляная кислота (HCI)
Соляная кислота (HCI) Кристаллические решетки
Кристаллические решетки Водневий показник ph
Водневий показник ph Поверхностные явления. Типы поверхностных явлений
Поверхностные явления. Типы поверхностных явлений Стирка по научному
Стирка по научному Тайна великого открытия периодической таблицы
Тайна великого открытия периодической таблицы