Слайд 2 ЖОСПАР:
Теориялық кіріспе
а) Дебай-Гюккель I жуықтауы б) Индивидуалды ғылыми жұмыста Дебай-Гюккель
І жуықтауын пайдаланып есептелген мәндер
в)Графикалық сызбалар
Қорытынды
Слайд 3ТЕОРИЯЛЫҚ КІРІСПЕ:
1923Ж ДЕБАЙ ЖӘНЕ ХЮККЕЛЬМЕН АЙТЫЛҒАН. ЭЛЕКТРОЛИТТЕРДІҢ СТАТИСТИКАЛЫҚ ТЕОРИЯСЫ КЕЛЕСІ ЖАҒДАЙЛАРҒА СӘЙКЕС КЕЛЕДІ:
ИОНДАР ЕРІТІНДІ КӨЛЕМІНДЕ РЕТСІЗ ТАРАЛМАЙ, КУЛОННЫҢ ӘСЕРЛЕСУ ЗАҢЫНА СӘЙКЕС ТАРАЛҒАН. ЖЕКЕ ИОНДАРДЫҢ ЖАН-ЖАҒЫНДА ИОН АТМОСФЕРАСЫ (ИОН БҰЛТЫ) БАР – ОЛ ҚАРАМА – ҚАРСЫ ЗАРЯДТАЛҒАН ИОННАН ТҰРАТЫН СФЕРА. СФЕРА ҚҰРАМЫНА КІРЕТІН ИОНДАР ҮЗДІКСІЗ БАСҚА ИОНДАРМЕН ОРНЫН АУЫСТЫРЫП ОТЫРАДЫ. ЕРІТІНДІДЕГІ БАРЛЫҚ ИОНДАР БІРДЕЙ (ТЕҢ), ОЛАРДЫҢ ӘРБІРЕУІ ИОНДЫҚ АТМОСФЕРАСЫМЕН ҚОРШАЛҒАН, СОНЫМЕН ҚАТАР ЦЕНТРЛІК ИОН БАСҚА ИОННЫҢ ИОНДЫҚ АТМОСФЕРАСЫНЫҢ ҚҰРАМЫНА КІРЕДІ.
Слайд 4 ЭРИХ ХЮККЕЛЬ ПЕТЕР ДЕБАЙ
ДЕБАЙ-ХЮККЕЛЬ ТЕОРИЯСЫ МЫНАДАЙ ЕКІ ЖАҒДАЙҒА НЕГІЗДЕЛГЕН:
1) КҮШТІ ЭЛЕКТРОЛИТТЕР
ЕРІТІНДІДЕ ТОЛЫҒЫМЕН ДИССОЦИАЦИЯЛАНАДЫ(А=1)
2) КҮШТІ ЭЛЕКТРОЛИТТЕРДІҢ ИДЕАЛ ЕРІТІНДІДЕН АУЫТҚУЫ ИОНДАР АРАСЫНДАҒЫ ЭЛЕКТРОСТАТИКАЛЫҚ КҮШЬЕРДІҢ ӘСЕРІНЕН БОЛ
Слайд 5
Дебай-Хюккельдің бірінші жуықтауы
Слайд 6 ТАПСЫРМА №5
0,001; 0,006; 0,04; 0,01 М КОНЦЕНТРАЦИЯЛАРЫ БАР
COSO4 ҚОСЫЛЫСТАР ҮШIН ОРТАША-ИОНДЫҚ
АКТИВТIЛIК
КОЭФФИЦИЕНТТI БIРIНШI ДЕБАЙ-ХЮККЕЛЬ
ЖУЫҚТАУЛАРЫ МЕН 25, 35, 45, 65 КЕЗIНДЕГI ТЕҢДЕУЛЕРI БОЙЫНША ЕСЕПТЕ.
A) СУЛЫ ОРТАДА
B) ЭТИЛ СПИРТІ ОРТАДА
АЛЫНҒАН МӘНДЕР БОЙЫНША ОРТАША-ИОНДЫҚ АКТИВТIЛIК
КОЭФФИЦЕНТ ПЕН ИОНДЫҚ АТМОСФЕРА ҚАЛЫҢДЫҒЫНА
БАРЛЫҚ АТАП ӨТIЛГЕН ФАКТОРЛАРДЫҢ ӘСЕРI ТУРАЛЫ
ҚОРЫТЫНДЫ ЖАСА.
Слайд 7Сулы ортада әртүрлі температурадағы орташа-иондық активтiлiк коэффициенттiң концентрацияға тәуелділігі:
Слайд 8Этил спирті ортасында әртүрлі температурадағы орташа-иондық активтiлiк коэффициенттiң концентрацияға тәуелділігі:
Слайд 12 Қорытынды:
Дебай-Хюккель жуықтауларын пайдалана отырып берілген ерітіндінің орташа-иондық активтілік коэффициенттерін тауып мынадай
тұжырым жасадық: орташа-иондық активтiлiк коэффициент пен иондық атмосфера қалыңдығына концентрация мен температура әсер етеді. Графикте көрсетілгендей концентрация мен температура артқан сайын иондық атмосфера қалыңдығы артады, себебі температура жоғарлағанда иондардың жылулық қозғалыс әсерінен иондық атмосфера кеңейсе,ал концентрация артқан сайын иондық атмосфера жанында иондар жиналады.Ал орташа иондық активтілік коэффициенті температура мен концентрация артқан сайын кемиді,себебі электростатикалық және электоферротикалық күштер әсер етеді.Бөлшектер көбеюінен иондардың жылдамдығы азаяды.Спирттік ортада иондық атмосфера қалыңдығы сулы ортадан жоғары болады,өйткені спирттік ортада күшті электорлиттер әлсіз электролитке айналып сутектік байланыс түзуге бейім болады.
 Силикатная промышленность. 9 класс
Силикатная промышленность. 9 класс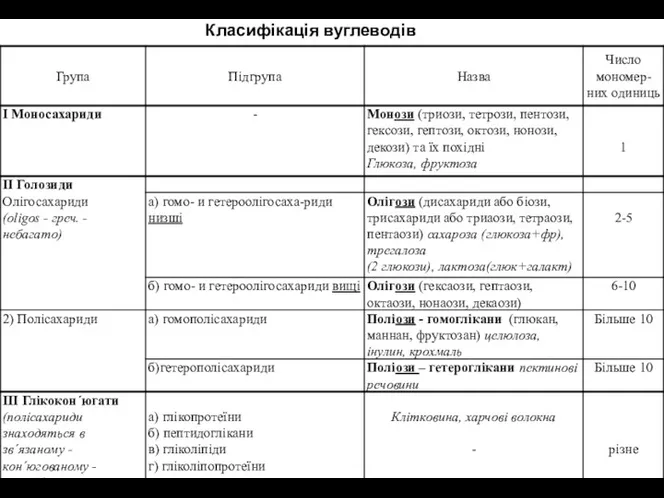 Вуглеводи. Лекція
Вуглеводи. Лекція Le trasformazioni fisiche della materia. Tema 3
Le trasformazioni fisiche della materia. Tema 3 Природній та супутній нафтові гази, їх склад, використання
Природній та супутній нафтові гази, їх склад, використання Установка первичной переработки нефти ЭЛОУ-АТ-1
Установка первичной переработки нефти ЭЛОУ-АТ-1 20230205_okislitelno-_vosstanovitelnye_reaktsii
20230205_okislitelno-_vosstanovitelnye_reaktsii Тепловые эффекты химических реакций
Тепловые эффекты химических реакций Непредельные, ненасыщенные, ацетиленовые алкины
Непредельные, ненасыщенные, ацетиленовые алкины 20230330_zakony_termodinamiki_i_kinetika
20230330_zakony_termodinamiki_i_kinetika Electron configuration and periodicity
Electron configuration and periodicity Подготовительные курсы для абитуриентов химического факультета БГУ
Подготовительные курсы для абитуриентов химического факультета БГУ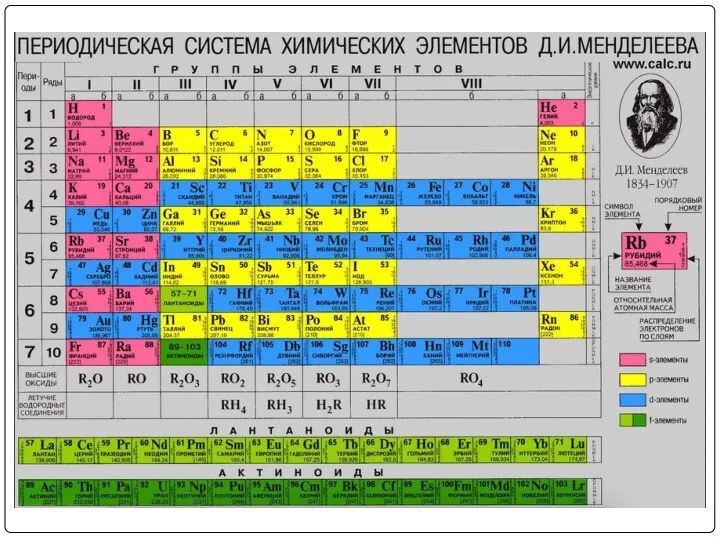 Аммиак. Происхождение названия
Аммиак. Происхождение названия Атмосфера. Химия стратосферы
Атмосфера. Химия стратосферы Производство бензина
Производство бензина π-комплексы металлов. Природа связи металлуглерод в π-комплексах металлов. Отличия в свойствах от обычной σ-связи
π-комплексы металлов. Природа связи металлуглерод в π-комплексах металлов. Отличия в свойствах от обычной σ-связи Закономерность изменений в строении электронных оболочек атома
Закономерность изменений в строении электронных оболочек атома Типовые процессы технологии неорганических веществ. (Тема 3)
Типовые процессы технологии неорганических веществ. (Тема 3) Берилій
Берилій Химические свойства солей
Химические свойства солей Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Кремнийдің құрамы, құрылысы және қасиеттері
Кремнийдің құрамы, құрылысы және қасиеттері Химический элемент гелий
Химический элемент гелий Оксиды углерода
Оксиды углерода Нефтепродукты в косметическом производстве. Биологически активные вещества
Нефтепродукты в косметическом производстве. Биологически активные вещества Понятие о единичных и симметрично-равных направлениях
Понятие о единичных и симметрично-равных направлениях Амины
Амины Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Азот и фосфор
Азот и фосфор