Содержание
- 2. Повторение пройденного Что такое атом? Что такое ион? Чем ион отличается от атома? Что такое степень
- 3. Способы классификации химических реакций По тепловому эффекту экзо (+)- и эндо (-) термические реакции По числу
- 4. Что такое степень окисления? Условный заряд атомов химических элементов в соединениях на основе представления о том,
- 5. Определение СО СО в простом веществе равна 0, например: F 2 Cl 2 O 2 СО
- 6. Алгоритм определения СО Запишем знаки химических элементов Определим число внешних электронов для каждого элемента Запишем эти
- 7. Определите степень окисления 1. Определите степень окисления каждого элемента в соединении: Al 2 (SO 4 )
- 8. Определение СО Большинство элементов могут проявлять переменную степень окисления в соединениях. Например, рассчитать степень окисления азота
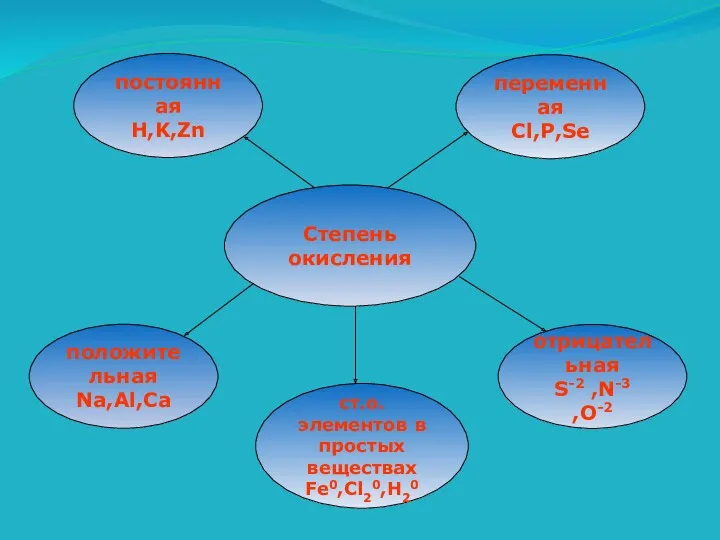
- 9. Степень окисления переменная Cl,P,Se отрицательная S-2 ,N-3 ,O-2 положительная Na,Al,Ca постоянная H,K,Zn ст.о. элементов в простых
- 10. Валентность и СО разные понятия!!! Валентность –это способность свободных его атомов (в более узком смысле —
- 11. Окислительно -восстановительные реакции Химические реакции , в результате которых происходит изменение степени окисления атомов химических элементов
- 12. Окислитель Восстановитель
- 13. Окислитель и восстановитель Окислителем называют реагент, который принимает электроны в ходе окислительно-восстановительной реакции. Восстановителем называют реагент,
- 14. Пример Напишем уравнение реакции: C0 + O20 = CO2 C0 – 4ē → C+4 O20 +
- 15. Запишите уравнения реакций 1. Al + S = Al 2 S 3 2. P + CL
- 16. ПРОЦЕСС ОКИСЛЕНИЯ И ВОССТАНОВЛЕНИЯ Окислением называют процесс отдачи электронов атомом, молекулой или ионом, который сопровождается повышением
- 17. К типичным восстановителям относятся простые вещества, атомы которых имеют малую электроотрицательность (металлы, водород, углерод, анионы, находящиеся
- 18. Правила определения функции соединения в окислительно-восстановительных реакциях. 1. Если элемент проявляет в соединении высшую степень окисления,
- 19. Составление окислительно-восстановительных реакций методом электронного баланса Метод основан на сравнении степеней окисления атомов в исходных веществах
- 20. Алгоритмическое предписание для составления уравнений окислительно-восстановительных реакций методом электронного баланса 1.Составить схему реакции. 2. Определить степени
- 21. Алгоритмическое предписание для составления уравнений окислительно-восстановительных реакций методом электронного баланса 5. Определить, какой элемент окисляется (его
- 22. Алгоритмическое предписание для составления уравнений окислительно-восстановительных реакций методом электронного баланса 8. Сбалансировать число электронов между окислителем
- 23. Взаимодействие сульфата железа (2) с перманганатом калия в кислой среде (H+ ). 1. Напишем уравнение реакции.
- 24. 2. Определим число электронов отданных восстановителем и принимаемых окислителем, а также коэффициенты при восстановителе и окислителе:
- 25. Пример. 1) Zn0 + H2+SO4 (разб) → Zn+2SO4 + H20 Zn0 - 2 ē → Zn+2
- 26. 3. Определим коэффициенты при исходных веществах и продуктах реакции, исходя из баланса атомов в левой и
- 27. Окисление и восстановление - две стороны единого процесса, и в соответствие с законом сохранения массы количество
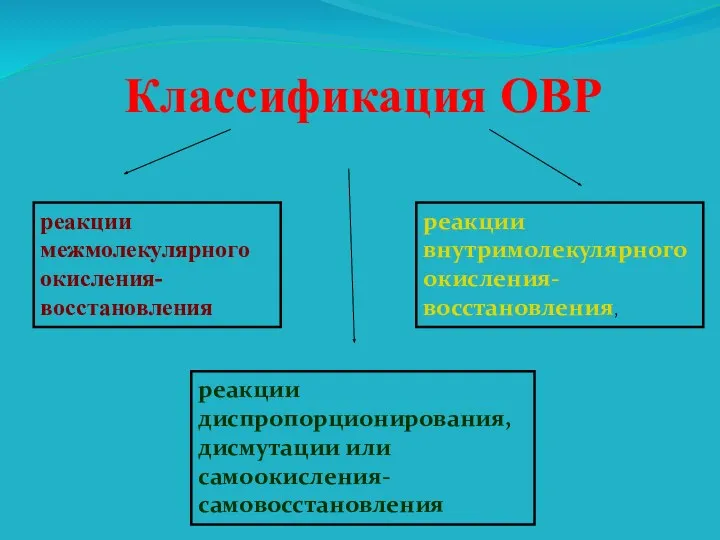
- 28. Классификация ОВР реакции межмолекулярного окисления-восстановления реакции внутримолекулярного окисления-восстановления, реакции диспропорционирования, дисмутации или самоокисления-самовосстановления
- 29. е Окислительно-восстановительные реакции в природе и жизни человека: 1. Фотосинтез 2.Реакции круговорота веществ в природе 3.
- 34. Скачать презентацию





























 Скорость химических реакций. Катализ. Химическое равновесие
Скорость химических реакций. Катализ. Химическое равновесие Классификация и свойства оксидов
Классификация и свойства оксидов Цветные сплавы
Цветные сплавы Водородная связь
Водородная связь Тяжелые металлы. Загрязнение токсичными металлами окружающей среды
Тяжелые металлы. Загрязнение токсичными металлами окружающей среды Виды вспомогательного оборудования химических производств
Виды вспомогательного оборудования химических производств Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Общие понятия неорганической химии. Химические свойства основных классов неорганических веществ. Лекция 3
Общие понятия неорганической химии. Химические свойства основных классов неорганических веществ. Лекция 3 Комплексономертиялық титрлеу. Дәріс № 6
Комплексономертиялық титрлеу. Дәріс № 6 Предельные углеводороды
Предельные углеводороды Физико-химические методы анализа. Лекция 1
Физико-химические методы анализа. Лекция 1 Теплові явища, що супроводжують розчинення речовин. Розчинення як фізико-хімічний процес. Кристалогідрати
Теплові явища, що супроводжують розчинення речовин. Розчинення як фізико-хімічний процес. Кристалогідрати Амины. Общая характеристика, номенклатура, изомерия. Получение. Физико-химические свойства. Отдельные представители
Амины. Общая характеристика, номенклатура, изомерия. Получение. Физико-химические свойства. Отдельные представители Роль хімії в пізнанні природи
Роль хімії в пізнанні природи Строение атома и химическая связь
Строение атома и химическая связь Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Алкадиены. Химические свойства алкадиенов
Алкадиены. Химические свойства алкадиенов Азотсодержащие органические соединения. Амины. Анилинароматический амин
Азотсодержащие органические соединения. Амины. Анилинароматический амин Вода на Земле. Строение молекулы воды
Вода на Земле. Строение молекулы воды Гидрогеохимия урана и тория
Гидрогеохимия урана и тория Общая характеристика элементов IБгруппы. Медь. Серебро. Золото
Общая характеристика элементов IБгруппы. Медь. Серебро. Золото D-элементы: хром, молибден, вольфрам
D-элементы: хром, молибден, вольфрам Alkynes
Alkynes Строение алканов. Физические и химические свойства алканов. Получение алканов
Строение алканов. Физические и химические свойства алканов. Получение алканов Карбоновые кислоты
Карбоновые кислоты Синтетические органические вещества
Синтетические органические вещества Окисление перманганатом и бихроматом калияорганических соединений. Уровень ЕГЭ
Окисление перманганатом и бихроматом калияорганических соединений. Уровень ЕГЭ