Теплові явища, що супроводжують розчинення речовин. Розчинення як фізико-хімічний процес. Кристалогідрати презентация
Содержание
- 2. Теплові ефекти розчинення При розчиненні відбуваються два процеси: Перший - руйнування хімічних зв'язків у кристалічних решітках;
- 3. Якщо при гідратації виділяється енергії більше, ніж витрачається на руйнування кристалічних решіток, то при розчиненні енергія
- 4. Розчинення амоній нітрату Розчинення кальцій хлориду Теплові явища під час розчинення речовин у воді
- 5. Бесіда. Яким процесом (фізичним чи хімічним) є розчинення? Чому розчинення є фізичним процесом? (При розчиненні відбувається
- 6. Процес розчинення Вода є чудовим розчинником для полярних і неполярних речовин, які мають заряджені часточки
- 8. Кристалогідрати Тверді речовини, які містять у своєму складі воду називають кристалогідратами, а вода що міститься в
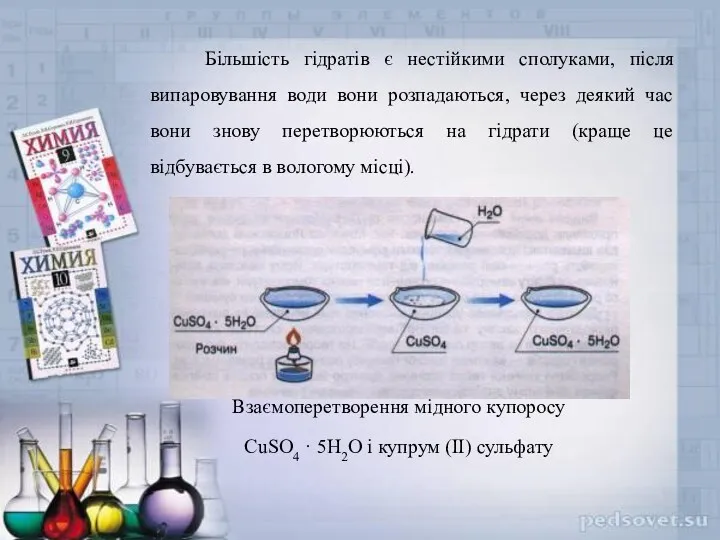
- 9. Більшість гідратів є нестійкими сполуками, після випаровування води вони розпадаються, через деякий час вони знову перетворюються
- 10. Деякі кристалогідрати і безводні солі: а) CuSO4 · 5H2O і безводний купрум (ІІ) сульфат; б) CoCl2
- 11. Розв'язування задач із застосуванням поняття про кристалогідрати 1. Кристалогідрат купрум (II) сульфату масою 5 г розчинили
- 12. Розв'язування задач із застосуванням поняття про кристалогідрати 2. Яку масу глауберової солі необхідно додати до 100
- 13. 3. 25 г мідного купоросу розчинили у 135 води. Визначте масову частку розчиненої речовини (M(CuSO4) =
- 14. Побудуйте графік розчинності мідного купоросу CuSO45H2О в воді за наступним даним: 10 20 30 40 50
- 15. Використовуючи графік визначте: Яку масу CuSO4 ·5H2 O можна розчинити в 100 мл води при 40
- 17. Скачать презентацию












 Основні принципи мас-спектрометрії
Основні принципи мас-спектрометрії General, specific properties are common to all matters
General, specific properties are common to all matters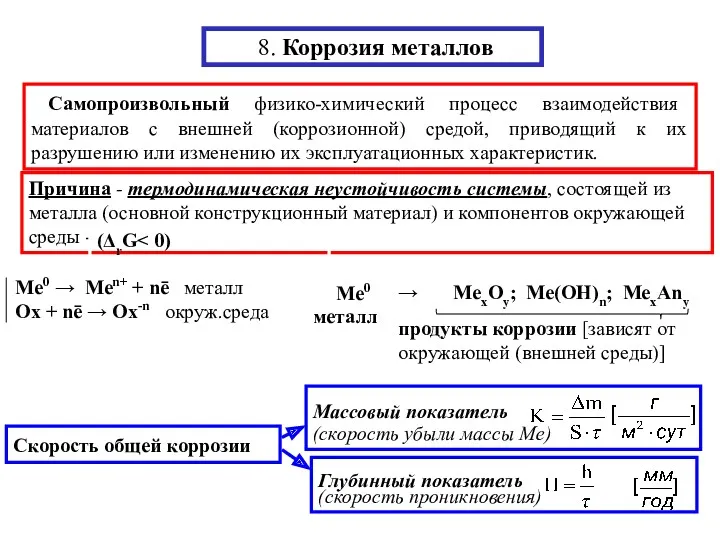 Коррозия металлов
Коррозия металлов Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Штучні і синтетичні волокна
Штучні і синтетичні волокна Метасоматические горные породы
Метасоматические горные породы Серебро
Серебро Көмірсутектерді пиролиздеу арқылы қарапайым олефиндерді алу
Көмірсутектерді пиролиздеу арқылы қарапайым олефиндерді алу Первоначальные представления об органических веществах
Первоначальные представления об органических веществах Металлы. Особенности строения. Классификация, физические и химические свойства
Металлы. Особенности строения. Классификация, физические и химические свойства Тотығу-тотықсыздану реакциялары. Тотығу және тотықсыздану
Тотығу-тотықсыздану реакциялары. Тотығу және тотықсыздану Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Carbohydrates (sugars)
Carbohydrates (sugars) Синтетические моющие средства. Механизм моющего действия
Синтетические моющие средства. Механизм моющего действия Рафинирование металлических расплавов
Рафинирование металлических расплавов Карбоновые кислоты
Карбоновые кислоты Адсорбция. Физическая и химическая адсорбция
Адсорбция. Физическая и химическая адсорбция Электронные представления в химии
Электронные представления в химии Требования к осадителю
Требования к осадителю Резина и её свойства . Полимеры и их использование
Резина и её свойства . Полимеры и их использование Фазовое равновесие
Фазовое равновесие Цветные маталлы и сплавы
Цветные маталлы и сплавы Каучук. Немного из истории
Каучук. Немного из истории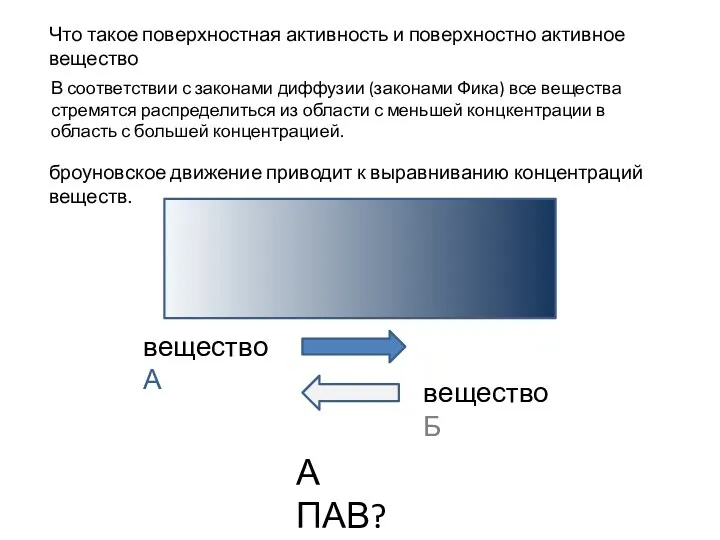 Поверхностная активность и поверхностно активное вещество
Поверхностная активность и поверхностно активное вещество От кулинарии — к кулинохимии
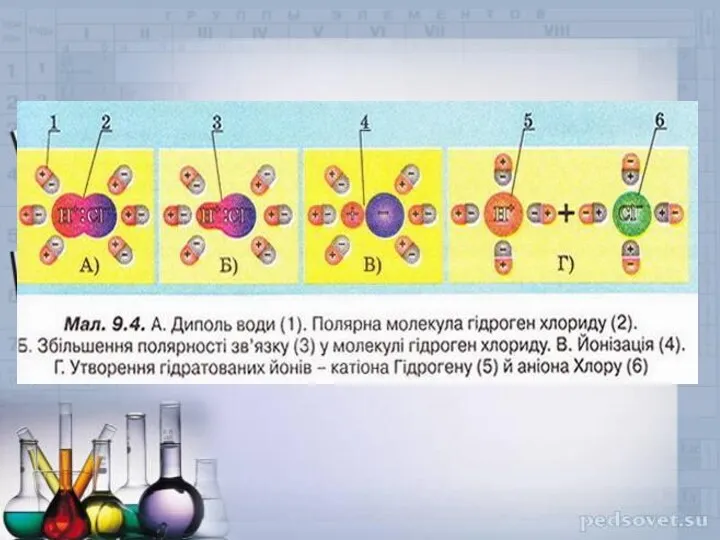
От кулинарии — к кулинохимии Образование ионов
Образование ионов Химиялық кинетика және электрохимия
Химиялық кинетика және электрохимия